在化学反应中,物质所含元素的化合价发生了变化的反应就是氧化还原反应。例:2Na +Cl2 ="=" 2NaCl,反应前后,Na、Cl的化合价发生了变化,该反应是氧化还原反应。根据化合价是否变化分析,下列反应属于氧化还原反应的是
| A.3H2 + N2==2NH3 |
| B.CaCO3 + 2HCl==CaCl2 + H2O + CO2↑ |
C.CaO+H2O Ca(OH)2 Ca(OH)2 |
| D.3NO2 + H2O ===2HNO3 +NO |
氯化铁溶液能与铜反应生成可溶性的氯化铜和氯化亚铁,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
请回答下列问题:
(1)步骤②③中实验操作的名称是 。
步骤②中发生了两个反应:2FeCl3+Fe = 3FeCl2和 ;
(2)步骤③中适量稀盐酸的标志是 ;
发生反应的化学方程式是 。
(3)该流程中可以循环、回收利用的物质是 。
下列对于物质变化的认识中,正确的是
| A.我们观察到的物质的宏观变化,本质上都是构成物质的微粒不断运动与变化的结果 |
| B.外界条件是导致物质变化的决定性因素 |
| C.物质发生化学变化时,微粒之间一定发生了相互作用,而物质发生物理变化时,微粒之间没有发生相互作用 |
| D.凡是伴随着能量的变化,一定是化学变化 |
已知 。一定量的Ca(HC03)2固体在密闭容器中受热分解(此过程CaCO3不分解)。下列图像表示该过程中某些量的变化趋势,其中错误的是
。一定量的Ca(HC03)2固体在密闭容器中受热分解(此过程CaCO3不分解)。下列图像表示该过程中某些量的变化趋势,其中错误的是
物质总是在不断运动变化着,请你判断下列哪一种变化与其它三种有着本质上的不同( )
| A.火药爆炸 | B.酒精挥发 | C.植物光合作用 | D.食醋除水垢 |
(1)某学习小组收集到一些铜绿(碱式碳酸铜)他们拟通过化学反应获得铜,根据下图资料,回答下列问题。
①碱式碳酸铜的物理性质之一是 。
②用稀硫酸、铁为原料将碱式碳酸铜转化为铜,反应的化学方程式是: 。
(2)另一小组收集了一些硫酸铁与硫酸亚铁的混合物,如果经实验测知,硫酸铁与硫酸亚铁混合物中含硫a﹪,则其中含铁的质量分数为 。
研究氢气、一氧化碳和二氧化碳具有重要意义.
(1)在汽车“催化转化器”内发生反应的化学方程式是:2NO+2CO N2+2CO2.某化学探究小组的同学为探究温度、催化剂的比表面积对化学反应速率的影响,设计了下列三组实验.
N2+2CO2.某化学探究小组的同学为探究温度、催化剂的比表面积对化学反应速率的影响,设计了下列三组实验.
| 实验编号 |
T/℃ |
NO初始浓度/g•L﹣1 |
CO初始浓度/g•L﹣1 |
催化剂的比表面积/m2•g﹣1 |
| Ⅰ |
280 |
0.036 |
0.162 |
82 |
| Ⅱ |
280 |
0.036 |
0.162 |
124 |
| Ⅲ |
350 |
0.036 |
0.162 |
124 |
(1)分析上表中实验数据,回答下列问题:探究温度对化学反应速率影响的实验是 (填写实验编号);研究催化剂的表面积对化学反应速率影响的实验是 (填写实验编号).
(2)在300℃、70MPa下,使用催化剂可由氢气和二氧化碳合成乙醇,同时生成水,写出反应的化学方程式 .
(3)燃料燃烧时产生的热量不同.已知在某温度下各种燃料燃烧时产生的热量见下表:
| 燃料 |
质量/g |
产物 |
产生的热量/KJ |
| 氢气 |
2 |
水蒸气 |
241.8 |
| 甲烷 |
16 |
二氧化碳气体和水蒸气 |
890.3 |
| 乙醇 |
46 |
二氧化碳气体和水蒸气 |
1367 |
分析表中数据,燃烧单位质量的上述燃料产生的热量由多到少的顺序是 (用化学式表示).
在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如下图所示。下列说法正确的是
| A.该反应是化合反应 |
| B.在该反应中丁一定没有参加化学反应 |
| C.丙可能是单质 |
| D.甲和乙的质量之和一定等于生成丙的质量 |
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如下所示:
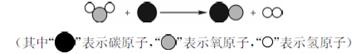 下列说法正确的是
下列说法正确的是
A.图中表示化合物的是 |
| B.该反应类型为化合反应 |
| C.该反应中反应物两种分子的个数比为3∶1 |
| D.反应前后原子的种类和数目保持不变 |
下列物质的用途与其依据的性质不符合的是()
| A. | 氧气用于急救病人--氧气能供给呼吸 |
| B. | 一氧化碳用于冶金工业--一氧化碳难溶于水 |
| C. | 石墨常用作电极--石墨具有导电性 |
| D. | 炭黑常用来制作碳素墨水--碳在常温下化学性质稳定 |
【改编】如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是
| A.该反应中两种反应物的质量比为1:3 |
| B.反应中元素的化合价没有改变 |
| C.反应中原子的种类和数目没有发生改变 |
| D.反应后生成了两种物质 |
《蜡烛的化学史》是英国科学家法拉第所著的传世科普经典,今天我们沿着大师的足迹进行探究.蜡烛是由石蜡和棉线组成的.
(1)石蜡放入水中,浮在水面上,说明石蜡的密度比水的密度 (填“大”或“小”).
(2)点燃蜡烛在其燃烧过程中,属于物理变化的是 .
(3)取一火柴梗,拿住一端迅速平放入火焰中约1秒后取出,可观察到两端变黑,中间无明显变化.说明火焰的 (填“外焰”“内焰”或“焰心”)部分温度最高.
(4)轻轻一吹即可使蜡烛熄灭,原因是 (填序号).
A.降低石蜡的着火点
B.隔绝了空气
C.温度降到了着火点以下.
(5)点燃一根直径为4cm的蜡烛,观察到烛芯周围有一杯状的烛油.蜡烛燃烧的质量与燃烧的时间呈现如图2所示的关系.
①据图判断蜡烛燃烧的化学反应速率是 (选填“稳定”或“不稳定”)
②烛芯周围的烛油没能发生燃烧的原因是 .
③事实上,人的呼吸与蜡烛的燃烧在某些化学原理论,人的呼吸与蜡烛的燃烧在某些化学原理上相似,请写出其中的一点 .
甲、乙、丙、丁四种物质,它们在密闭容器中反应前后质量的变化关系如下表所示.则下列说法错误的是
| 物质名称 |
甲 |
乙 |
丙 |
丁 |
| 反应前质量/g |
40 |
10 |
10 |
0 |
| 反应后质量/g |
6 |
M |
28 |
16 |
A.甲是化合物
B.乙可能是这个反应的催化剂
C.M=38
D.此反应基本类型为分解反应
物质的用途与性质密切相关,下列因果关系不成立的是
| A.因为镁燃烧能产生耀眼白光,所以可用于制作照明弹 |
| B.因为熟石灰能和酸发生反应,所以可用熟石灰改良酸性土壤 |
| C.铁制品表面涂“银粉”(铝粉)防生锈,是由于铝的化学性质比铁活泼 |
| D.因为甲醛能使蛋白质变性,起到防腐作用,所以甲醛水溶液可用于浸泡水产品 |
物质的化学变化
物质世界时时刻刻都在发生着变化。自然界中物质的变化通常分为两大类,即物理变化和化学变化。
(1)化学变化区别于物理变化的本质特征是 ;
(2)化学变化是有条件的,并且是可以控制的。人们在科学实验和日常生活中就有许多控制化学变化的事例。请参照举例,从化学角度说明下列事例中人们是控制化学变化的原理。
| 编号 |
事例 |
原理 |
| 举例 |
厨房中油锅着火,用锅盖盖灭 |
隔绝空气,使燃烧反应停止 |
| 事例1 |
实验室用过氧化氢制氧气时加入二氧化锰 |
|
| 事例2 |
易变质的食品采用真空包装,可以延长保质期 |
|
| 事例3 |
夏天,为防止食物变质,放在冰箱中 |
|
| 事例4 |
用鼓风机向煤炉中吹入空气,可以使炉火更旺 |
|
试题篮
()