溶液在生产和科研中具有广泛的用途。请回答下列问题:
(1)每年5月12日为全国“防灾减灾日”。家庭准备云南白药、碘酒、红药水、双氧水、高锰酸钾等杀菌消毒、止血、防感染的药品,是很好的预防措施。
①碘酒的溶剂为 ,双氧水中的溶质为(填化学式) 。
②高锰酸钾由(填数字) 种元素组成。
(2)在我国青海湖地区有一种说法:冬天捞碱,夏天晒盐。这里的碱指的是Na2CO3,盐指NaCl,两种物质的溶解度曲线如右图表示。
①10 ℃时,100 g水中最多溶解碳酸钠 g。 ②40 ℃时,碳酸钠的溶解度(填字母序号) 氯化钠的溶解度。
a.大于 b.等于 c.小于
③请根据两种物质的溶解度曲线图说明我国青海湖地区冬天捞碱的原因为 。
下图为A、B、C三种物质的溶解度曲线,请回答。
(1)M点表示的意义是 。
(2)t10C时,三种物质的溶解度由小到大依次为 ;t30C时,溶解度最大的是 。
(3)若把混在A中的少量C除去,应采用 方法;
(4)由t30C降至t10C时,三种物质中析出晶体最多的是 ;
(5)若把10g20%的A溶液稀释到10%,需加水的质量为 g;(计算写过程,以下相同)
水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)"生命吸管"(如右图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等。其中活性炭起到和过滤的作用。
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为。
(3)农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为g。
(4)根据下表回答问题。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度 /g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
| NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
77.3 |
①60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法正确的是(填字母序号)。
A.溶质的质量不变
B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变
D.可升高温度或增加溶剂
水和以水为溶剂制成的溶液,与人们的生活有着密切的关系。
(1)生理盐水中的溶剂是 。
(2)市售的一种罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动饮料罐使它们混合,饮料温度就会降低,这种固体物质可能是 (填字母)。
| A.烧碱 | B.食盐 | C.硝酸铵 | D.生石灰 |
(3)下图为a、b两种固体物质的溶解度曲线,请依据曲线图回答问题:
①在t3℃时,50g水中最多能够溶解a物质的质量是 ;
②在 ℃时,a物质的饱和溶液和b物质的饱和溶液中,溶质的质量分数相等。
③把100g质量分数为20%的a溶液从t3℃降温到t2℃,此时a溶液的质量分数是 。
(4)现有一瓶浓硫酸,标签如图所示。欲将该瓶浓硫酸完全稀释成20%的稀硫酸,需要水的质量是 g。 
某兴趣小组做了如下实验.
【实验一】提纯NaCl
请根据实验回答下列问题:
(1)操作①、②、③依次为下图中的(填序号) .
(2)若得到NaCl的产率比实际值偏低,则可能的原因是(填序号) .
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上
D.溶解11g含有泥沙的NaCl时,加入的水量不足
(3)用上述实验所得的氯化钠配制溶质质量分数为5%的氯化钠溶液50g,不需要的仪器为(填序号) .
A.量筒 B.天平 C.烧杯 D.漏斗 E.蒸发皿 F.玻璃棒 G.酒精灯
【实验二】溶解和结晶KNO3
请根据实验和KNO3溶解度曲线回答下列问题(水的密度以1g/mL计):
| 实验操作 |
实验结果 |
| 取100mL水,加入25gKNO3,搅拌,20℃ |
全部溶解,得溶液① |
| 再加Xg KNO3,搅拌,20℃ |
恰好饱和,得溶液② |
| 再加25g KNO3,搅拌,20℃ |
得溶液③ |
| 加热 |
全部溶解,得溶液④ |
| 冷却至20℃ |
晶体析出,得溶液⑤ |
(4)溶液③的质量为 ;一定属于不饱和溶液的是(填数字序号) ;溶质的质量分数一定相等的是(填序号) .
(5)析出晶体的质量为(填序号) .
A.25g B.X+25g C.X+100g.
甲、乙、丙三种固体物质的溶解度曲线如下图所示。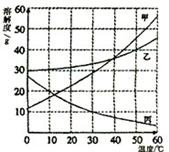
(1)30℃时,丙的溶解度是___________。
(2)20℃时,甲、乙、丙三种物质的溶解度按由大到小的顺序排列的是 。
(3)欲将20℃时丙不饱和溶液变为饱和溶液,可采用的方法是 (写出一种即可)。
(4)5℃时,取甲、乙、丙三种固体物质各20g分别加入盛有100g水的烧杯中,充分搅拌后得到的溶液,能够饱和的是_________________物质的溶液。又将三个烧杯中的混合物温度都升高到30℃,所得溶液溶质质量分数的大小关系是_______________。
(5)现要配制20℃时70g10%的甲溶液。该实验的部分操作如下图所示。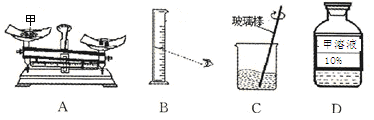
①需要称取甲的质量是________________,称量时图A出现了右盘低的现象,接下来的操作应该是____________________。
| A.左边的平衡螺丝向左调 | B.将游码向左移动 |
| C.右盘中减少砝码 | D.左盘中增加甲 |
②量取水时,如果按照图B的方法读数,会使配制的溶液溶质质量分数_______________(填“偏大”或“偏小”)。
③图C中用玻璃棒搅拌的作用是________________________。
实验室配制100g 10%的氯化钠溶液,请按要求回答问题。
(1)量时如果用质量为23.1g的烧杯盛放固体,在托盘天平上已放30g的砝码,则天平上的游码位置应是图中的__ __ (填字母)。 
(2)下列仪器中,量取水时需要用到d和____仪器,溶解时需要用到e和___仪器。
a.烧杯 b.10mL量筒 c.100mL量筒 d.滴管 e.玻璃棒 f.药匙 g.蒸发皿
(3)在粗盐提纯中,将氯化钠溶液蒸发至有较多量固体析出后,应 ,并用玻棒不断搅拌,利用余热将余下溶液蒸发至干。
(4)实验室中配好的溶液,应贴上标签密封放到试剂柜中保存。一定溶质质量分数的氯化钠溶液须密封保存的原因是________。
右图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题。
(1)t1℃时,100g水中溶解20g甲,溶液刚好饱和;那么,50g水中溶解 g乙,溶液达到饱和;
(2)t2℃时,比较两物质的溶解度大小: ;
(3)t1℃时,若要将甲物质的饱和溶液变为不饱和溶液,可采用的方法是
(写出一种即可);
(4)若要从甲中含有少量乙的混合溶液
中提纯甲,可用的方法是 。
归纳与整理是化学学习的一种重要方法。
(1)某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你来解决下列问题:
A.小红同学从某一欠收农田里取回一份土壤样品,如果检测结果呈酸性,从经济和可行方面考虑,那么要改良此土壤的酸性,应向农田里施加 (填化学式)。
B.小红同学用下图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应)。
I.为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成 。
II.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为: 。
III.为了验证反应③能够发生,你选择的物质是 。
a.Na2CO3 b.HCl c.FeCl3 d.Ba(NO3)2
C.请你设计一个实验除去FeCl2溶液中少量的CuCl2,请写出主要操作步骤和化学方程式。实验主要操作步骤: 、 ,
化学方程式: 。
(2)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
①25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为 g。
②要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是 。
③现有操作步骤: a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是 (填字母序号)。
④将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数 (填“变大”、“变小”或“不变”)。
⑤向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是 。
水是生命之源,扬州是运河之城,也是南水北调的起点。请根据题意回答下列有关水溶液的问题。
(一)将10克NaOH固体完全溶解在40毫升水中(水的密度为1g/cm3),所配溶液中溶质的质量分数为 。某同学在配制过程中,量取水时仰视读数(其它操作均正确),其所配氢氧化钠溶液中溶质的质量分数将 (填“偏大”或“偏小”)。另一位同学称取NaOH时,由于操作不熟练,花了较长时间,那么,他所配氢氧化钠溶液中溶质的质量分数将 。(填“偏大”或“偏小”)。
(二)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:

(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为 g。
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是 。
(3)现有操作步骤: a.溶解 b.过滤 c.降温结晶 d.加热浓缩。若甲固体中含有少量乙,则提纯甲的操作步骤是 (填字母序号)。
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数 (填“变大”、“变小”或“不变”)。
(5)向100g35℃的水中加入48g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是 。
小明看到妈妈用洗涤剂洗衣服上的油污时,联想到自己学习过的洗涤方法:①用汽油除油污;②用酒精洗掉沥青;③用炉具清洁剂除油污;④用汽油洗掉碘;⑤用肥皂洗掉衣服上的油渍;⑥用稀盐酸除水垢。请从洗涤原理的角度选择适当的分类标准对上述洗涤方法加以分类,你的分类标准是(1) ,包含的方法是(2) (填序号)。
(4分)右图是 A、B、C三种物质的溶解度曲线,回答下列问题:
(1)________℃时,A、C的溶解度相等.
(2)若A物质中混有少量B物质,可用 的方法得到较纯的A物质.
(3)在t2℃时,将一定量B物质的饱和溶液恒温蒸发10g水,可析出晶体B(不含结晶水) g.
(4)现将t3℃时A、B、C三种物质的饱和溶液分别降至t1℃,所得溶液的溶质质量分数由小到大的顺序是_______________(用A、B、C填空)
化学与生活息息相关,请运用化学知识回答下列问题:
(1)测土壤溶液的酸碱度常用 ;
(2)检验软水和硬水常用 ;
(3)在水的净化中常用的除臭剂是 ;
(4)用分子的知识解释“缉毒犬”能够辨别气味,发现毒品的原因是 .
水是重要的物质,在实验室中常用于溶解物质、配制溶液.
(1)向50mL水(密度为1g/mL)中溶解一定量KNO3固体的操作如下,请根据如图实验现象和溶解度曲线回答.
①A、B、C中一定是饱和溶液的是 ,一定是不饱和溶液的是 (填字母);
②当x= g时,B中恰好没有固体剩余;
③硝酸钾从溶液中析出晶体常用 方法.
(2)现用溶质质量分数为8%的氯化钠溶液和水配制50g质量分数为4%的氯化钠溶液。根据下列仪器,请回答下列问题.
①计算:需要8%的氯化钠溶液的质量为_________克,需要水 克
②上面的仪器中除D、E外,还必须选用的仪器有 (填字母);E的作用是 。
2012年3月22日是“世界水日”。水与人类的生活和生产密切相关。请回答以下问题:
(1)生理盐水中的溶质是 (填化学式)。
(2)下列洗涤方法中,利用乳化原理的是 ( )
A.用食醋除水垢 B.用稀盐酸除铜粉中的铁粉
C.用汽油清洗油渍 D.用洗洁精清洗油污
(3)课外活动中,同学们玩起了以水为主题的“化学反应接龙”游戏。游戏的规则为:用前一个反应的一种生成物作为下一个反应的反应物,并按序号和要求的基本反应类型循环,如上图a所示。仿照示例完成下列反应的化学方程式。
示例:①分解反应:电解水2H2O 2H2↑+O2↑
2H2↑+O2↑
②置换反应
③化合反应
(4)右图b是A、B、C三种物质(均不含结晶水)在水中的溶解度曲线。
①t1℃时,A、B、C三种物质中溶解度最大的是 ;
②t2℃时,将C物质的饱和溶液转化为不饱和溶液的方法有 (填一种)。
试题篮
()