某工厂生产高锰酸钾的流程如图所示,请回答下列问题:
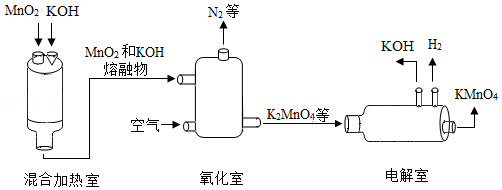
(1)“混合加热室”发生的主要是 (填“物理变化”或“化学变化”)。
(2)“电解室”反应中,反应前后化合价发生变化的元素有 (写元素符号)。
(3)生产流程中可循环利用的物质是 (写化学式)。
(4)写出氧化室中发生反应的化学方程式: 。
(5)取47.4g高锰酸钾,加热一段时间后停止,共收集到3.2g氧气,计算剩余固体中氧元素的质量分数是 (计算结果保留到0.1%)。
海洋是一个巨大的资源宝库。海水资源综合利用的部分途径如图。
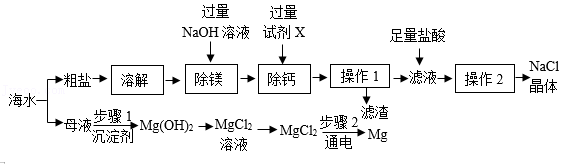
已知:粗盐中的杂质有泥沙、MgCl2、CaCl2,流程中部分操作及试剂已省略。
(1)试剂X的作用是除去粗盐中的Ca2+,则试剂X为 (填化学式)。
(2)“操作1”中玻璃棒的作用是 ,“操作2”的名称为 。
(3)滤渣中除泥沙外,还含有 。
(4)实际生产中,步骤1常选用 作为沉淀剂。
(5)步骤2需电解 状态的MgCl2以获得金属镁。
真空热还原法生产钙的主要转化过程如图:

(1)石灰石的主要成分是 。
(2)Ⅱ中反应有两种产物,固体X一定含有氧元素和铝元素,从元素守恒角度说明理由 。
(3)装置Ⅲ中发生的是 (填“物理”或“化学”)变化。
某兴趣小组利用废镍材料(含有金属Ni及少量Fe、Ag)探究相关物质的性质并回收镍,设计流程如图所示(部分产物略去)
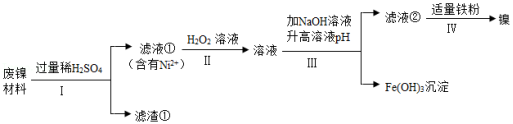
查阅资料:a.H 2O 2溶液可将Fe 2+转化为Fe 3+。
b.Fe 3+、Ni 2+转化为对应的氢氧化物沉淀时,溶液pH有如图关系:

(1)步骤Ⅰ的操作为 。
(2)滤渣①的成分为 。
(3)单质Fe参与反应的化学方程式为 (任写一个)。
(4)滤液②中有Ni 2+、无Fe 3+,则滤液②pH可能为 (填序号)。
A.pH=1
B.pH=2
C.pH=6
D.pH=10
(5)Ni、Fe、Ag三种金属的活动性由强到弱的顺序为 。
CO、CO 2和CaCO 3的转化关系如图所示。下列说法错误的是( )

| A. |
①可通过物质的还原性实现 |
| B. |
②可通过物质的可燃性实现 |
| C. |
③可通过与澄清石灰水反应实现 |
| D. |
④可通过分解反应实现 |
在给定条件下,下列选项所示的物质间转化能实现的是( )
| A. |
Cu |
| B. |
S |
| C. |
Fe 3O 4 |
| D. |
NaOH溶液 |
航空航天技术是一个国家科技、工业和国防实力的重要体现。南京理工大学陈光教授团队研究成功的"PST高温TiAl合金单晶"大幅度提高了耐高温性能,显著改善了材料塑性,对于新型轻质高温结构材料的发展和应用具有非常重要的意义。"PST TiAl单晶"实现了高强高塑的优异结合,持久寿命优于已经成功应用于GEnx发动机的4822合金1~2个数量级,有望将目前TiAl合金的使用温度从650~750℃提高到900℃以上,其抗压能力是第四代单晶合金的3倍,有了这种材料技术,中国也能够制造出世界一流的航空发动机。
(1)关于TiAl合金单晶的说法错误的是 。
A.TiAl合金属于单质
B."PST TiAl单晶"密度小、耐高温、强度大、可塑性强
C."PST TiAl单晶"持久寿命明显优于4822合金
D.钛和钛合金被认为是21世纪的重要金属材料,医疗上可用来制造人造骨等
(2)工业上常用铝土矿(主要成分为Al 2O 3,含Fe 2O 3杂质)为原料冶炼铝,工艺流程如图。请回答下列问题。
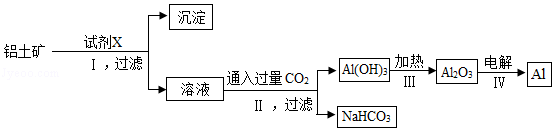
已知:氧化铝与酸、碱都能发生反应;
氧化铝与氢氧化钠溶液反应的化学方程式为Al 2O 3+2NaOH═2NaAlO 2+H 2O。
①试剂X是 (填"氢氧化钠溶液"或"盐酸"),反应Ⅰ后过滤所得的沉淀是 。
②Ⅱ中反应的化学方程式是 ;
③列举产物NaHCO 3的一种用途 ;
④电解氧化铝的化学方程式是 。
海水是一种重要资源,利用海水可制取镁等物质,某化学兴趣小组的同学设计了如下实验流程进行实验:
分析该流程图,下列说法错误的是( )
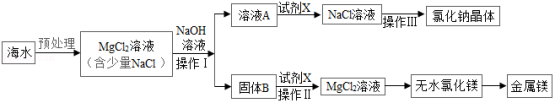
A.操作Ⅰ,操作Ⅲ都需用到的玻璃仪器是玻璃棒
B.固体B是Mg(OH. 2,试剂X是盐酸
C.加入NaOH溶液应过量,其目的是使MgCl 2完全反应
D.处理等量海水,若将NaOH溶液换成石灰乳,既能节约成本又能提高镁的产量
回收利用废旧金属具有重要意义。某机械厂金属废料的成分是Zn、Cu、ZnO和CuO,某化学小组利用该金属废料回收铜并制取氧化锌和硫酸铜。请回答下列问题。
【活动一】回收铜并制取氧化锌,实验方案如图:
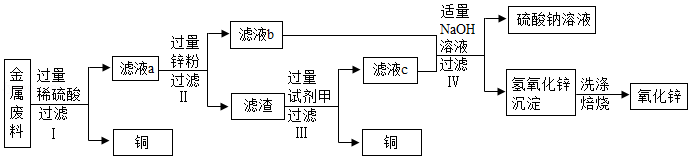
(1)步骤Ⅰ所得滤液a中溶质的成分是 (填写化学式)。
(2)步骤Ⅲ加入试剂甲的名称是 。
(3)步骤Ⅳ加入适量NaOH溶液的目的是 。
【活动二】利用活动一回收的铜制取硫酸铜,设计方案如下:
方案A:Cu CuO CuSO 4
方案B:Cu CuSO 4
【信息】Cu+2H 2SO 4(浓) CuSO 4+SO 2↑+2H 2O
(4)方案A中氧化铜与稀硫酸反应的化学方程式为 CuO+H 2 SO 4 = CuSO 4 +H 2 O 。
(5)小组同学从绿色化学的视角分析方案B不合理,理由是 (写出一条即可)。
在钢铁工业推进碳减排、碳捕集的过程中,化学发挥了重要作用。
(1)“焦炭炼钢”是先将铁精矿(Fe2O3)和焦炭同时加入高炉,鼓入热空气,充分反应后得到生铁,再将生铁转移至炼钢炉中炼制得钢。
①高炉炼铁的主要反应原理是在高温下, 夺取了Fe2O3里的氧将铁还原出来。
②某钢铁厂每年需要向高炉中加入120万吨的焦炭,若加入的焦炭全部转化为CO2,则该钢铁厂每年排放CO2的质量为 万吨。
(2)为了实现CO2的捕集利用,我国研制出一种多功能复合催化剂(含NaFe3O4),能将CO2转化为汽油,转化步骤如下:
CO2 CO
CO (CH2)n
(CH2)n 汽油
汽油
①步骤Ⅰ除生成CO外,还生成另一种氧化物。该氧化物的化学式是 。
②下列说法错误的是 (填字母)。
a.所得汽油中含有C、H两种元素
b.NaFe3O4中O为﹣2价,Fe为+3价
c.上述转化不仅有利于CO2减排,还可以减轻人类对化石能源的需求
(3)一种以“氢能炼钢”替代“焦炭炼钢”的工艺流程如图所示。

①高温下,用H2炼铁时反应的化学方程式为 。
②跟“焦炭炼钢”工艺相比,“氢能炼钢”的主要优点有 。
③从物质组成的角度,说明向炼钢炉中加入废钢的目的: 。
绘制知识网络是化学学习的一种有效方法,元素单质及其化合物的“价态—类别”二维图就是其中的网络图之一。如图是铁及其化合物的“价态—类别”二维图,下列有关说法或方程式正确的是( )
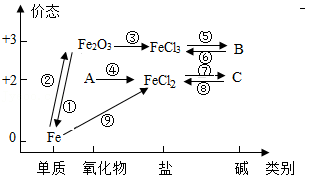
A.物质A的名称是氧化铁
B.①反应可能是Fe2O3+3Al 3AlO+2Fe
3AlO+2Fe
C.⑤反应可能是FeCl3+3NaOH═Fe(OH)3↓+3NaCl
D.⑤~⑨全部是复分解反应
古诗《石灰吟》:“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑不怕,要留清白在人间。”中蕴含了如图所示三种物质间的相互转化关系,下列说法不正确的是( )
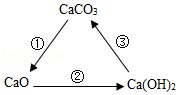
A.CaO俗名叫生石灰,是一种氧化物
B.“烈火焚烧若等闲”描述的是反应①的变化
C.反应②发生时,会放出热量
D.反应③是改良酸性土壤的原理
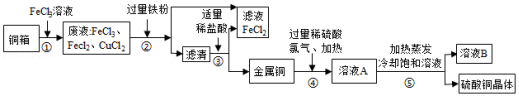
电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),如图是某兴趣小组设计的处理该生产过程中产生废液的流程图,据如图回答下列问题:
查阅资料:2Cu+2H2SO4+O2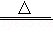 2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是 (写化学式)。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是 ,步骤②还需要进行的实验操作是 。
(3)步骤③加入适量稀盐酸充分反应。当观察到 现象时,说明滤液中只剩下铜。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是 。
(5)溶液B中含有的溶质是 。
人类常利用化学反应得到所需要的物质。如图是X、Y、Z、W四种物质的转化关系(都能通过一步反应实现),则X、Y、Z、W依次可能是( )

A.C、CO、CO2、H2CO3
B.H2O2、O2、H2O、H2
C.CaO、Ca(OH)2、CaCl2、CaCO3
D.Cu、CuO、Cu(OH)2、CuSO4
试题篮
()