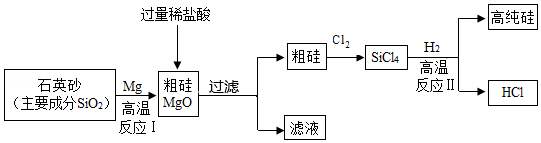
制造芯片的基材主要是高纯硅。如图是制备高纯硅的一种工艺流程:
回答下列问题:
(1)反应Ⅰ的化学方程式是 。
(2)过滤所得粗硅应充分洗涤,以除去表面可能吸附的HCl和 (填化学式)。
(3)反应Ⅱ的基本类型属于 ;反应Ⅱ要在无氧气环境中进行,原因是 (答出一种即可)。
(4)上述生产流程中,可以循环利用的物质是 (填化学式)。
某化工厂按如下步骤进行生产:
(1)以煤为燃料煅烧石灰石;(2)用饱和Na2CO3溶液充分吸收(1)中产生的CO2气体(Na2CO3+CO2+H2O=2NaHCO3;(3)使(1)中产生的CaO与水反应;(4)熟石灰与碳酸钠溶液反应.该厂生产过程中所涉及的物质有①石灰石;②碳酸钠;③碳酸氢钠;④烧碱;⑤二氧化碳;⑥熟石灰( )
A.起始原料是①③B.起始原料是②⑥
C.最终产品是⑤⑥D.最终产品是③④
内江拥有中国西南地区最大的再生资源基地,可回收处理大量废旧塑料电器及玻璃等,某品牌电器的废旧电路板中含有Fe、Cu、Ag、Ni(镍,银白色金属) 等金属,如下图是某车间回收部分金属的工艺流程。已知,2Cu+O2+2H2SO4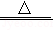 2CuSO4+2H2O。
2CuSO4+2H2O。
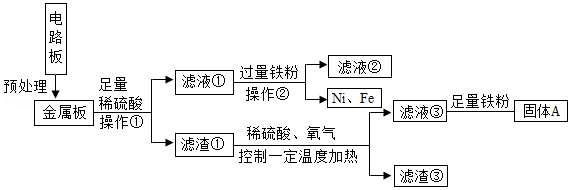
回答下列问题。
(1)操作①中,使用的玻璃仪器除烧杯、玻璃棒外,还需 ;
(2)滤渣③中含有的金属是 ;
(3)根据以上工艺流程图,可以得出Ni、Fe的金属活动性强弱顺序是Ni Fe(填“>”或“<”)。
(4)滤液③中加入足量铁粉的主要目的是 ,固体A除主要含有铜外,还含有一定量的铁,为了进一步提纯铜,可以向固体A中加入适量的稀硫酸,发生反应的化学方程式为 ;
(5)相比于直接焚烧废旧电路板回收金属,该工艺流程的主要优点是 。
氧化锌广泛用于皮肤病的治疗,工业氧化锌常含有少量杂质(CuO、FeO、SiO2等)不能直接使用。提纯、净化氧化锌的简易流程如图所示:

参考资料:SiO2既不溶于水也不与酸反应
(1)反应器Ⅰ中加入足量稀硫酸,充分反应后,生成硫酸盐的化学式为 ;
(2)残渣中除金属锌外,还有 ;
(3)操作一、操作二和操作三采用的分离方法是 ;
(4)操作四发生反应的化学方程式为 。
氢基熔融冶金技术是利用氢作为还原剂代替碳还原剂,从而实现减少CO2排放的目的,实现低碳冶金。氢基熔融还原生产高纯铸造生铁的主要流程如图所示(部分略去)。
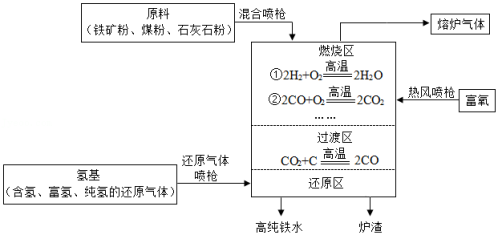
(1)燃烧区的作用是 ,燃烧区发生燃烧反应的物质还有 (填化学式)。
(2)还原区的反应除3CO+Fe2O3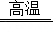 2Fe+3CO2,另一主要反应的化学方程式是 。
2Fe+3CO2,另一主要反应的化学方程式是 。
(3)从环境保护角度,与高炉炼铁技术相比,氢基熔融冶金技术的优点是 。
工业上合成 NH 3 的工艺流程可简化为:
(1)工业上制取 N2 时所用的廉价、易得的原料是 ;
(2)用焦炭和水蒸气制取氢气的反应过程为:C+H2O CO+H2,CO+H2O CO2+H2
其中发生还原反应的物质是 ;
(3)在高温、高压、催化剂存在的条件下,生成 NH3的化学方程式为 ;
(4)将降温分离出的 N 2、H 2 送回合成塔的目的是 ;
A. 充分利用原料 B. 防止氮气污染空气.
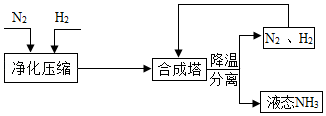
某矿石主要成分是MgO,含少量的Fe2O3、CuO和SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
回答下列问题:
(1)步骤①和步骤②均用到的操作是 。
(2)溶液A中所含的阳离子有Fe3+、Cu2+、Mg2+和 (填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:
对应离子 |
Fe3+ |
Cu2+ |
Mg2+ |
开始沉淀时的pH |
1.9 |
4.2 |
9.1 |
完全沉淀时的pH |
3.2 |
6.7 |
11.1 |
步骤②加入熟石灰,调节溶液的pH范围为 ,固体C中所含成分的化学式为 。
(4)步骤③制得Mg(OH)2的化学方程式为 。
海水提取粗盐后的母液还可用来提取金属镁,其流程如图:

回答下列问题:
(1)如在实验室进行操作a,使用玻璃棒的目的是 ,沉淀A的化学式是 。
(2)用贝壳生产石灰乳,发生反应的化学方程式有: 、 。
(3)由MgCl2溶液得到MgCl2•6H2O晶体,需要进行的实验操作有: 、 、过滤、洗涤。
(4)用203t MgCl2•6H2O晶体最多能制备金属镁 t。
绘制知识网络是化学学习的一种有效方法,元素单质及其化合物的“价态—类别”二维图就是其中的网络图之一。如图是铁及其化合物的“价态—类别”二维图,下列有关说法或方程式正确的是( )
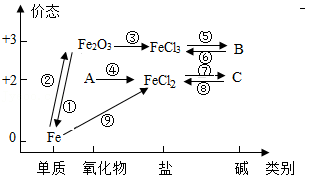
A.物质A的名称是氧化铁
B.①反应可能是Fe2O3+3Al 3AlO+2Fe
3AlO+2Fe
C.⑤反应可能是FeCl3+3NaOH═Fe(OH)3↓+3NaCl
D.⑤~⑨全部是复分解反应
古诗《石灰吟》:“千锤万凿出深山,烈火焚烧若等闲。粉身碎骨浑不怕,要留清白在人间。”中蕴含了如图所示三种物质间的相互转化关系,下列说法不正确的是( )
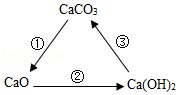
A.CaO俗名叫生石灰,是一种氧化物
B.“烈火焚烧若等闲”描述的是反应①的变化
C.反应②发生时,会放出热量
D.反应③是改良酸性土壤的原理
电子工业上制造铜电路板,常用30%的FeCl3溶液腐蚀镀铜电路板上的铜箔(Cu),如图是某兴趣小组设计的处理该生产过程中产生废液的流程图,据如图回答下列问题:
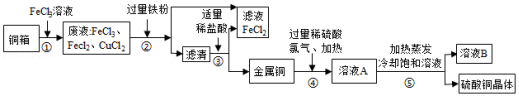
查阅资料:2Cu+2H2SO4+O2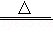 2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
2CuSO4+2H2O;2FeCl3+Fe═3FeCl2
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种溶质,据此可判断步骤①中铜与FeCl3反应生成的两种产物是 (写化学式)。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是 ,步骤②还需要进行的实验操作是 。
(3)步骤③加入适量稀盐酸充分反应。当观察到 现象时,说明滤液中只剩下铜。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是 。
(5)溶液B中含有的溶质是 。
人类常利用化学反应得到所需要的物质。如图是X、Y、Z、W四种物质的转化关系(都能通过一步反应实现),则X、Y、Z、W依次可能是( )

A.C、CO、CO2、H2CO3
B.H2O2、O2、H2O、H2
C.CaO、Ca(OH)2、CaCl2、CaCO3
D.Cu、CuO、Cu(OH)2、CuSO4
氯化亚铜CuCl是一种难溶于水和乙醇且在潮湿空气中易变质的物质,广泛应用于冶金、电镀、医药等行业、CuCl的制备流程如图:
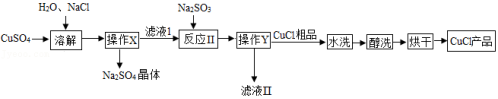
(1)"操作Y"名称是 。
(2)CuCl中铜元素的化合价为 。
(3)请配平"反应Ⅱ"的化学方程式: 。
(4)在"滤液Ⅱ"中可以循环利用的物质(水除外)是 。(填化学式)
(5)"醇洗"的目的是 ,防止后续过程中氯化亚铜变质。
2019年诺贝尔化学奖授予对锂离子电池研究作出贡献的三位科学家。如图是从钴酸锂废极片[主要成分为钴酸锂(LiCoO2)]中回收得到Co2O3和Li2CO3的一种工艺流程。
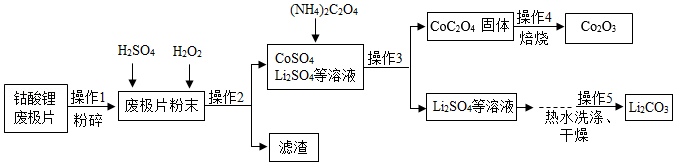
(1)操作1中,粉碎废极片的目的是 ;
(2)实验室中完成操作2时,需用到的玻璃仪器是 (填一种即可);
(3)操作4中,在高温条件下,CoC2O4在空气中反应生成Co2O3和二氧化碳,化学方程式为 ;
(4)操作5中,Li2CO3晶体用热水洗涤比用冷水洗涤损耗更少,说明Li2CO3的溶解度随温度升高而 。
试题篮
()