海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图(如图)回答问题:
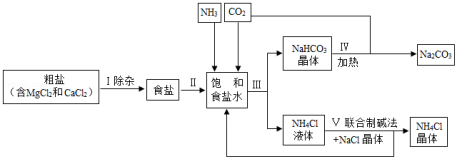
(1)步骤Ⅰ除杂中,常见的方法有两种:一是物理方法,即用NaCl溶液浸洗粗盐,溶解除去其中的可溶性杂质,则浸洗溶液应选用NaCl的 (填“饱和”或“不饱和”)溶液;二是化学方法,操作步骤依次为:加水溶解→加过量试剂①→加过量试剂②→过滤→加适量盐酸,以下试剂①②组合选用合理的是 。
A.①Ca(OH)2②Na2CO3
B.①Na2CO3②Ca(OH)2
C.①KOH②Na2CO3
D.①NaOH②Na2CO3
(2)步骤Ⅲ先向饱和食盐水中通入氨气,再通入二氧化碳,这样做的目的是 ,写出步骤Ⅲ反应的化学方程式 。
(3)步骤Ⅳ发生的反应属于 反应(填基本反应类型)。
(4)我国化学家侯德榜创立的联合制碱法的优点有 。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
硫酸亚铁是一种重要的补铁剂。实验室以废铁屑(含少量Fe2O3)为原料制备硫酸亚铁晶体的流程如图所示:
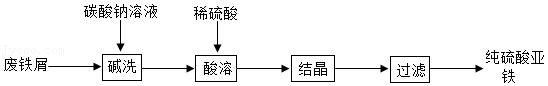
已知:铁与硫酸铁反应的化学方程式为Fe+Fe2(SO4)3═3FeSO4。
(1)“碱洗”是为了洗去铁屑表面的油污。用热的碳酸钠溶液浸泡,过滤,再用蒸馏水洗涤2~3次。取最后一次洗涤液,测其pH,若pH= ,说明洗涤液中无碳酸钠。
(2)“酸溶”是向“碱洗”过的铁屑中加入过量稀硫酸。
①写出铁与稀硫酸反应的化学方程式: 。
②所用硫酸溶液浓度不能太稀,原因是 。
③废铁屑中的少量Fe2O3不需要进行除杂处理,原因是 。
(3)“结晶”的相关操作依次为:蒸发浓缩、降温结晶。蒸发浓缩的目的是 ,便于结晶。
(4)含量测定:准确称取制得的硫酸亚铁样品2.82g于锥形瓶中,加蒸馏水完全溶解,加入稀硫酸,滴加溶质质量分数为1.58%的高锰酸钾溶液,当恰好完全反应时,消耗高锰酸钾溶液的体积为20.00mL(该高锰酸钾溶液密度近似为1g•mL﹣1)。列式计算该样品中硫酸亚铁的含量(结果用百分数表示,保留一位小数)。
已知:高锰酸钾与硫酸亚铁反应的化学方程式为10FeSO4+2KMnO4+8H2SO4═5Fe2(SO4)3+2MnSO4+K2SO4+8H2O(相对分子质量:FeSO4=152,KMnO4=158)
制造芯片的基材主要是高纯硅。如图是制备高纯硅的一种工艺流程:
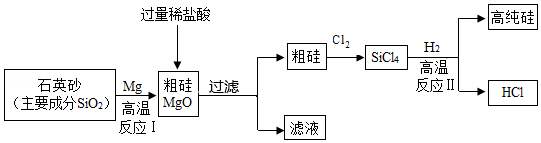
回答下列问题:
(1)反应Ⅰ的化学方程式是 。
(2)过滤所得粗硅应充分洗涤,以除去表面可能吸附的HCl和 (填化学式)。
(3)反应Ⅱ的基本类型属于 ;反应Ⅱ要在无氧气环境中进行,原因是 (答出一种即可)。
(4)上述生产流程中,可以循环利用的物质是 (填化学式)。
如图是某化工企业利用“侯氏制碱法”生产纯碱的部分工艺流程示意图:
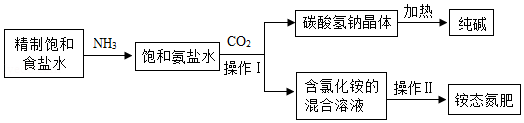
查阅资料知:①NH4Cl NH3↑+HCl↑;②氨气极易溶于水,氨水呈碱性。
(1)检验食盐水是否饱和的方法是 。
(2)操作Ⅰ的名称是 。实验室进行此操作时,玻璃棒的作用是 。
(3)“侯氏制碱法”中,向饱和氨盐水中通入足量的CO2,使氨气、水、NaCl和CO2反应生成NaHCO3等,该反应的化学方程式为 ;先通氨气形成饱和氨盐水,后加压通入二氧化碳,这样操作的目的是 。
(4)处理含氯化铵混合溶液时,不直接加热蒸干得到氯化铵固体的原因是 。
回答下列问题。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如图:
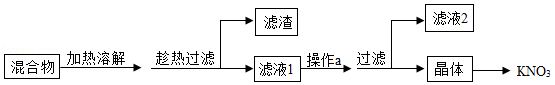
①结合如表分析,趁热过滤的原因是 。
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
KNO3 |
13.3 |
31.6 |
63.9 |
110 |
169 |
|
②操作a的名称是 。
③滤液2的溶质是 。
(2)A~D为初中化学常见物质,A、D为金属,在常温下通过如图所示转化可获取硝酸钾。回答下列问题。
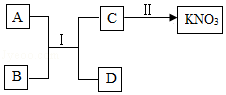
①反应Ⅰ能发生的原因是 。
②若D为银白色贵重金属,则反应i的化学方程式是 ,基本反应类型是 。
③一步实现反应Ⅱ,能否加入氯化钾?判断并说明理由 。
④硝酸钾可作化肥,能供给作物两种养分,属于 肥料。
如图所示,是小科建构的铜及其化合物之间相互转化的关系图。
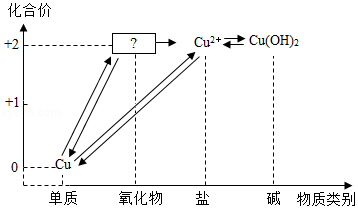
(1)写出图中“?”处物质的化学式 。
(2)要一步实现图中“Cu→Cu2+”的转化,可将铜加入适量的某种盐溶液中,则该溶液的溶质是 。
(3)根据图中的转化关系,利用硝酸铜溶液制备纯净的硫酸铜晶体。请设计一个实验方案,要求写出主要操
作步骤及所需要的试剂 。
一水硫酸四氨合铜的化学式为[Cu(NH3)4]SO4•H2O,是一种高效、安全的杀菌剂。它在乙醇﹣﹣水混合溶剂中的溶解度随乙醇体积分数的变化曲线如图甲所示。小明在实验室以氧化铜为主要原料合成该物质,他设计的合成路线如图乙所示:

(1)溶液A中一定存在的溶质为 。
(2)溶液B中含硫酸四氨合铜,“一系列操作”是指向溶液B中加入适量 、过滤、洗涤、干燥等。
以FeSO4•7H2O为原料制备铁红(Fe2O3)的一种方法如图:

已知“沉淀”时的主要反应为:2FeSO4+H2O2+2H2O═2FeO(OH)↓+2H2SO4
(1)FeO(OH)中铁元素的化合价为 。FeO(OH)可表示为mFe2O3•nFe(OH)3, 。
(2)“沉淀”时需控制溶液的pH与反应的温度。
①“沉淀”时调节溶液的初始pH约为4,过程中应始终保持溶液的pH为3.0~4.5,需不断加入物质Z调节溶液的pH,Z应具备的性质有 (填字母)。
A.能与酸反应
B.能与碱反应
C.不与FeO(OH)反应
②“沉淀”时反应温度不宜过高,其原因是 。
(3)“过滤”后需对固体进行洗涤与干燥。洗涤时被除去的沾于固体表面的阴离子为 (填离子符号)。
(4)“煅烧”时反应的化学方程式为 。
(5)如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。煅烧温度较低时,产品中Fe2O3质量分数较低,其原因是 。当煅烧温度达800℃时,继续升高温度,产品中Fe2O3质量分数降低,且铁元素质量分数升高,所得产品发黑,其可能原因是 。

(6)用该方法制备Fe2O3,计算理论上13.9t FeSO4•7H2O(相对分子质量为278)可制得Fe2O3的质量(写出计算过程)。
硼及其化合物在现代工农业、医学、国防中有着重要的应用价值。利用硼镁矿可制备硼,工艺流程如图所示。请回答下列问题:

(1)B2O3中B元素的化合价为 。
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是 ;回收副产物Mg(OH)2可制得流程 的反应物。
(3)H3BO3加热分解只生成两种氧化物,流程②的化学反应方程式为 。
(4)根据流程③的化学反应方程式:B2O3+3Mg 2B+3MgO,理论上制备1.1吨的硼,需消耗镁多少吨写出计算过程)?
2020年6月23日,我国长征五号B运载火箭搭载第55颗北斗导航卫星发射成功,北斗三号全球卫星导航系统星座部署全面完成。
Ⅰ.火箭中液氢燃料通过氢泵涡轮高速输送到发动机燃烧室,与液氧混合燃烧产生推动力。该反应的化学方程式为 。
Ⅱ.人造地球卫星的结构材料常用镁合金等,金属镁可从海水中提取,工艺流程如图:
(1)粗盐经过溶解、过滤、蒸发后得到的精盐是 (选填“纯净物”或“混合物”)。
(2)反应②的过程是 (选填“放热”或“吸热”)过程。
(3)“母液”中含MgCl2,以上①~④步化学反应中未涉及的反应类型是 。
a.化合反应
b.分解反应
c.复分解反应
d.置换反应
(4)已知某海域海水中总的含盐量约为3.5%,盐中镁元素的质量分数约为3.7%,则海水中镁元素的质量分数约为 (保留两位有效数字),由此可知,用海水晒盐后剩余的“母液”来提取镁,而不直接用海水的主要原因是 。
覆铜板是制作印刷线路板的基本材料。覆铜板中的金属Sn占2﹣10%,Cu占90﹣98%.简易工艺流程如图:
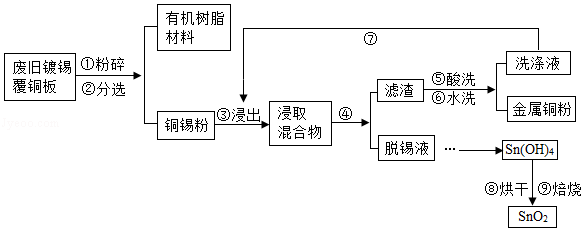
(1)将废旧镀锡覆铜板粉碎后,通过步骤②可将其分离为有机树脂材料(固体)和铜锡粉。根据化学常识回答,此工艺利用的是 的性质(填字母代号)。
a.溶解性不同
b.密度不同
c.沸点不同
(2)步骤④中涉及的分离操作是 (填操作名称)。
(3)通过步骤⑤和⑥所得洗涤液的pH 7(填“>”、“<”、“=”)。
(4)设计步骤⑦的主要目的是 。
(5)步骤⑨中涉及的主要化学方程式为 。
利用废弃的黄铜(含铜、锌)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图(反应条件已略去):
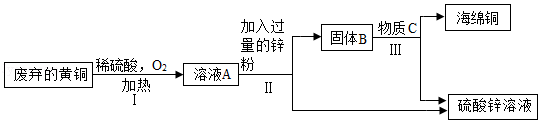
已知:2Cu+2H2SO4+O2 2CuSO4+2H2O
(1)过程Ⅱ中加入过量锌粉的目的是 。
(2)过程Ⅲ中有气体产生,所选用的物质C是 (填一种酸)。
海洋中蕴藏着丰富的化学资源,从海水中提取金属镁的主要步骤如图:
资料:海滩贝壳的主要成分是CaCO 3

(1)为节约资源,试剂X常用海滩贝壳为原料制得,则试剂X为 (填化学式);
(2)操作Y的名称为 ;
(3)在熔融状态下的MgCl 2,通电后会生成镁与一种气体单质,该反应的化学方程式为 。
(4)镁常用作合金,一般地合金相对于纯金属,具有的优良特性有 (填序号)。
A.硬度小
B.熔点高
C.抗腐蚀性强
新冠肺炎疫情防控期间,湘潭市各学校开展全域喷洒低浓度“84”消毒液进行消毒。“84”消毒液的有效成分是NaClO(次氯酸钠),模拟制备“84”消毒液的流程如图所示,其中A是密度最小的气体,B俗称烧碱,Cl2是一种黄绿色的有毒气体。请回答下列问题:
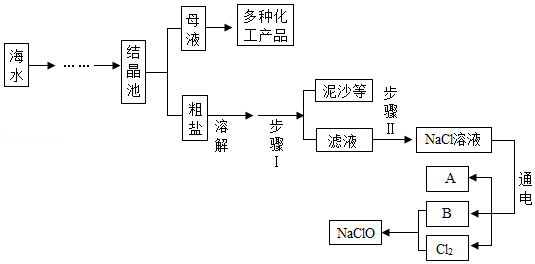
(1)A的化学式为 ,B的化学式为 。
(2)溶解过程中玻璃棒的作用是 ,步骤Ⅰ中主要的操作名称是 。
(3)步骤Ⅱ中,通常用碳酸钠来除去滤液中的氯化钙杂质,请写出有关反应的化学方程式 ,该反应属于 反应(填基本反应类型)。
(4)电解水时,一般在水中加入少量硫酸钠或氢氧化钠的目的是 ,不能加入NaCl的原因是 。
试题篮
()