保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降.制备流程如图:

(1)反应Ⅰ的原理为:Zn+2SO2═ZnS2O4,该反应类型为 .
(2)反应Ⅱ为复分解反应,该反应的化学方程式为 .
(3)操作a的名称为 .
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是 ,加入NaCl的原因是 .
(5)198gZn(OH)2理论上能得到Zn的质量为 g.
高纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产。某兴趣小组按如图所示实验步骤,模拟工业流程制备高纯碳酸钙。请回答下列问题。
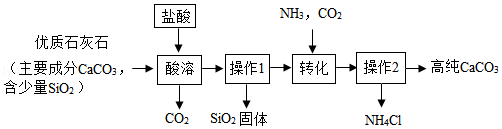
(1)“酸溶”过程中,将一定浓度的盐酸缓慢加入粉碎后的优质石灰石中,同时搅拌。搅拌的目的是 。
(2)“操作1”、“操作2”步骤中,需要用到的玻璃仪器有烧杯、玻璃棒和 。
(3)“操作2”中分离得到的NH4Cl,在农业上可用作 。
纳米碳酸钡是一种重要的无机化工产品,其生产原料的主要成分是BaCO 3同时还有少量SiO 2.生产工艺流程简要如图:

已知 SiO 2是一种难溶于水也难溶于酸的固体。请回答下列问题:
(1)SiO 2中Si的化合价是 。
(2)若在实验室中进行该实验操作|的名称是 。
(3)写出工艺中BaCO 3转化成BaCl 2的化学方程式 。
(4)上述工艺中可循环利用的物质是 ,该工艺中副产物A可用作 (写种用途即可)。
以镁矿石(主要成分MgCO3、SiO2)为原料生产MgO的工艺流程如图

注:SiO2难溶于水和常见的酸;“沉镁”过程中有Mg(OH)2生成。
(1)滤渣X的主要成分为 (填化学式)。
(2)实验室中用图一所示装置进行过滤。
①该装置中仪器A的名称为 。
②若过滤时滤液出现浑浊,可能的原因是 (填字母)。
a.滤纸已破损 b.漏斗中液面低于滤纸边缘 c.滤纸未紧贴漏斗内壁
(3)“沉镁”时MgSO4与NH3•H2O发生反应。结合图二,写出该反应的化学方程式 。
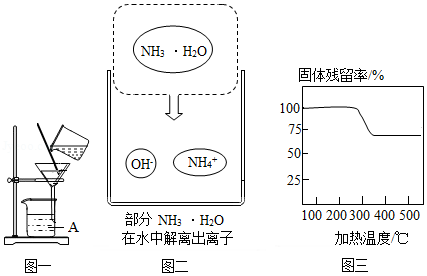
(4)已知在不同温度下,充分加热等质量的Mg(OH)2,加热温度与固体残留率的关系如题图三所示。“加热”时温度至少要达到350℃,原因是 。
利用电石渣[主要成分为Ca(OH)2、MgO]制备硫酸钙的主要工艺流程如图: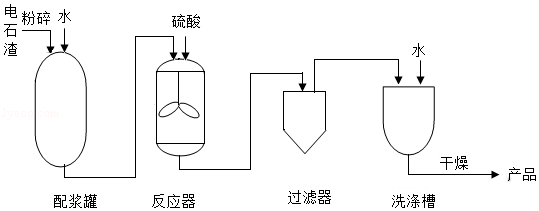
已知:MgO难溶于水;MgSO4易溶于水; CaSO4微溶于水。
(1)反应器中搅拌的目的是 。
(2)反应器中发生的反应主要有MgO+H2SO4═MgSO4+H2O和 。
(3)上述流程中,用于分离提纯的设备有 。
孔雀石的主要成分是CuCO3•Cu(OH)2及少量不溶性杂质(杂质不与酸反应),某同学按下列实验步骤制取了少量氧化铜。

(1)白色沉淀的化学式为 。
(2)写出步骤③中发生反应的化学方程式 ; 。
(3)蓝色沉淀受热分解生成另一种氧化物的化学式是 。
(4)若向溶液A中逐滴加入NaOH溶液,其过程中溶质种数会发生变化,最多时可达 种。
实验室以MnO 2为原料制备少量高纯MnCO 3的流程如下:
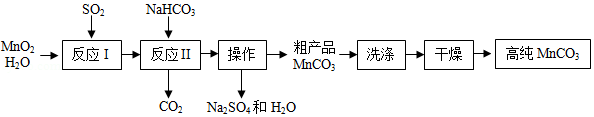
已知:①反应Ⅰ的化学方程式:MnO 2+SO 2═MnSO 4;
②MnCO 3、Mn(OH) 2均难溶于水,MnCO 3在100℃时开始分解。
(1)反应Ⅰ属于基本反应类型中的 反应。
(2)流程中"操作"的名称为 ,所需要的主要玻璃仪器有 。
(3)反应Ⅱ的化学方程式为 。反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO 3粗产品中将混有 (填化学式)。
(4)验证MnCO 3粗产品表面附着有Na 2SO 4杂质:取样品少许,向其中加入水,搅拌、过滤,向滤液中加入适量的 (填化学式)溶液,有白色沉淀产生。
(5)为获得高纯MnCO 3,需选择"低温"干燥的原因是 。
胆矾(CuSO4•5H2O)在工农业生产中有广泛的用途。实验室利用废旧电池的铜帽(主要含铜和锌)为原料制备胆矾。实验流程如图所示:
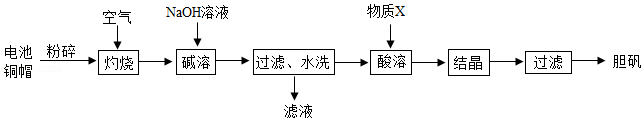
查阅资料:氧化锌能溶于氢氧化钠溶液。
(1)废旧电池铜帽的表面常有油污,可用洗洁精预先除去,洗洁精在除去油污的过程中起 作用。
(2)“碱溶”步骤中,为加快反应速率可采取多种措施,如搅拌、 等。
(3)“酸溶”时,发生反应的化学方程式是 。
(4)“灼烧”完全(已充分反应)的判断依据是 。
粗盐中含有泥沙等不溶性杂质,还含有氯化钙、氯化镁、硫酸钠等可溶性杂质。
提纯粗盐并制取纯碱的工艺流程如图:
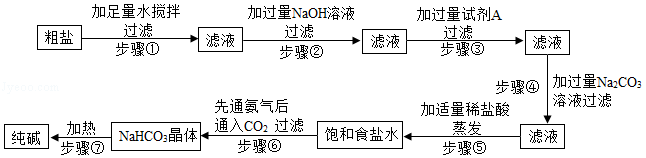
已知:①20℃时,将CO2通入含有NH3的饱和NaCl溶液中生成NaHCO3晶体和NH4Cl溶液
②20℃时,几种物质在水中的溶解度/g
NaCl |
NH4Cl |
NaHCO3 |
36.0 |
37.2 |
9.6 |
请根据上述题中有关信息,回答下列问题:
(1)步骤③中加入试剂A的化学式是 ;
(2)步骤④中加入过量Na2CO3溶液的目的是 ;
(3)在步骤⑥反应中,有NaHCO3晶体析出,而没有NH4Cl和NaCl析出的原因是 ;
(4)步骤⑦中NaHCO3转化为纯碱的化学反应方程式是2NaHCO3 Na2CO3+CO2↑+H2O,该化学反应属于 反应(填基本反应类型)。
已知:向饱和食盐水中通入氨气得到饱和铵盐水,饱和铵盐水能与CO2发生反应:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如图:
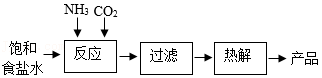
(1)常温时,饱和铵盐水的pH (填“=”或“>”)7。反应时,溶液中生成的NH4Cl中含有原子团的名称是 。
(2)过滤时,若经两次过滤滤液仍浑浊其原因可能是 (任写一条)。
(3)热解时,NaHCO3分解得到Na2CO3、CO2和H2O,该反应的化学方程式为 。
氯化亚铜CuCl是一种难溶于水和乙醇且在潮湿空气中易变质的物质,广泛应用于冶金、电镀、医药等行业、CuCl的制备流程如图:
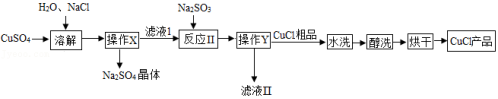
(1)"操作Y"名称是 。
(2)CuCl中铜元素的化合价为 。
(3)请配平"反应Ⅱ"的化学方程式: 。
(4)在"滤液Ⅱ"中可以循环利用的物质(水除外)是 。(填化学式)
(5)"醇洗"的目的是 ,防止后续过程中氯化亚铜变质。
无水氯化钙(CaCl 2)是重要的干燥剂,CaCl 2•6H 2O与冰的混合物是实验室常用的制冷剂,将CaCl 2•6H 2O加热可得CaCl 2.某工厂以石灰石为原料生产无水氯化钙的流程如图所示,原料石灰石中含有的杂质主要是MgCO 3、MgSO 4。

(1)过滤和蒸发均用到的玻璃仪器是 。
(2)石灰石溶解时,杂质MgCO 3发生反应的化学方程式为 ,该反应是 (填基本反应类型)
(3)加入BaCl 2溶液除去的杂质离子是 ,加入氢氧化钙溶液除杂的化学方程式为 。
(4)由CaCl 2•6H 2O得到CaCl 2是 变化(填"物理"或"化学")。
已知:NaOH溶液能与MgSO4溶液反应生成Na2SO4和难溶于水的Mg(OH)2.镁大多是从海水中提取。某小组从预先处理后的海水中提取镁的主要步骤如图:

(1)沉淀时,NaOH应过量的目的是 。
(2)过滤时,使用玻璃棒的作用是 。
(3)溶解时,稀盐酸与Mg(OH)2发生反应的化学方程式为 ,该反应的反应类型为 。
碳酸钾广泛应用于玻璃、纺织印染和肥皂生产等领域。制取碳酸钾的工艺流程示意图如图: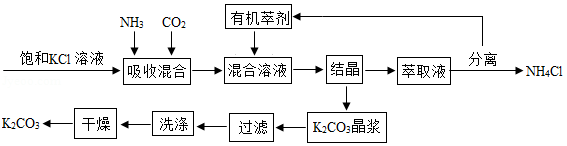
温度/℃ |
0 |
10 |
20 |
30 |
40 |
60 |
80 |
100 |
K2CO3的溶解度/g |
107.0 |
109.0 |
111.0 |
114.0 |
117.0 |
126.0 |
139.0 |
156.0 |
根据如图表信息,回答下列问题:
(1)生成碳酸钾的化学方程式为 。
(2)上述流程中可循环使用的物质是 ,NH4Cl在农业上可用作 。
(3)得到K2CO3晶浆的结晶方法是 。
(4)上述流程中洗涤K2CO3晶体应选用 (填序号)。
①NH4Cl溶液
②热水
③饱和K2CO3溶液
过氧化钙( CaO2)是用途广泛的优良供氧剂。以电石渣[主要成分为Ca(OH)2,含少量CaCO3为原料制备CaO2的一种工艺流程如图1:

[查阅资料]
Ⅰ.Ca(OH)2+2NH4Cl=CaCl2+2NH3•H2O
Ⅱ.CaCl2+2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4Cl
Ⅲ.CaO2•8H2O在水中不太稳定,会缓慢分解。
(1)“提取Ca(OH)2”时反应的基本类型是 ;Ca(OH)2的俗名为 ;“过滤1”所得滤渣的主要成分是 。
(2)在实验室进行过滤操作时,要遵循“一贴、二低、三靠”原则。其中“二低”指的是:滤纸边缘略低于漏斗口、 。生产过程中为了精确测定溶液的pH,常使用 (填仪器名称)。
(3)在其他条件不变的情况下,制备CaO2•8H2O的反应时间(t)对其产率(w)的影响如图2所示。
①平均反应速率最快的时间段为: (填字母)。
a.0~10min b.10~20min c.20~30min d.30~40min
②30min后,w开始下降的主要原因是 。
(4)为了测定加入的NH4Cl溶液中溶质的质量分数,取30.00g NH4Cl溶液于烧杯中,加入稍过量的AgNO3溶液,完全反应后过滤、洗涤、干燥、称量,得到14.35g 白色固体。通过计算确定该溶液中NH4Cl的质量分数(精确到0.1%) 。
试题篮
()