为测定某黄铜样品中锌的含量,某同学称取20g黄铜(铜和锌的合金)样品于烧杯中,向其中加入稀硫酸至不再产生气泡为止,共消耗100g质量分数为9.8%的稀硫酸,请计算:
(1)该黄铜样品中锌的质量。
(2)反应后所得溶液的溶质质量分数(计算结果保留0.1%)。
构建知识网络是一种重要的学习方法。图为某校化学学习小组的小阳同学绘制的铁的化学性质网络示意图。请分析回答下列问题: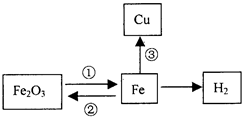
(1)反应①中可用 ▲ (填化学式)作还原剂;
⑵写出高炉中发生的反应①的化学方程
式: ▲ ;
写出反应③的化学方程式 ▲ ;
⑶反应②导致每年有大量的钢铁锈蚀,为阻止该反应的发生,人们常采用在钢铁表面涂刷油漆或镀上其它金属等方法。这两种方法的共同原理是阻止钢铁
与 ▲ 接触;
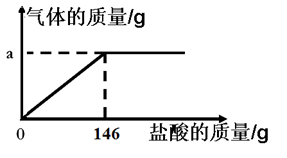
⑷该化学学习小组为了分析生铁中铁的含量,进行了如下实验研究:取12g生铁与10%的盐酸反应,并绘制了加入盐酸质量与放出气体质量的关系图(见右下图)。(说明:生铁中杂质不溶于水,不与盐酸、硫酸铜溶液反应。)
①铁完全反应用去盐酸的质量为 ▲ g。
②生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)
▲
(5)某同学列出了如下计算式:
生铁与盐酸刚好反应完全时所得溶液质量= (146+12-a)g
小明对该计算式提出了质疑,请指出其中的错误 ▲
。
(6)小华另设计了一个实验方案:用12g生铁粉与20%的硫酸铜溶液反应来分析生铁中铁的含量。请你画出加入硫酸铜溶液质量与固体质量变化关系的曲线。
20g含杂质(杂质不溶于水,也不溶于酸)的锌样品,与一定质量的稀硫酸恰好完全反应,所得溶液质量80.5g,同时生成氢气0.4g。试计算:
(1)样品中锌的质量分数。
(2)完全反应后生成物溶液中溶质的质量分数。
某同学打算用金属与稀硫酸反应制备氢气.
(已知:Zn+H2SO4===ZnSO4+H2↑
Fe+H2SO4===FeSO4+H2↑
2Al+3H2SO4===Al2(SO4)3+3H2↑)
铝、铁、锌的市场价格分别为:铝—4800元/t、铁—2100元/t、锌—10800元/t。如果不考虑其他因素,该同学要制备2g的氢气,选择哪一种金属最经济合算
试题篮
()