新冠肺炎疫情期间,可用体积分数为75%的乙醇(C2H5OH)消毒液进行手和其他皮肤的消毒。如图为某品牌乙醇消毒液的标签。(纯乙醇的密度约为0.8g/mL,水的密度约为1.0g/mL)。
请回答下列问题:
(1)H2O的相对分子质量为 ,H2O分子中H原子与O原子的个数比为 。
(2)乙醇由 元素组成,配制乙醇消毒液需要乙醇和水的体积比为 。
(3)乙醇消毒液中乙醇的质量分数约为多少?(要求写出计算过程,结果精确到0.1%)

下图为某高钙片的外包装药品部份说明,请仔细观察、阅读后回答下列问题。

(1)维生素D种类较多,其中维生素D2的化学式为C28H44O,试计算维生素D2的相对分子质量为 ;维生素D2中碳、氢、氧三种元素的质量比为 。
(2)如果按用量服用,则每天补充钙元素的质量为 g。
(3)根据你对补钙产品的调查和已有的化学知识,这里的“钙”指 (填字母)。
| A.原子 | B.分子 | C.单质 | D.元素 |
(4)计算该高钙片中碳酸钙的质量分数 (需有过程) 。
小明测得石灰石与一定量的稀盐酸反应后的溶液PH为2,也适量该溶液向其中逐滴加入碳酸钠溶液,并测得溶液PH随加入碳酸钠溶液体积的变化曲线如下图所示。
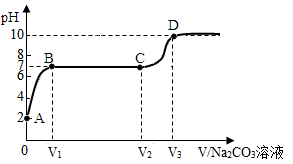
请回答下列问题:
(1)A点处溶液中的两种溶质是(写化学式);
(2)AB段可观察到的实验现象是 ;
(3)BC段发生反应的化学方程式是 ;
(4)CD段PH上升的原因是;
某氢氧化钙粉末中含有碳酸钙杂质.现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。
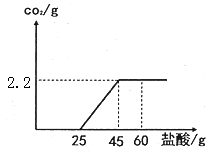
(1)生成二氧化碳的质量是g;
(2)加入60g稀盐酸后所得溶液中含有的溶质是、(填化学式);
(3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%).
有CO、CO2和N2的混合气体40 g,其中碳元素的质量分数为30%,使该混合气体与足量灼热的氧化铁完全反应,再将气体通入过量的澄清石灰水中,写出以上过程中发生反应的两个化学方程式:________________________;________________________。充分反应后得到白色沉淀的质量为___________________________。
追求化学家的足迹,建立严谨的科学实验基础。
(1)舍勒是最早制得氧气的化学家之一,他获得氧气的方法主要有以下两类:
a.加热分解硝酸钾、氧化汞、硝酸银等
b.用二氧化锰与浓硫酸加热:2MnO2+2H2SO4(浓)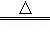 2MnSO4+2X+O2↑
2MnSO4+2X+O2↑
①a中反应物均可制得氧气,因为它们组成的共同点: ;
②b中物质X化学式为 ;
(2)舍勒由于受“燃素说”的影响(即认为一切可以燃烧的物质都是由灰和“燃素”组成的,物质燃烧后剩下的是灰,而燃素本身变成了光和热,逸散到空中去了),导致“氧气”从他的鼻尖下溜走.化学家拉瓦锡结合大量实验事实,否定了“燃素说”认为的“物质燃烧后质量应当减轻”的观点,真正发现了氧气
①写出铁丝在氧气中燃烧的化学方程式: ;
②以铁燃烧的事实,指出上述“燃素说”的谬误: .
(3)拉瓦锡还通过定量研究分析实验,推进了俄国化学家洛蒙诺索夫的发现获得公认并成为化学的重要定律:即在化学变化中物质的质量是守恒的。也称物质不灭定律。它是自然界普遍存在的基本定律之一。
①由质量守恒定律可知,化学反应前后一定不变的是_______(填字母)。
a原子种类
b原子数目
c分子种类
d分子数目
e元素种类
f物质种类
②X、Y、Z三种物质各15g ,在一定条件下充分反应生成新物质M 30g ;若增加10g X,X与Z恰好完全反应。则参加反应的Y、Z的质量比为_______。
某兴趣小组需要配制100g质量分数为9.8%的稀硫酸,假设常温下该稀硫酸的PH值为0.在装有100g该稀硫酸的烧杯中加入104.4gNa2CO3溶液,恰好完全反应,溶液呈中性.
(1)硫酸(H2SO4)的相对分子质量为 ;
(2)硫酸(H2SO4)中氧原子、氢原子的原子个数比为 ;
(3)实验室只有98%的浓硫酸,密度为1.84g/cm3.需要量取 mL(保留一位小数)
(4)如果向烧杯中滴加的碳酸钠溶液质量约为150g,在下图中,画出烧杯内溶液的PH值变化图象(标出Na2CO3溶液的质量)




(5)计算所得溶液的溶质质量分数是多少?(写出计算过程)
下表是100 g某食品的部分营养成分(其它成分不能提供热量):
| 总热量 |
蛋白质 |
糖类 |
油脂 |
水 |
钠 |
磷 |
钙 |
|
| 1984 kJ |
50 g |
20g |
待测 |
5g |
4.6 mg |
3.3 mg |
8mg |
|
(1)该食品所含的有机营养素是 __ ;每100 g该食品中所含营养成分质量最大的是 __ 。
(2)上表中钠、磷、钙指的是 (选填“单质”、“元素”、“离子”);
(3)若该食品中的钙以碳酸钙的形式存在,则100 g该食品中,碳酸钙为 mg;
(4)假设食物的总热量是由蛋白质、糖类、油脂提供的,单位质量的蛋白质、糖类、油脂完全氧化放热约为:油脂 38 kJ/ g 、蛋白质 20 kJ/ g、糖类 15 kJ/ g。
根据此数据计算,理论上100 g该食品中油脂的质量为 g。
将6.8 g含杂质的锌粒,加入到盛有50.0g过量的稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为56.6 g。试计算
(1)生成的气体的化学式是______________;其质量为______________ g。
(2)锌粒中所含锌的质量分数(精确到0.1%)。
(6分)为测定氯化钠和碳酸钠混合物的组成情况,某研究小组进行了如下实验。
请回答下列问题:
(1)实验中发生反应的化学方程式为
(2)求解混合物中发生反应物质的质量(x)的比例式为
(3)混合物中氯化钠和碳酸钠质量的最简整数比为 。
(4)在滴加氯化钡溶液的过程中,烧杯中各溶质质量的变化情况为
(5)所用氯化钡溶液中溶质质量分数为 。
洋洋同学从与医生的交谈中获悉:正常人每分钟约呼吸30次,每次约吸入0.4L空气,请问一个人一昼夜吸入体内的氧气约为_____升?(以空气中氧气的体积分数是21%计算,计算结果保留整数)
2013年12月2日,“嫦娥三号”探测器由“长征三号乙”运载火箭发射,首次实现月球软着陆和月面巡视勘察。
(1)“长征三号乙”运载火箭的第三级采用燃料是液氢、助燃剂是液氧。液氢燃烧的化学方程式为___ __,液氢应用于航天领域的优点是_______________。氢能源是最理想的燃料,目前广泛使用还存在困难,如:___________________(写一个)。
(2)“长征三号乙”运载火箭的一、二级火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推进剂,两者反应的化学方程式为C2H8N2 +2N2O4点燃 3N2 ↑+2CO2↑+4H2O↑。根据化学方程式计算:12 t C2H8N2完全燃烧需要助燃物N2O4的质量.(写出解题过程) (计算结果保留一位小数)
(3)“嫦娥三号”的“玉兔”月球车可从携带的锂电池储备一定的能源。锂电池的工作原理是锂与二氧化锰反应生成LiMnO2,从能量变化角度看,该反应将化学能转化为 。
为了测定某赤铁矿(其中杂质不溶于水,也不与稀硫酸反应)中氧化铁的质量分数,去赤铁矿样品与一定质量的19.6%的稀硫酸在烧杯中正好完全反应,过滤实验数据如下,请回答问题:
| |
反应前 |
反应后 |
|
| |
烧杯和稀硫酸的质量 |
赤铁矿样品质量 |
烧杯和滤液的质量 |
| 实验数据 |
180g |
20g |
196g |
(1)反应的化学方程式为_________;
(2)根据条件.列出求解参加反应的硫酸质量(x)的比例式_________;
(3)向反应后的溶液中加入34g水后,最终所得溶液溶质的质量分数为_________;
(4)配制上述质量分数为19.6%的稀硫酸.需要质量分数为98%的浓硫酸的质量是_________;
(5)制取含铁96%生铁336t,需要上述赤铁矿的质量是_________。
兴趣小组欲测定某未知浓度
溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
(1)配制30g 10%的
溶液.
步骤为:计算、称取、量取、、转移.量取水时应选用规格为mL(从10、50、100中选取)的量筒.最后将碳酸钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是(填序号).
A.30g B.10% C.
溶液
(2)测定未知浓度
,溶液的溶质质量分数.
取50g
溶液,逐滴滴加上述
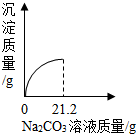
溶液的过程中,测得产生沉淀与加入
溶液的质量关系如图所示.
①恰好完全反应时,消耗
溶液的质量为g.
②请通过计算确定
溶液的溶质质量分数.
试题篮
()