NaOH俗称火碱、烧碱、苛性钠,是常见的碱,请回答下列问题:
(1)NaOH的名称是 ,易溶于水,溶于水生成自由移动的 (填微粒符号),所以NaOH溶液能够导电。
(2)向NaOH溶液中滴加稀硫酸,溶液的pH (填”增大”、“减小”或“不变”)。
(3)在试管中加入2mL 10%NaOH溶液,滴加5%CuSO4溶液4﹣5滴,生成 色的Cu(OH)2沉淀。用试管中的物质检验葡萄糖,发生如下反应:C6H12O6+2Cu(OH)2+NaOH C6H11O7Na+Cu2O↓+3X,推测X的化学式为 。
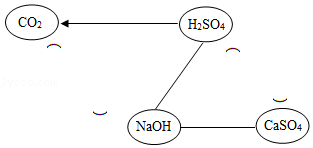
(4)参考如图,在( )内画出“→”或“﹣”补全图例(“→”表示物质间转化,“﹣”表示物质间相互反应)。请写出图例中,能发生复分解反应的化学方程式: (写出一个即可)。
在催化剂、加热的条件下,氨能和氧气发生反应:4NH3+5O2 4X+6H2O,则X的化学式为( )
A.N2B.NOC.NO2D.N2O
一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
物质 |
甲 |
乙 |
丙 |
丁 |
反应前质量/g |
26 |
8 |
2 |
4 |
反应后质量/g |
1 |
X |
16 |
15 |
A.上表中X的值是0
B.该反应的基本反应类型是化合反应
C.乙一定是该反应的催化剂
D.丙和丁变化的质量比为14:11
下列说法正确的是( )
A.为了解决能源危机,在水中加入催化剂把水变成汽油
B.石油的分馏可以得到汽油、煤油、液化石油气等产品,因此是化学变化
C.为了降低成本可用工业酒精勾兑饮用酒
D.食用加碘盐可以预防甲状腺肿大
图A、B、C、D是初中化学常见的实验据图回答下列问题 
(1)在做"物质在盛有氧气的集气瓶中燃烧"的实验时,常常要在集气瓶里预先加少量的水。B实验中水的主要作用是 ,A、B两个实验中的水可用少量细沙代替的是 。
(2)C是某气体在空气中燃烧的实验。能观察到火焰上方冷而干燥的烧杯壁有水滴出现说明该气体中一定含有 元素;然后迅速把烧杯倒过来,向烧杯内注入少量澄清石灰水,振荡,观察到澄清石灰水变浑浊,说明该气体中一定含有 元素。
(3)D是稀释浓硫酸的实验。正确操作中试剂X是 ,用玻璃棒搅拌的目的是 。
生活中的泡沫灭火器常装有硫酸铝溶液和碳酸氢钠溶液,使用时把泡沫灭火器倒转,两种药液相互混合,发生如下化学反应:
1Al2(SO4)3+ NaHCO3═ Na2SO4+ Al(OH)3↓+ CO2↑
(1)请完成上述反应的化学方程式的配平。
(2)上述反应生成的大量二氧化碳跟发泡剂(主要成分是皂角等原料制取的液体)混合形成液体泡沫,从喷嘴中快速喷射出来,覆盖在燃烧物的表面,以达到灭火目的。其中应用的灭火原理有 。
(3)当电器发生火灾时,应先 ,然后才能使用泡沫灭火器。
(4)泡沫灭火器表面通常喷红漆防锈防锈的原理是 。
消毒与清洁对公共场所和家庭是至关重要的。
(1)二氧化氯(ClO 2)可作水处理消毒剂,二氧化氯中氯元素的化合价是 。
(2)"洁则灵"与"漂白剂"不能混用,二者若混合易产生一种有毒气体X.反应原理为:NaClO+2HCl=NaCl+X↑+H 2O,则X的化学式为 。
(3)用炉具清洁剂(含有NaOH )清洗炉具时,应避免接触皮肤,其原因是 。
(4)使用洗洁剂清洗餐具上的油污时,利用了洗涤剂对油污的 作用。
2KI+H2SO4+O3═O2+M+K2SO4+H2O中M的化学式是( )
A.H2B.KOHC.HID.I2
人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

(1)金、银在自然界有单质形式存在,说明他们的化学性质都 。
(2)在生产生活实践中,人类逐渐掌握了多种金属的冶炼技术。
①)比较两种铁矿石磁铁矿(主要成分Fe3O4)和菱铁矿(主要成分FeCO3),从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是 。
②近代工业上采用电解熔融氧化铝(A12O3)的方法冶炼铝,Al2O3分解后得到两种单质,该反应的化学方程式为 : 。
(3)镁铝合金被誉为“21世纪绿色金属结构材料”。一种镁铝合金Mg17All2是特殊的储氢材料,完全吸收氢气后得到MgH2和Al,该反应的化学方程式为 。
(4)钛和钛合金是21世纪的重要的金属材料。钛合金制品放在海水中数年,取出后仍光亮如新,是因为其 (填字母序号)非常好。
A.可塑性 B.机械性能 C.抗腐蚀性能
(5)铁在潮湿的空气中反应生成疏松的铁锈。已知:2FeCl3+Fe=3FeC12
①铁锈的主要成分是 (填化学式):将生锈的铁制品放入一定量的稀盐酸中充分反应,变化过程中最多涉及 种化学反应基本类型。
②将10g表面生锈的铁钉(杂质已忽略)浸泡在100g溶质质量分数为7.3%的稀盐酸中充分反应,观察到铁锈已完全消失。反应停止后,取出光亮的铁钉洗涤、干燥、称量,质量为3.6g。则原锈铁钉中铁元素的质量分数为 。
(6)利用“活泼金属”可以制得H2,H2可用作汽车能源。若推广应用于汽车产业,则需综合考虑的因素有 (填字母序号)。
A.金属原料的成本 B.生成过程中的能耗和污染 C.金属的回收利用
工业上,高温煅烧石灰石可制取生石灰(CaCO3 CaO+CO2↑)。现有100g CaCO3样品,高温煅烧一段时间后,剩余固体的质量为67g。下列推断不符合客观事实的是( )
A.生成CO2的质量是33g
B.生成物中CaO的质量是42g
C.剩余固体中钙元素的质量分数大于40%
D.剩余固体中碳元素与氧元素的质量之比大于1:4
甲、乙、丙、丁4种物质在密闭容器中充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
物质 |
甲 |
乙 |
丙 |
丁 |
反应前质量/g |
30 |
3 |
6 |
8 |
反应后质量/g |
16 |
m |
4 |
24 |
A.甲和丙两物质中的元素种类与丁元素种类不同
B.乙一定是反应的催化剂
C.参加反应的甲、丙的质量比一定是7:1
D.甲、丁一定都是单质
硅(Si)是信息技术的关键材料,工业制硅的反应之一是SiCl4+2H2 Si+4X.下列说法正确的是( )
A.硅是地壳中含量最多的元素
B.X的化学式为H4Cl4
C.SiCl4中硅元素的化合价是﹣4
D.该反应为置换反应
在一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生某个反应,测得反应前后各物质的质量如下表:
物质 |
甲 |
乙 |
丙 |
丁 |
反应前质量/g |
20 |
30 |
20 |
15 |
反应后质量/g |
0 |
x |
y |
10 |
下列叙述错误的是( )
A.参加反应的甲与丁的质量比为4:1
B.x+y=75
C.y≤20时,该反应一定是化合反应
D.x的取值范围:0≤x≤30
维C泡腾片是一种常见的补充维生素C的保健品。某品牌维C泡腾片(以下称“本品”)的主要成分如图1所示。
(1)下列关于维生素C的说法正确的是 (填字母)。
a.维生素C由C、H、O三种元素组成
b.维生素C的相对分子质量为176g
C.维生素C由6个碳原子、8个氢原子和6个氧原子构成
d.维生素C中C、H、O元素的质量比为9:1:12
(2)阅读本品的营养成分表:每100g维C泡腾片含钠5750mg(1mg=10﹣3g)。已知本品其他成分不含钠元素,则本品中碳酸氢钠的质量分数为 。
(3)维C泡腾片水溶液酸碱性的测定:将本品一片投入蒸馏水中,有气泡产生,反应原理为:H3C6H5O2+3NaHCO3=Na3C6H5O2+3CO2↑+3 (填化学式)。
待不再产生气体后,测得溶液呈酸性。
(4)维C泡腾片中碳酸氢钠质量分数的测定:称量相关实验用品质量,将本品一片投入蒸馏水中,待不再产生气体后,称量锥形瓶及瓶内所有物质的总质量。装置如图2所示。
相关数据如表:
物品 |
反应前 |
反应后 |
||
锥形瓶 |
蒸馏水 |
维C泡腾片 |
锥形瓶及瓶内所有物质 |
|
质量/g |
71.75 |
50.00 |
4.00 |
125.53 |
①根据以上数据计算本品中碳酸氢钠的质量分数(写出计算过程,结果精确到0.1%)。
②实验测定结果与题(2)计算结果相比有明显偏差,其可能原因是 。

燃料的发现和利用提高了人类生活的质量,推动了人类文明的进步。
(1)将煤隔绝空气加强热,得到焦炭、煤气等,该过程属于 (填“物理”或“化学”)变化。煤与高温水蒸气反应生成CO和H2.在300℃、1.5MPa、催化剂存在的条件下,CO和H2可转变为液体燃料甲醇(CH3OH)。写出CO与H2反应成甲醇的化学方程式: 。
(2)焦炭(主要成分是碳)是高炉炼铁的重要原料。炼铁高炉内发生的主要化学反应如图1所示,其中反应②体现了焦炭的 性。

(3)乙醇可作为酒精灯、酒精喷灯的燃料。某铜质酒精喷灯的结构如图2所示。使用酒精喷灯时,先在预热盘中注入酒精并点燃,一段时间后,调节空气调节杆,即可点燃酒精喷灯。结合燃烧的条件回答:点燃预热盘中酒精的目的是 。
(4)氢气的制取和储存越来越受到人们的关注。
①最理想的制氢方法:在合适的催化剂作用下,利用太阳光使水分解。该制氢过程 (填“吸收”和“放出”)能量,生成的氢气与氧气在相同条件下的体积之比为 。
②我国稀土资源丰富,某种稀土储氢材料(用M表示)的储氢原理可表示为M+3H2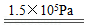 LaNi5H6.M的化学式为 。
LaNi5H6.M的化学式为 。
试题篮
()