2021年3月,中央财经会议明确把碳达峰、碳中和纳入生态文明建设整体布局,争取在2060年前实现碳中和。“碳中和”是指在一定时间内产生的二氧化碳排放总量,通过二氧化碳去除手段来抵消掉这部分碳排放,达到“净零排放”的目的。
(1)二氧化碳是引起温室效应的主要气体,根据图甲回答支持这一结论的信息是: 。

(2)科学家已经研究出多种方式来实现二氧化碳的转化。
①固碳的另一种方法是将收集的二氧化碳和水混合后注入地下玄武岩中,最终与岩石中的矿物质作用形成固态的石头碳酸盐。这种固碳方式属于 变化(选填“物理”或“化学”)。
②我国研发的“液态太阳燃料合成技术”(图乙),甲醇(CH3OH)等液体燃料被形象地称为“液态阳光”。甲醇制取过程中能量转化是:太阳能→电能→ 能。甲醇合成时,若碳元素全部来自于二氧化碳,则制取10吨甲醇需要消耗二氧化碳 吨。
(二氧化碳转化成甲醇的方程式为:CO2+3H2 CH3OH+H2O)
CH3OH+H2O)
为测定石灰石样品中碳酸钙含量,某小组同学在一定质量的样品中加入足量稀盐酸,利用生成CO2的质量来测定(忽略稀盐酸挥发的影响)。
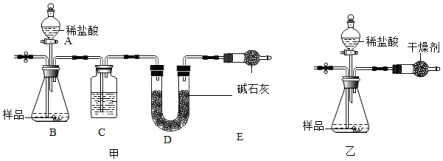
(1)小科用图甲装置实验,通过测定反应前后D装置质量的变化来得到CO2质量。为了避免水蒸气对实验的影响,使测最结果更准确,装置C中应装入 (填试剂名称)。
(2)小明用图乙装置实验,通过测定反应前后装置总质量的变化来得到CO2质量。他用碱石灰做干燥剂,请判断这种做法是否合理并说明理由 。
(3)实验时。正确选择干燥剂后,两装置均可通过左侧导管鼓入某种气体一段时间,来进一步减小误差。下列操作可行的是 。
选项 |
实验装置 |
反应开始前鼓入的气体 |
反应结束后鼓入的气体 |
A |
甲 |
氮气 |
氮气 |
B |
甲 |
干燥空气 |
干燥空气 |
C |
乙 |
氮气 |
氮气 |
D |
乙 |
干燥空气 |
干燥空气 |
小宁用稀盐酸和石灰石反应制取二氧化碳(石灰石中的杂质既不溶于水也不和酸反应),为了探究反应后溶液的成分,他又进行如下实验:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,发现先有气泡产生,后生成白色沉淀。下表为产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系。
碳酸钠溶液总质量/g |
25.0 |
50.0 |
75.0 |
100.0 |
125.0 |
150.0 |
175.0 |
200.0 |
气体总质量/g |
1.1 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
沉淀总质量/g |
0 |
0 |
2.5 |
5.0 |
m |
n |
9.0 |
9.0 |
(1)表中n= 。
(2)所取的反应后50g溶液中溶质是 。
(3)所用碳酸钠溶液中溶质的质量分数是多少?
在5.6g铁粉中,先逐滴加入一定量的Cu(NO 3) 2溶液,充分反应后再逐滴加入AgNO 3溶液,剩余固体质量与所加溶液总质量的关系如图所示。下列说法正确的是( )
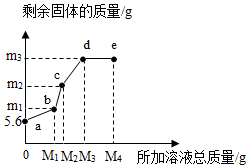
| A. |
所加溶液质量为M 1g时,生成Cu的质量为m 1g |
| B. |
bc段发生的是Cu和AgNO 3溶液的反应 |
| C. |
m 3的值为21.6 |
| D. |
e点溶液中不含Cu(NO 3) 2 |
小嘉发现:向碳酸钠溶液中倾倒稀盐酸,很快就产生了气泡:向碳酸钠溶液中逐滴加入稀盐酸,滴加一定量后才有气泡产生。查阅资料:向碳酸钠溶液中逐滴加入稀盐酸,先发生的反应是Na2CO3+HCl═NaCl+NaHCO3;当Na2CO3全部转化成NaHCO3后,再发生反应NaHCO3+HCl═NaCl+H2O+CO2↑。为此他用如图所示装置进行了如下实验:
步骤一:在广口瓶中加入10克溶质质量分数为10.6%的碳酸钠溶液,用注射器向瓶中缓慢注入一定量的溶质质量分数为7.3%的稀盐酸,观察到瓶内无明显现象; 步骤二:继续用注射器向瓶中注入稀盐酸,一段时间后观察到瓶内连续产生气泡,烧杯中澄清石灰水?。 |
(1)步骤二中,观察到烧杯中澄清石灰水 。
(2)上述实验中,加入稀盐酸多少克后,才开始产生二氧化碳? 。
(3)向一定量碳酸钠溶液中无论是倾倒还是逐滴加入足量的稀盐酸,完全反应后产生二氧化碳质量是相同的,其本质原因是什么? 。

氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。实验室中制备KClO3的化学反应方程式为3Cl2+6KOH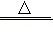 5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
(1)参加反应的氯气的质量为 g。
(2)所用KOH溶液中溶质的质量分数是多少?
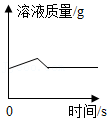
(1)将一定量的锌和金属R的混合粉末加入一定量的氯化铜溶液中,溶液质量的变化情况如图所示。下列说法错误的是 (填标号)。
A.金属活动性Zn>R
B.反应结束后过滤、滤渣中一定有Cu,可能有Zn和R
C.反应结束后过滤,若向滤渣中加入稀硫酸有气泡产生,则滤液一定无色
(2)某金属粉末含有Mg、Al、Cu、Ag中的一种或几种,取24g该金属粉末与足量稀盐酸反应产生2g氢气,则该金属粉末的组成有 种情况。
某造纸厂排放含NaOH的废水200吨,恰好需要含溶质4.9吨的硫酸溶液中和处理,求该废水中NaOH的溶质质量分数。
现有一定质量的碳酸钠和氯化钠的固体混合物,其中含氯元素7.1g。向该混合物中加入138.1g一定溶质质量分数的稀盐酸,恰好完全反应,得到氯化钠溶液并生成4.4g气体。计算:
(1)原固体混合物中氯化钠的质量;
(2)反应后所得溶液中溶质的质量分数。
金属在生产和生活中的应用极为广泛。
(1)生铁和钢是两种含碳量 的铁合金(填“相同”或“不同”)。
(2)下列生活用品利用金属良好导热性的是 (填序号)。
A.镀铬水龙头
B.铸铁暖气片
C.黄铜钥匙
(3)我国古代很早就认识到铜盐溶液里的铜能被铁置换,这一方法是湿法冶金技术的起源。铁与硫酸铜溶液反应的化学方程式为 。
(4)焊接钢轨的反应原理是铝与氧化铁在高温条件下反应生成铁和氧化铝,该反应的化学方程式为 。
(5)已知氧化镁和氧化铝都能与酸反应生成盐和水。现有氧化镁、氧化铝和铁的混合物9.9g,向其中加入245g质量分数为10%的稀硫酸,恰好完全反应,得到254.8g溶液,则原混合物中氧化镁的质量为 g。
2020年9月,中国向世界宣布了2030年前实现碳达峰、2060年前实现碳中和的目标。
(1)为减缓大气中二氧化碳含量的增加,下列措施可行的是 (填序号)。
A.植树造林,开发和利用太阳能、水能、风能等新能源
B.禁止使用煤、石油、天然气等化石燃料
(2)绿色植物通过光合作用吸收二氧化碳,生成葡萄糖并放出氧气,其反应的化学方程式:6CO2+6H2O 葡萄糖+6O2,则葡萄糖的化学式为 。若吸收44g二氧化碳,理论上可释放出氧气 g。
葡萄糖+6O2,则葡萄糖的化学式为 。若吸收44g二氧化碳,理论上可释放出氧气 g。
(3)近年我国科学家合成了一种新型催化剂,可将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为 。
(4)将一氧化碳和二氧化碳的混合气体3.2g通过足量灼热氧化铜粉末,充分反应,将所得的气体全部通入足量的氢氧化钡溶液中,气体全部被吸收,生成白色碳酸钡沉淀,溶液质量减少15.3g。则原混合气体中碳、氧元素的质量比为 (填最简比)。
在82.8克碳酸钠溶液中,逐滴加入盐酸,所加盐酸的质量与产生气体的质量关系如图所示(滴加过程中先发生化学反应:Na2CO3+HCl═NaHCO3+NaCl)。试计算(不考虑气体的溶解和盐酸的挥发):

(1)m的值为 。
(2)刚好不再产生气体时,溶液中溶质的质量分数(写出化学方程式及计算过程)。
某工厂生产的NaCl产品中含有杂质MgCl2,化学兴趣小组取100g样品完全溶解于313.6g水中,向该溶液中分5次加入一定浓度的氢氧化钠溶液,每次30g,充分反应。测得实验数据如下表所示:
(注:发生反应的化学方程式为MgCl2+2NaOH═Mg(OH)2↓+2NaCl)
次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
加入氢氧化钠溶液的质量/g |
30 |
30 |
30 |
30 |
30 |
累计生成沉淀的质量/g |
2.9 |
5.8 |
8.7 |
11.6 |
11.6 |
请完成下列各题:
(1)第 次恰好完全反应。
(2)样品中MgCl2的质量是 g。
(3)计算恰好完全反应时所得溶液的溶质质量分数(写出规范的计算过程)。
学习小组的同学通过如图实验测定一瓶失去标签的稀硫酸中溶质的质量分数。
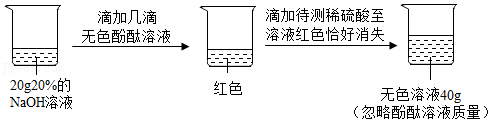
请完成下列分析与计算:
(1)反应中用去稀硫酸的质量为 g。
(2)计算稀硫酸中溶质的质量分数。
为测定某镁矿石中镁元素的质量分数,兴趣小组的同学取了5g该镁矿石粉末,加入过量的稀硫酸,充分反应后过滤、除杂,得到只含有MgSO4和H2SO4两种溶质的混合溶液100g,将该100g混合溶液放于烧杯中,然后取40g氢氧化钠溶液,分4次加入到盛有100g混合溶液的烧杯中,充分反应,测得的实验数据如下表所示:
实验编号 |
第一次 |
第二次 |
第三次 |
第四次 |
加入氢氧化钠溶液质量/g |
10 |
10 |
10 |
10 |
烧杯中生成沉淀的总质量/g |
0.464 |
1.044 |
1.160 |
1.160 |
请计算:
(1)100g混合液中硫酸镁的质量。
(2)该镁矿石中镁元素的质量分数。(假设5g镁矿石中的镁元素全部转化为100g混合溶液中MgSO4中的镁元素)
(3)加入的氢氧化钠溶液的溶质质量分数。
试题篮
()