某化学兴趣小组欲测定某石灰石样品中碳酸钙的质量分数,先将10g样品放入烧杯中,再把100g稀盐酸分5次加入该样品中(该实验条件下,杂质不与酸反应,也不溶解于水,忽略稀盐酸挥发),得实验数据如表格。
稀盐酸的质量 |
充分反应后剩固体的质量 |
第一次加入20g |
8g |
第二次加入20g |
6g |
第三次加入20g |
4g |
第四次加入20g |
2g |
第五次加入20g |
2g |
请计算;
(1)10g石灰石样品中碳酸钙的质量分数是 。
(2)求稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%)。
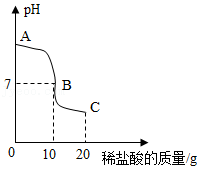
常温下,一锥形瓶中盛有10g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加一定溶质质量分数的稀盐酸,用pH传感器测得溶液pH与加入稀盐酸的关系曲线如图所示,请回答下列问题:
(1)图中B点溶液呈 色。
(2)计算稀盐酸中溶质质量分数。(写出计算过程)
孔雀石的主要成分是Cu2(OH)2CO3,还含有Fe2O3、Al2O3、SiO2杂质,用该矿石制备Cu的流程如图所示(部分产物略去):
 (1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(1)过程①中,操作a是溶解和 ,还有一种气体产物是 ,滤液X中含有的金属阳离子为 。
(2)过程①中硫酸略过量,则过程②调pH除杂的最佳试剂是 (选填“CuO”或“Na2CO3”)。
(3)下列关于制取铜的两种方案的说法,正确的是 。
A.“方案一”得到的铜产品更纯
B.“方案一”不存在消耗能量的问题
C.“方案二”需考虑废气污染的问题
D.“方案二”得到纯铜的产率更高
(4)过程③发生的反应:2CuSO4+2H2O 2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
2Cu+O2↑+ (补充完方程式),当收集到800t氧气时,产生Cu的质量是多少?(写出必要的计算过程)
某石灰水中含有氢氧化钙1.48g,要使该石灰水中的氢氧化钙转化为碳酸钙沉淀,至少需要二氧化碳的质量是多少?
电解水时常在水中加入少量的Na2SO4,既可增强溶液导电性,Na2SO4又不参与反应。如图水槽中有86.8g水,某兴趣小组把4.0g Na2SO4固体加入水中,充分溶解后进行电解。一段时间后停止通电,在试管A中收集到1.2g气体。回答下列问题:
(1)水的相对分子质量为 。
(2)B管中收集到的气体的质量是 g。
(3)电解后溶液中Na2SO4的质量分数是多少?(写出计算过程)

某课外活动小组同学取一定量的铜与氧化铜的粉末固体混合物放入烧杯中,加入50g稀硫酸,恰好完全反应,烧杯中固体的质量随时间变化情况如图所示。计算所用稀硫酸的溶质质量分数。

某补钙片的主要成分为CaCO3,每片钙片重0.5g(假设钙片中其他成分不含钙元素,不溶于水且不与任何物质发生反应)。化学兴趣小组为测定钙片中钙元素的含量,进行了如图实验:
根据图示信息,完成下列各题:
(1)钙片中钙元素的质量分数为 。
(2)求恰好完全反应时所得溶液的溶质质量分数?(要求写出计算过程)
目前,新型冠状病毒肺炎疫情形势依然严峻,为做好个人防护,生活中常用75%的乙醇溶液进行手部消毒。另外,乙醇还用作酒精灯的燃料,酒精灯添加燃料不得超过其容量的 ,约含乙醇92g。已知:乙醇完全燃烧的反应为C2H5OH+3O2
,约含乙醇92g。已知:乙醇完全燃烧的反应为C2H5OH+3O2 2CO2+3H2O。请问:
2CO2+3H2O。请问:
(1)从是否含碳元素的角度,乙醇属于 (填“有机物”或“无机物”);
(2)92g乙醇完全燃烧,消耗氧气的质量是多少(写出计算过程)。
某氯碱工厂用电解饱和食盐水制取烧碱,原理为:2H2O+2NaCl 2NaOH+H2↑+Cl2↑,另将生成的H2与Cl2恰好完全化合生成HCl制取浓盐酸。现将22.1t饱和食盐水电解完全(忽略水的挥发和气体的溶解),共收集到H2为0.1t。试计算:
2NaOH+H2↑+Cl2↑,另将生成的H2与Cl2恰好完全化合生成HCl制取浓盐酸。现将22.1t饱和食盐水电解完全(忽略水的挥发和气体的溶解),共收集到H2为0.1t。试计算:
(1)NaOH中质量分数最大的元素为 。
(2)电解后所得烧碱溶液的溶质质量分数(结果精确到0.1%)。
(3)制得溶质质量分数为36.5%浓盐酸的质量。
二氧化氯(ClO 2)常用于自来水消毒,工业制取原理为:2NaClO 3+4HCl(浓)═2ClO 2↑+2NaCl+Cl 2↑+2H 2O。某工厂将30kg NaClO 3固体加到100kg浓盐酸中,反应一段时间后,生成13.5kg ClO 2(生成的气体全部逸出,其它物质全部形成溶液)。
已知:NaClO 3和ClO 2的相对分子质量分别为106.5和67.5。
试计算:
(1)NaClO 3中钠元素和氧元素的质量比为 。
(2)参加反应的NaClO 3的质量。
(3)所得溶液中NaClO 3的质量分数(计算结果精确到1%)
钙是生物体骨骼的重要组成元素。鱼骨中含有碳酸钙,现设计图甲实验测定鱼骨中的碳酸钙含量,并将测得的数据绘制成图乙。

提示①食醋的主要成分是醋酸(HAc)。醋酸和碳酸钙反应的化学方程式为CaCO3+2HAc═CaAc2+H2O+CO2
②鱼骨中其它成分与食醋反应生成的气体可忽略不计
(1)该实验中浓硫酸的作用是 。
(2)由图乙中的AB曲线,可知锥形瓶中反应速率的变化情况是 (选填“变大”、“变小”或“不变)。
(3)根据图中的数据计算鱼骨中碳酸钙的质量分数。
(4)生活中,用喝醋的方法除去卡在咽上的鱼刺,这种做法是不科学的。请你结合实验结果加以说明 。
2021年3月,中央财经会议明确把碳达峰、碳中和纳入生态文明建设整体布局,争取在2060年前实现碳中和。“碳中和”是指在一定时间内产生的二氧化碳排放总量,通过二氧化碳去除手段来抵消掉这部分碳排放,达到“净零排放”的目的。
(1)二氧化碳是引起温室效应的主要气体,根据图甲回答支持这一结论的信息是: 。

(2)科学家已经研究出多种方式来实现二氧化碳的转化。
①固碳的另一种方法是将收集的二氧化碳和水混合后注入地下玄武岩中,最终与岩石中的矿物质作用形成固态的石头碳酸盐。这种固碳方式属于 变化(选填“物理”或“化学”)。
②我国研发的“液态太阳燃料合成技术”(图乙),甲醇(CH3OH)等液体燃料被形象地称为“液态阳光”。甲醇制取过程中能量转化是:太阳能→电能→ 能。甲醇合成时,若碳元素全部来自于二氧化碳,则制取10吨甲醇需要消耗二氧化碳 吨。
(二氧化碳转化成甲醇的方程式为:CO2+3H2 CH3OH+H2O)
CH3OH+H2O)
小宁用稀盐酸和石灰石反应制取二氧化碳(石灰石中的杂质既不溶于水也不和酸反应),为了探究反应后溶液的成分,他又进行如下实验:取反应后的溶液50g于烧杯中,逐滴滴入碳酸钠溶液,发现先有气泡产生,后生成白色沉淀。下表为产生的气体总质量、沉淀总质量与滴入碳酸钠溶液总质量的关系。
碳酸钠溶液总质量/g |
25.0 |
50.0 |
75.0 |
100.0 |
125.0 |
150.0 |
175.0 |
200.0 |
气体总质量/g |
1.1 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
2.2 |
沉淀总质量/g |
0 |
0 |
2.5 |
5.0 |
m |
n |
9.0 |
9.0 |
(1)表中n= 。
(2)所取的反应后50g溶液中溶质是 。
(3)所用碳酸钠溶液中溶质的质量分数是多少?
氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。实验室中制备KClO3的化学反应方程式为3Cl2+6KOH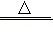 5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
5KCl+KClO3+3H2O。若用Cl2与200g的KOH溶液恰好完全反应,反应后溶液质量为221.3g。计算:
(1)参加反应的氯气的质量为 g。
(2)所用KOH溶液中溶质的质量分数是多少?
试题篮
()