有一含有纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取30g的样品放入烧杯中,向烧杯中加入100g足量的稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为123.4g(假设产生的气体全部逸出。)
(1)反应中生成的气体的质量是 g;
(2)样品中碳酸钠的质量分数是多少?
(1)用氯化钠固体配制100 g溶质质量分数为12%的NaCl溶液的操作步骤为 、 、 、 。如果将这100 g溶质质量分数为12%的NaCl溶液加水稀释为4%的NaCl溶液需加水 g。
(2)某课外兴趣小组对实验室中的一瓶稀硫酸样品进行分析。他们分别用100g稀硫酸与不同质量的锌粒(含杂质,杂质不与稀硫酸反应)反应,三次实验的数据如下表。
| 实验次数 |
1 |
2 |
3 |
| 加入锌粒的质量(g) |
4 |
8 |
12 |
| 充分反应后剩余物质的总质量(g) |
103.9 |
107.8 |
111.8 |
请回答下列问题:
①第 次实验,锌粒与稀硫酸恰好完全反应。
②计算稀硫酸的质量分数(写出计算过程)。
一定质量的金属铁和稀硫酸恰好完全反应,产生气体的质量为0.2g
(1)反应后溶液中溶质FeSO4的质量为 g.
(2)向反应后的溶液中加入BaCl2溶液,当加入的BaCl2溶液质量为208g时,恰好完全反应,此时生成沉淀的质量为 g.
(3)计算所加BaCl2溶液的溶质质量分数 .
现有氯酸钾和二氧化锰的混合物共26.5g,待反应不再有气体生成后,将试管冷却,得到剩余固体16.9g,求:
(1)制取氧气的质量?
(2)剩余固体中含有的各物质的质量为多少克?
在氯化钙和氯化钠的混合物中加入一定量的水,全部溶解得到50克混合溶液,向该溶液中逐滴加入一定溶质质量分数的碳酸钠溶液,生成沉淀与加入碳酸钠溶液的质量关系如图所示.计算:
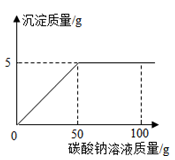
(1)所加碳酸钠溶液的溶质质量分数.
(2)若恰好完全反应时所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
根据《羊城晚报》报道:今年8月,有十几个民工饮用散装酒后双目失明,继而死亡。据调查,散装酒中含有超标的有毒物质甲醇,其化学式为:CHXO,求:
(1)已知甲醇的相对分子质量为32,则X为 ;
(2)甲醇完全燃烧时,生成二氧化碳和水,发生如下反应:2CHXO + 3O2 CO2+4H2O
CO2+4H2O
则生成二氧化碳和水的质量比为 。
(3)如果甲醇在氧气中不完全燃烧可发生如下反应:8CHXO + nO2 mCO2+2CO+16H2O
mCO2+2CO+16H2O
若反应生成3.6g水,请计算:
①m值是 ;
②参加反应的氧气质量是多少克?(写出规范步骤并计算)
取氯酸钾和二氧化锰的混合物26g,加热至混合物固体质量不再减少为止,冷却后称得剩余固体质量为16 .4g。计算:
(1)生成氧气的质量
(2)原混合物中氯酸钾的质量
盐酸、氢氧化钠是常见的酸碱。
(1)盐酸溶液中阳离子符号是 ,氢氧化钠的俗称是 (写一种)。
(2)向稀氢氧化钠溶液中滴入酚酞溶液。当滴入稀盐酸至完全中和时。溶液的颜色变化是 ,取少量中和后的溶液加热蒸干,现象是 。
(3)根据化学方程式计算,含HCl 7.3g的稀盐酸可中和氢氧化钠的质量为多少?
某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液20g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?(写出计算过程)
把干燥的KClO3固体15g与5gMnO2混合均匀,装入大试管中,加热制氧气。待反应一段时间后停止加热,将试管冷却,称量得剩余固体的质量为15.2g。试计算:(1)反应后生成多少克氧气?
(2)反应后剩余固体中含有哪些物质?各多少克?
新的一年,同学们的学习方式有了很大变化。下面是《气体制取与收集》学习的课堂片段:
【自主学习】仿照氧气制取的学习和气体制取的一般思路,阅读课本,老师提供了几组药品,让同学们交流并选出适宜实验室制取二氧化碳的一组。
【合作交流】围绕以上问题,各小组展开了激烈的交流,下面是老师从第二小组同学交流中听到的各位学生的发言:
1号:碳酸盐用块状石灰石(主要成分碳酸钙),为什么不用纯碱(碳酸钠)呢?
3号:碳酸钠是粉未状的,反应的速度太快,不易控制,
2号:同意3号同学的说法,那我们把碳酸钠压制成块状可以吗?
各位都在思考,问题未能解决。
【展示释疑】通过各个小组的展示,大家明白了实验室制取二氧化碳应该选择石灰石和稀盐酸。
实际实验中,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题。
请你帮助二组学生解决2号学生提出的问题,实验室把碳酸钠压制成块状_______(选填“可以”或“不可以”)代替石灰石制取二氧化碳。
【能力提升】某小组想测定所用石灰石样品中碳酸钙的质量分数,取用了2g的石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中,(样品中除碳酸钙外,其余成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下:
| 稀盐酸的用量 |
剩余固体的质量 |
| 第一次加入5g |
1.5g |
| 第二次加入5g |
1.0g |
| 第三次加入5g |
0.5g |
| 第四次加入5g |
0.3g |
(1)从以上数据可知,这四次实验中,第______次石灰石样品中碳酸钙已完全反应。
(2)求石灰石中碳酸钙的质量分数?
(3)求检测过程中所产生二氧化碳的质量?
将91.6g氢氧化钾溶液与一定质量的氯化镁溶液混合,恰好完全反应,过滤后,得到11.6g沉淀和280g滤液,求氯化镁溶液的溶质质量分数.
赤铁矿是常用的炼铁原料,其主要成分为氧化铁(其余为杂质,且杂质中不含有铁元素)求:(1)氧化铁中各元素的质量比;(2) 氧化铁中铁元素的质量分数;
(3)若赤铁矿中含有氧化铁质量分数为80%,则200g该铁矿石中含有多少克铁元素?
试题篮
()