某学习小组欲测定刚配制的BaCl2溶液中溶质的质量分数,采取下列两种方法:
方法1:取100gBaCl2溶液,加入适量的AgNO3溶液,两者恰好完全反应,并测得生成AgCl沉淀的质量为m1g;
方法2:取100gBaCl2溶液,加入m2g溶质的质量分数为a%的Na2SO4溶液,恰好使BaCl2溶液完全沉淀;
已知相关物质的相对分子质量:BaCl2=208 Na2SO4=142 AgCl=143.5
(1)请任选一种方法计算该BaCl2溶液中溶质的质量分数(写出详细的计算过程);
(2)如果采取上述两种方法,可推知a= (用含m1、m2的代数式表示)
实验室现有一瓶标签破损的稀硫酸溶液,为了测定其溶质的质量分数,某同学进行了以下实验:用一个洁净的小烧杯取该溶液100克,向其中加入足量的锌粒,充分反应后,烧杯内剩余物质的质量减少了0.4克。(反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑)试求:
(1)H2SO4的相对分子质量
(2)该稀硫酸溶液中溶质的质量分数(要求:结合化学方程式计算,并写出计算过程)
某化学兴趣小组为研究酸的化学性质,他们将一定量稀硫酸加入到盛有少量CuO的试管中,观察到黑色粉末全部溶解,溶液呈 色,该反应的化学方程式为 。为进一步确定反应后所得溶液中的溶质成分,他们进行了以下实验探究。
【提出猜想】猜想一: ;猜想二:H 2SO 4和CuSO 4
【资料查询】CuSO 4溶液呈弱酸性,加入Zn粒时有极少量的气体产生。
【实验探究】为了验证猜想,该兴趣小组的同学设计了如下实验方案。
方案一:取所得溶液少许于试管中,滴入石蕊试液,振荡,若观察到溶液显红色,则猜想二正确。
方案二:取所得溶液少许于另一支试管中,加入足量Zn粒,若观察到产生大量气体、 等现象,则猜想二正确。
【讨论交流】A、经过讨论,大家一致认为方案一是错误的,其理由是 。
B、要使由H 2SO 4和CuSO 4组成的混合溶液中的溶质只有CuSO 4,可向其中加入过量的 (填序号)。
a、CuO b.Cu(OH) 2 c、Cu d.Cu(NO 3) 2
【拓展探究】某混合溶液由硫酸和硫酸铜溶液组成。上述小组同学又进行了如下实验:取124.5g该混合溶液于烧杯中,然后将120gNaOH溶液分六次加入其中,毎次充分反应后称量所得溶液的质量,所测数据如下表所示。
| |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
第6次 |
| 加入NaOH溶液的质量/g |
20 |
20 |
20 |
20 |
20 |
20 |
| 反应后溶液的质量/g |
144.5 |
164.5 |
179.6 |
189.8 |
200 |
220 |
| 每次产生沉淀的质量/g |
0 |
0 |
m |
n |
9.8 |
0 |
计算:
(1)上述表格中产生沉淀的质量:m= ,n= 。
(2)所加NaOH溶液中溶质的质量分数。
(3)第5次加入NaOH溶液充分反应后所得溶液中溶质的质量分数。
某同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下

请回答下列问题:
(1)滤液可作化肥使用,你认为它属于 肥;
(2)该同学制得氧气的质量 g;
(3)计算滤液中溶质质量分数。
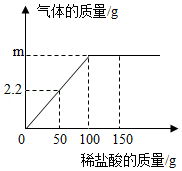
小苏打是发酵粉的主要成分之一,可用于制作发面食品。一化学兴趣小组对某小苏打样品中各成分的含量做了如下测定:将一定质量的该样品(已知杂质只含NaCl)加水全部溶解后,得到104.4g溶液,向该溶液中逐渐加入稀盐酸,产生的气体与加入稀盐酸的质量关系如图所示。试计算:
(1)m的值为 。
3与NaCl的质量比 。
某化学兴趣小组为了测定某纯碱样品(只含有Na2CO3、NaCl)中Na2CO3质量分数,取5克样品,往其中加入一定质量的稀盐酸,产生气体的质量与所加稀盐酸的质量变化如图,试计算:
(1)共产生 克二氧化碳;
(2)该纯碱样品中Na2CO3的质量分数;
(3)求恰好完全反应时所得溶液的质量分数?

小莉同学家里有一只破损的手镯(银锌合金),她想探究此手镯中银的含量,于是请化学老师一起探究。首先称得手镯质量为22.8g,在用足量的稀硫酸分多次与此手镯充分反应,实验结果如表:
| |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
| 滴入稀硫酸的质量/g |
20 |
20 |
20 |
20 |
20 |
| 充分反应后剩余固体质量/g |
21.5 |
20.2 |
18.9 |
18.5 |
18.5 |
根据上表中的数据分析,完成下列问题:
(1)手镯中银的质量是: g.
(2)所用稀硫酸的溶质质量分数是多少?
某同学用自制电解器电解水,为了加快电解速率,可在水中加少许硫酸钠增强其导电性,当他在93.6g质量分数为5%的硫酸钠溶液中通电一段时间后,正极上产生3.2g氧气,计算:
(1)负极上产生氢气的质量;
(2)通电后溶液中硫酸钠的质量分数;
(3)该同学认为电解速率较慢,又继续向通电后的溶液中加入硫酸钠,若要使溶液中溶质的质量分数变为10%,则需要加入硫酸钠固体的质量是多少?
工业上常用一定浓度的稀硫酸对表面生锈的铁件进行酸洗.某酸洗池里盛有440kg质量分数为40%的硫酸溶液,放入表面生锈的铁件浸泡,浸泡过程中单质铁也有部分损失,假设溶液中只发生了如下反应:
Fe 2O 3+3H 2SO 4=Fe 2(SO 4) 3+3H 2O
Fe+Fe 2(SO 4) 3=3FeSO 4
取出铁件用水冲洗,冲洗液倒入酸洗池中合并共得到580kg溶液,其中只有H 2SO 4和FeSO 4两种溶质,经过测定硫酸的质量分数降低到5%.计算:
(1)消耗H 2SO 4的质量.
(2)损失的单质铁的质量.
(3)要使H 2SO 4的质量分数恢复到40%,需要加入质量分数为98%的硫酸的质量.
为测定某硫酸溶液中溶质的质量分数,化学小组同学取10g该硫酸溶液,向其中加入21.2gBaCl 2溶液,二者恰好完全反应,过滤后称得滤液的质量为28.87g。请计算:
(1)反应后生成沉淀的质量是 g。
(2)该该硫酸溶液中溶质的质量分数。(计算结果精确到0.1%)
某化学兴趣小组,为了测定铜锌合金样品中锌的含量,称取样品20克于烧杯中,向其中加入50克稀硫酸至恰好完全反应,反应后烧杯中物质的总质量为69.8克,求:
(1)样品中锌的质量分数?
(2)恰好完全反应后所得溶液中溶质的质量分数?
学习了酸和碱的知识后,阿达力同学知道了白醋的主要成分是醋酸(CH3COOH)。为了测定白醋中醋酸的质量分数,他在30g白醋中滴加5.6%的氢氧化钾溶液,反应完全共用去氢氧化钾溶液100g(其他成分不参加反应)。
(化学反应方程式为:CH3COOH+KOH═CH3COOK+H2O)
请计算:(1)氢氧化钾溶液中溶质的质量为 g;
(2)白醋中醋酸的质量分数为多少?
向100g硫酸铜溶液中,逐滴加入NaOH溶液,化学反应方程式为:
CuSO 4+2NaOH═Cu(OH) 2↓+Na 2SO 4
加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:
(1)Cu(OH) 2质量为 g;
(2)计算硫酸铜溶液溶质质量分数(请写出计算过程)。

试题篮
()