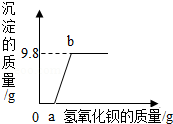
某溶液中可能含有盐酸、硫酸、硝酸钠、氯化铜中的一种或几种,为了探究其组成,取一定质量的该溶液,向其中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。请回答下列问题。
(1)该溶液中一定含有的溶质是 ,可能含有的溶质是 。(均填化学式)
(2)请写出上述过程中发生中和反应的化学方程式 。
(3)当滴加氢氧化钡溶液至图中b点时,溶液中一定含有的溶质是 。(填化学式)
(4)所取溶液中含有氯化铜的质量为 。
按下列要求各写一个化学方程式(1分×4=4分)
(1)实验室用固体混合物制氧气
(2)高炉中炼铁的原理
(3)用纯碱制烧碱
(4)波尔多液不能用铁制容器盛装
化学用语是国际通用的化学语言,是学习化学的重要工具,请用化学用语回答下列问题:
(1)红磷在空气中燃烧产物的化学式 ;
(2)烧碱溶液、食盐溶液中都存在的金属离子 ;
(3)硝酸铵中质量分数最大的元素 ;
(4)通过化合反应生成水的化学方程式 .
50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到222.8g固体(已换算成无水硫酸盐)。则反应产生氢气的质量是 g。
波尔多液是一种农药,由Ca(OH) 2溶液和CuSO 4溶液混合而成。某农场需要大量的波尔多液,农场工人就地取材,利用农场废弃的铜渣(只含有铜和一定量的铁)和附近的石灰石来制作波尔多液。下面是制作波尔多液的工艺流程图:

请回答下列问题:
(1)CaO的俗名是 ,写出由CaO生成Ca(OH) 2的化学方程式 。
(2)请说出如何由铜渣得到纯净的铜 。
(3)B物质是 ,写出由B物质生成CuSO 4的化学方程式 。
(4)将铜渣与Zn按质量比10:1的比例分别加入到足量的盐酸溶液中,产生H 2的质量恰好相等,铜渣中铜的质量分数是 。(精确到0.1%)
对于化学反应:2A =" 2B" +C,已知:反应生成B和C的质量比为B∶C = 1∶8。请填空:
| 物质 |
A |
B |
C |
| 反应前质量/g |
100 |
0 |
5 |
| 反应后质量/g |
64 |
|
|
乙醇俗称酒精,可以用作酒精灯、内燃机等的燃料,用灯帽盖灭酒精灯的灭火原理是 ;乙醇完全燃烧的化学方程式为 ;现有乙醇和乙醛(CH3CHO)的混合物共13.4g,完全燃烧后生成26.4g CO2,则生成水的质量为 g。
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。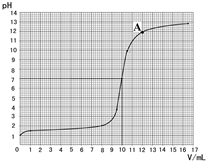 (2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)
测定溶液的pH,得到的数据如下:
| 加入氢氧化钠 的体积/mL |
0 |
1.0 |
8.0 |
9.5 |
10.5 |
12.0 |
16.5 |
| 烧杯中溶液pH |
1.0 |
1.3 |
2.0 |
3.9 |
9.9 |
11.9 |
12.8 |
依据表中数据绘制出烧杯中溶液的pH与加入氢氧
化钠溶液体积(V)之间的变化关系图。
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为 mL,A点所表示的溶液中溶质的化学式为 。
(4)计算此瓶盐酸的溶质质量分数。(请写出计算过程。氢氧化钠溶液的密度按1.0g/mL计算)
取6.4g表面部分被氧化的镁条放入烧杯中,加入100g溶质质量分数为19.6%的稀硫酸,恰好完全反应,则反应后生成硫酸镁的质量为 g.
金属在生产、生活和社会发展中应用较为广泛,中国制造,让世界瞩目!
(1)航天:我国用长征三号乙运载火箭成功发射第55颗北斗导航卫星,化学材料在其中起到了重要作用,铝合金和钛合金被广泛用于航天工业、一般情况下,铝合金的强度和硬度比纯铝 (填“高”或“低”)。
(2)交通:制造港珠澳大桥需要大量的钢铁,请写出一种防止钢铁生锈的方法: 。
(3)冶炼:我国湿法炼铜很早就有记载,东汉《神农本草经》曾记载石胆“能化铁为铜”。向硝酸铜和硝酸银的混合溶液中加入一定量的镁粉,充分反应后过滤,滤液呈蓝色,则滤出的滤液中一定含有金属离子是 。
(4)应用:随州编钟被誉为“世界第八大奇迹”,代表了我国古代青铜工艺的较高水平,青铜是铜锌合金。现有铜锌合金质量20克,与100克质量分数为19.6%的稀硫酸恰好完全反应,则铜锌合金中铜的质量分数为 。
实验室里,常采用加热高锰酸钾或分解过氧化氢的方法制氧气。
(1)高锰酸钾属于 (填"酸"、"碱"或"盐"),用它制氧气的化学方程式是 。
(2)高锰酸钾制氧气的实验中,不需要使用的一组仪器是 (填序号)。
a.烧杯 玻璃棒
b.大试管 集气瓶
c.酒精灯 铁架台
d.导管 单孔塞
(3)利用化学方程式计算,制取4.8g氧气,至少需要过氧化氢的质量是多少?
碳酸钠俗称纯碱或苏打,在生活、生产和实验研究中均有广泛应用。
[配制溶液]配制溶质质量分数分别为1%、2%和4%的Na2CO3溶液
(1)若配制50g溶质质量分数为4%的Na2CO3溶液,下列操作正确的是 (填字母)。
a.用托盘天平称取2g Na2CO3固体
b.选用50mL量筒量取所需体积的水
c.选用带玻璃塞的广口试剂瓶,将配好的溶液装瓶并贴标签
(2)分别测定25℃时,上述3种溶液的pH,记录数据如下:
实验编号 |
Ⅰ |
Ⅱ |
III |
溶质质量分数 |
1% |
2% |
4% |
溶液pH |
11.62 |
11.76 |
11.90 |
分析Ⅰ、Ⅱ、Ⅲ三组数据可得出的结论是 。
[制备物质]用Na2CO3溶液和FeSO4溶液发生复分解反应制备FeCO3
[已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀]
(3)在烧杯中制备FeCO3沉淀时,应选用的加料方式是 (填字母)。
a.将FeSO4溶液与Na2CO3溶液同时加入到烧杯中
b.将Na2CO3溶液缓慢加入到盛有FeSO4溶液的烧杯中
c.将FeSO4溶液缓慢加入到盛有Na2CO3溶液的烧杯中
(4)潮湿的FeCO3固体置于空气中易变质,反应如下:4FeCO3+6H2O+O2═4X+4CO2.则X的化学式为 。
[标定浓度]标定待测盐酸的溶质质量分数
(5)将Na2CO3固体在270℃干燥至恒重,准确称取0.212g无水Na2CO3于锥形瓶中,加入50mL蒸馏水溶解,滴入待测盐酸,当两者恰好完全反应时,消耗盐酸的体积为20.00mL(该盐酸的密度近似等于lg•mL﹣1,反应中Na2CO3所含的碳元素全部转化为CO2)。
①列式计算待测盐酸的溶质质量分数(结果用百分数表示,保留两位小数)。
②若上述测定过程中Na2CO3固体未经充分干燥,则测出盐酸的溶质质量分数将 (填“偏大”、“偏小”或“无影响”)。
化学与生产和生活密切相关。请回答下列问题:
(1)俗语道“酒香不怕巷子深”,原因是 (用微粒的观点解释)。
(2)武德合金常用作保险丝,是因为合金的熔点比组成它的纯金属的熔点要 (填“高”或“低”)
(3)“灯影牛肉”是达州的一张美食名片,其牛肉中主要含有的营养物质是 (填字母序号)。
A.糖类 B.蛋白质 C.油脂 D.维生素
(4)华为公司研发了一种以甲醇为原料的新型手机电池,其容量为锂电池的10倍,可连续使用1个月才充一次电,其电池反应原理为:2CH3OH+3X+4NaOH═2Na2CO3+6H2O.其中X的化学式为 。
(5)人们在使用含碳燃料过程要注意通风,如果氧气不足会产生一氧化碳,使人中毒。某液化石油气中含有丙烯,其化学式为C3H6.小王同学取4.2g丙烯和12.8g氧气在一密闭容器中点燃,恰好完全反应,测得生成二氧化碳的质量8.8g,一氧化碳的质量2.8g,那么生成水的质量 g,写出该反应的化学方程式 。
质量相等的四种物质①H2O2②KMnO4③KClO3④H2O,完全分解后所制得氧气的质量由大到小的顺序为 (填序号,下同);四种金属①Zn②Mg③Al④Fe分别投入质量相等且足量的稀硫酸中,充分反应后所得四种溶液的质量相等,则投入金属的质量由小到大的顺序为 。
复习课上,老师要求学生用不同的方法鉴别稀硫酸和氢氧化钠溶液。小东、小南两位同学取同一溶液分别进行如下实验:
【实验方案】
| 实验步骤 |
实验现象 |
实验结论 |
|
| 小东 |
用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH |
pH试纸变色 pH7(填">"或"<") |
该溶液是氢氧化钠溶液 |
| 小南 |
取适量溶液于试管中,加入经打磨过的铝条 |
有气泡产生 |
该溶液是稀硫酸 |
【提出问题】为什么我们取相同溶液而实验结论却不同呢?
【解决问题】
小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是,于是一致认为该溶液是氢氧化钠溶液。为什么小南加入铝条会有气泡产生呢?通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是:
。
【拓展延伸】利用老师要求鉴别的那两种溶液,测定镁铝铜合金中各成分的含量。实验设计如下:

【回答问题】
(1)写出操作I中玻璃棒的作用:。
(2)a溶液是,选择该溶液的理由是。
(3)金属铜的质量为g,固体A含有的物质是,溶液A中所含溶质是。
试题篮
()