化学来源于生活又服务于生活。下表是生活中常用物质溶液的pH及主要成分化学式:
| 序号 |
① |
② |
③ |
④ |
⑤ |
| 名 称 |
食 醋 |
白 酒 |
白糖水 |
石灰水 |
纯碱溶液 |
| 主要成分 |
CH3COOH |
C2H5OH |
C12H22O11 |
Ca(OH)2 |
Na2CO3 |
| 溶液pH |
3 |
7 |
7 |
11 |
8 |
请结合上表信息回答下列问题:
(1)当你被蚊虫叮咬(释放一种酸性物质)后,为减轻疼痛,可在叮咬处涂(填序号);
(2)用久的铝壶内有水垢(主要成分为
),可用(填序号)少量多次清除。
小明同学取下列生活中的物质,测得其pH如下表所示:
| 物质 |
肥皂水 |
雨水 |
糖水 |
柠檬汁 |
洗洁精 |
| pH |
10.2 |
5.2 |
7.0 |
2.5 |
12.2 |
由此判断:
(1)酸性最强的物质是__________________________。
(2)能使无色酚酞试液变红色的物质是____________。(填一种即可)
(3)正常雨水的pH约为5.6。小明生活的环境所降的雨水_____________(填“属于”或“不属于”)酸雨。
(4)常用于改良酸性土壤的碱是____________(填化学式)
氢氧化钠溶液露置在空气中易发生变质,有关反应的化学方程式为____.利用某种试剂,既能证明氢氧化钠溶液已经变质,同时,适量的该试剂又能除去氢氧化钠溶液部分变质而生成的少量杂质,该试剂可以是____,有关反应的化学方程式为____.
A、B、C、D、E五种物质为初中化学中常见的化合物,它们之间的关系如
图所示(连线表示能发生化学反应)。 A、C、E均为氧化物,且A是一种常见的温室气体;B溶液的pH<7,实验室常用它制取A或H2;而D常用于检验A;C和E反应能生成D。
(1)固态A的俗名是 ▲ ,固态E的俗名是 ▲ ;
(2)用D检验A的化学方程式为 ▲ ;
(3)图中中和反应的化学方程式为 ▲ 。
某化学兴趣小组的同学对一瓶久置的熟石灰粉末的组成进行实验探究,请你
一起参与他们的探究活动。
[提出问题]这瓶熟石灰粉末是否已经变质生或了CaCO3?
[进行猜想]猜想一:熟石灰全部变成了CaCO3。
猜想二:熟石灰部分变成了CaCO3。
猜想三:熟石灰没有变质。
[设计实验]该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容。
| 实验步骤 |
实验现象 |
实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞试液 ③取少量滤渣于试管中,加入盐酸 |
② 。 ③ 。 |
猜想成立 |
[反思与应用]①要证明猜想二成立,可参照上述实验方案进行探究,在步骤②中产生的实验现象是 。
②熟石灰变质是由于 的缘故。在初中化学我们所学过的物质中还有
(举一例)等具有这样的性质,因此象熟石灰这类物质在实验室应 保存。
重庆奉节盛产脐橙。脐橙适宜生长在pH为5.5~6.5的土壤环境中。为了防治脐橙在生长过程中发生“脐橙炭疽病”,可喷洒农药波尔多液(由硫酸铜、石灰加水配制而成)。根据上述材料回答下列问题:
(1)脐橙适宜生长在 (填“酸性”、“碱性”或“中性” )的土壤里;
(2)某块山地的土壤pH为4.8~5.5,欲种植脐橙,应采取的改良措施是:
;
(3)果农们在配制农药波尔多液时,均使用塑料桶或木桶,而不使用铁桶,其原因是(用化学方程式表示): ;
(4)脐橙生长过程中,叶色发黄,你建议农民伯伯们施用哪种化肥?
(填序号)
A.CO(NH2)2 B.KCl C.Ca3(PO4)2
有下列物质:①烧碱 ②浓硫酸 ③大理石 ④小苏打 ⑤甲烷 ⑥金刚石,请按下列要求填空(填序号):能用来划玻璃的是 ,能用来蒸馒头的盐是 ,瓦斯的主要成份是 ,可用做建筑材料的是 。
已知,A、B、C、D四种物质之间存在以下转化关系。其中C是单质,D是相对分子质量最小的氧化物 。试回答
。试回答
(1)写出A、C、D三种物质的化学式:A________、C_________、D_________。浅绿色溶液B中溶质的化学 式_______________。
式_______________。
(2)写出A→C的化学方程式_________________________________。
(3)写出C→D的化学方程式_________________________________。
人的胃液里含有适量盐酸。服用含MgCO3 的抗酸药可治疗胃酸过多症,有关反应的化学方程式为 ;该抗酸药说明书上标明的食用方法为“嚼食”,将药片嚼碎后服用的优点是 。
根据自己所学的知识回答下列问题:
(1)怎样准确测定土壤的酸碱度,叙述操作过程。
(2)污染空气的指数项目为 、 、 等。
(3)某化工厂购买的固体氢氧化钠没有密封保存,结果部分变质,我的分析是它吸收了空气中的 后又和空气中的 发生了反应,该反应的化学方程式为 ,检验该固体是否变质可选用试剂的化学式为 。
将一定质量的浓盐酸盛于烧杯中,敞口放置在实验室安全之处。
① 浓盐酸的质量和放置天数关系的曲线(见右图)正确
的是 (填写“甲”或“乙“)。 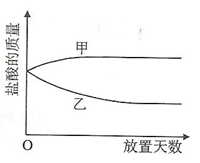
② 随着放置天数的增加,浓盐酸的质量发生变化的主要
原因是________ _____ ______。
③ 把浓盐酸稀释后可用于去除铁制品表面的铁锈(主要
成分为Fe2O3),反应的化学方程式是
写出下列物质(或主要成分)的化学式:
(1)食盐的主要成分 ;(2)黑火药成分之一硝酸钾 ;
(3)汽水中含有的碳酸 ;(4)中和胃酸用的氢氧化铝
某学校化学课外活动小组的同学,取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如下表所示:
| 测定时刻 |
5:05 |
5:10 |
5:15 |
5:20. |
5:25 |
5:30 |
| pH |
4.95 |
4.94 |
4.94 |
4.88 |
4.86 |
4.85 |
(1)所降雨水 _________(填“是”或“不是”)酸雨,在测定的时间内雨水的酸性____________(填“增强”或“减弱”)。
(2)经调查,这一地区有一个硫酸厂(生产过程中产生硫的氧化物)和一个电镀厂,这些工厂使用的燃料主要是煤(煤中含有硫元素)。另外,这一地区的生活燃料主要也是煤,还有液化石油气。试分析造成这一地区酸雨的主要原因是什么? 你认为应采取什么措施?
小军同学在学完“酸的化学性质”后,邀请你与他讨论“食醋在厨房中的妙用”:
(1)复习酸的化学性质
| ①酸与指示剂作用 |
酸溶液能使紫色石蕊溶液变红色 |
酸溶液不能使无色酚酞溶液变色 |
| ②酸与活泼金属作用 |
Fe+2HCl=FeCl2+H2↑ |
Fe+H2SO4=FeSO4+H2↑ |
| ③酸与某些金属氧化物作用 |
Fe2O3+HCl=FeCl3+H2O |
…… |
| ④…… |
|
由于小军的课堂笔记没做好“③酸与某些金属氧化物作用”后面的化学方程式未配平,请帮他写出配平后的化学方程式: 。
(2)讨论交流:① 小军自豪地说,目前世界卫生组织正在推广使用中国铁锅,使用铁锅炒菜时,放点食醋时,可以补充人体需要的微量元素 元素,该反应的原理是利用了酸的化学性质 (填表格中序号“①”、“②”或“③”)。
② 你告诉小军,食醋的作用远远不止这些呢,如 (任写一点食醋在生活中的妙用)。
(3)反思
盐酸、硫酸、食醋具有相似化学性质的原因是因为它们的水溶液中都含有 离子。
试题篮
()