某化肥厂生产的一种化肥包装袋上的部分说明如图所示。化学兴趣小组为测定其纯度,做了以下实验(杂质溶于水,且不与硝酸银溶液反应),请根据如图所示的实验过程和提供的数据进行计算。

(1)过滤后最终所得固体的质量为 g;
(2)所用硝酸银溶液的溶质质量分数是多少?(写出计算过程)
(3)该化肥是否合格?(写出计算过程,计算结果精确到0.1%)
实验室用质量分数为20.0%的稀硫酸处理含 的废液。向100.0g废液中加入稀硫酸至溶液恰好呈中性,最终得到2.33g沉淀。请计算:
(1)配制490.0g20.0%的稀硫酸需质量分数为98.0%的浓硫酸 g。
(2)废液中 的质量分数。
实验室有部分已变质为碳酸钠的氢氧化钠样品,质量为1.86g。某实验小组将此样品加入水中完全溶解,配成100g溶液,然后向其中缓慢滴加9.8%的稀硫酸,搅拌使气体全部逸出。滴加过程中,相关数据如表:
|
测定次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
|
滴加稀硫酸总质量/g |
0 |
10 |
20 |
30 |
40 |
|
溶液总质量/g |
100 |
110 |
119.56 |
129.56 |
m |
|
溶液pH |
13.3 |
10.2 |
7.0 |
0.9 |
0.8 |
请回答下列问题:
(1)氢氧化钠(NaOH)由 元素组成。
(2) 中碳原子与氧原子的个数比为 。
(3)第 次测定时,溶液中只有一种溶质。表中m= 。
(4)计算样品中碳酸钠( )的质量分数。(写出计算过程,结果精确到1%)
硫酸铜对过氧化氢( )的分解有催化作用。取8.5%的过氧化氢溶液40g倒入锥形瓶中,向其中加入15%的硫酸铜溶液6.6g,使过氧化氢完全分解,若产生的气体全部逸出,请计算:
(1)过氧化氢的相对分子质量为 。
(2)产生氧气的质量(写出计算过程)。
(3)反应后所得硫酸铜溶液中溶质的质量分数为 。
向氯化铜和盐酸的混合溶液中滴加一定溶质质量分数的氢氧化钡溶液,充分搅拌,加入氢氧化钡溶液的质量与生成沉淀的质量关系如图所示。
请完成下列问题:
(1)a点时,溶液的pH 7。
(2)求所用氢氧化钡溶液中溶质的质量分数。(写出计算过程)

我国明代科技著作《天工开物》中有利用炉甘石(主要成分是ZnCO3)火法炼锌的工艺记载,主要反应原理为ZnCO3+2C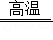 Zn+3CO↑,现用200kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。
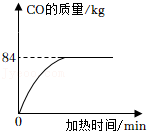
Zn+3CO↑,现用200kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。
(1)此过程中产生CO的质量是 kg。
(2)列式计算此炉甘石中ZnCO3的质量分数。
我国科学家在人工合成淀粉领域取得了突破性进展,其基本变化过程为“ 。”淀粉中C、H元素的质量之比为 _____,C的质量分数为_____ (计算结果保留一位小数,下同)。
氮肥有促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质含量的作用。 是一种常见的氮肥,请计算:
(1) 的相对分子质量_____;
(2) 中氮元素的质量分数_____(精确到 )。
小华同学为测定某稀盐酸中溶质的质量分数,在烧杯里放入一定质量的大理石,然后分次加入该稀盐酸,充分反应后测得生成二氧化碳的质量如表所示(大理石中的杂质不参与反应)。
加稀盐酸的次数 |
第一次 |
第二次 |
加稀盐酸的质量/g |
25 |
25 |
生成二氧化碳的质量/g |
2.2 |
1.1 |
(1)两次加稀盐酸后,生成二氧化碳的总质量是 g。
(2)计算该稀盐酸中溶质的质量分数(计算结果保留至0.1%)。
北京冬奥会最大的特点之一是“绿色环保”。运动员使用的可降解聚乳酸一次性餐具是以乳酸( )为主要原料得到的聚酯类聚合物。请你计算:
(1)乳酸中碳、氢、氧元素的质量比为 。
(2)乳酸中碳元素的质量分数为 。
N4O6是科学家发现的一种新型火箭燃料。试计算:
(1)N4O6中氮元素和氧元素的质量比是 (最简整数比)。
(2)152g N4O6中氮元素的质量是 g。
某氯化钠溶液中含有氯化镁(MgCl2),学习小组为测定其中氯化镁的质量分数,在50.0g该溶液中加入50.0g氢氧化钠溶液恰好完全反应,经测定生成沉淀的质量为2.9g。请回答下列问题:
(1)反应后溶液的质量为 g;
(2)求原氯化钠溶液中氯化镁的质量分数(写出计算过程)。
磷酸二氢钠(NaH2PO4)是我国自主研发的新型冠状病毒灭活疫苗(Vero细胞)的辅料之一。请计算:
(1)磷酸二氢钠中有 种元素;
(2)磷酸二氢钠中氢元素和氧元素的质量比为 (填最简比)。
葡萄糖(C6H12O6)是人类生命活动所需能量的重要来源,剧烈运动后肌肉酸痛是由于部分葡萄糖转化成了乳酸(C3H6O3)。
(1)C6H12O6的相对分子质量为 。
(2)葡萄糖中碳元素的质量分数 乳酸中碳元素的质量分数(填“>”、“<”或“=”)。
试题篮
()