水和溶液在生产、生活中起着十分重要的作用,请回答下列问题.
(1)硬水是指含有较多 的水,在生活中常采用 的方法降低水的硬度.
(2)NaCl、KNO 3两种物质的溶解度曲线如图所示.
在20℃时,KNO 3的溶解度与NaCl的溶解度相比,前者与后者的关系是 (填字母),在50℃时,KNO 3溶液的溶质质量分数与NaCl溶液的溶质质量分数相比,前者与后者的关系是 (填字母).
A.大于 B.小于 C.等于 D.无法确定
(3)不同温度下,氧气的溶解度随压强的变化如图所示,图中t 1对应的温度为40℃,则t 2对应的温度 (填字母)
A.大于40℃B.小于40℃C.无法确定
(4)若用溶质质量分数为16%的NaCl溶液和蒸馏水配制100g溶质质量分数为10%的NaCl溶液,则所需16%的NaCl溶液与蒸馏水的质量比为 .

资源、能源与环境已成为人们日益关注的问题。
(1)化石燃料包括 、石油和天然气,天然气的主要成分是 (写化学式)。
(2)二氧化硫和一氧化氮是大气污染物。请写出这两种气体的化学式并标出元素的化合价
、 。
(3)下列实验中,对应的现象以及结论都正确且两者具有因果关系的是 。
| 选项 |
实验 |
现象 |
结论 |
| A |
在空气中点燃纯净的氢气 |
燃烧,火焰为淡蓝色 |
氢气能支持燃烧 |
| B |
将铁丝和铜丝分别放入稀盐酸中 |
铁丝表面有气泡产生,铜丝表面无变化 |
铁的金属活动性比铜强 |
| C |
将二氧化碳通入紫色石蕊溶液中 |
紫色石蕊溶液变成红色 |
二氧化碳显酸性 |
| D |
高温下,将一氧化碳通过氧化铁粉末 |
黑色粉末变为红色 |
一氧化碳具有还原性 |
根据"粗盐中难溶性杂质的去除"实验,回答有关问题.
(1)实验步骤:
①溶解 称取5.0g粗盐,逐渐加入10mL水中,直到不再溶解,剩余粗盐1.2g.
②过滤
③蒸发 请从溶解度的角度分析,试验中不采用降低溶液温度的方法得到精盐的依据是
④计算产率 得到精盐3.2g,则精盐的产率为 (计算结果保留一位小数).
(2)整个实验中至少要进行 次称量.
(3)从海水中获得的粗盐,经过上述实验得到的精盐属于 (填"混合物"或"纯净物").
根据如图装置图,回答有关问题。

(1)写出装置图中标号仪器的名称:a ,b 。
(2)写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式 ,可选用的发生装置是 (填字母)。
(3)写出实验室用高锰酸钾制取氧气的化学方程式 ,如图E装置来收集氢气,当导管口气泡 放出时,再把导管口伸入盛满水的集气瓶,开始收集。
天然水净化为自来水的主要流程如下:
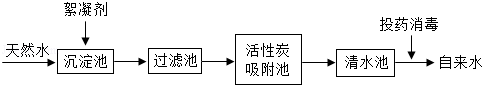
(1)下列说法不正确的是(填字母) .
A.过滤池可以除去难溶性杂质
B.活性炭吸附池可以除去水中的色素和臭味
C.清水池中一定是软水
(2)明矾[KAl(SO 4) m•12H 2O]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝.m= ,氢氧化铝的化学式为 .
(3)目前不少自来水用液氯(Cl 2)作为消毒剂,液氯注入水后发生反应的示意图:

其中"  "、"○"、"●"代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.
"、"○"、"●"代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用.
①C物质的水溶液能使紫色的石蕊溶液变成 色,取C物质的水溶液少许,向其中加入稀硝酸和硝酸银溶液,观察到有白色沉淀产生,发生反应的化学方程式是 ,利用此法可检验自来水中是否含有Cl ﹣.
②液氯与水反应的化学方程式是 .
(4)天然水中微生物使有机物(以C 6H 10O 5表示)转化为CO 2和H 2O的过程中所需O 2的量叫做生化需氧量(BOD,单位为mg•L ﹣ 1),反应的化学方程式为:C 6H 10O 5+6O 2 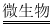 6CO 2+5H 2O,测得20℃时1L某天然水样中含有机物(C 6H 20O 5)的质量为10.8mg,则该水样的BOD值是多少?(写出计算过程)
6CO 2+5H 2O,测得20℃时1L某天然水样中含有机物(C 6H 20O 5)的质量为10.8mg,则该水样的BOD值是多少?(写出计算过程)
掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一.
①生活中,常会接触到下列物质:
A.铜丝 B.甲烷 C.过氧化氢 D.碘酒
其中属于混合物的是(填字母,下同) ,属于氧化物的是 .
②根据物质在转化过程中的特点,可将化学反应分为化合反应,分解反应、置换反应和复分解反应四种基本反应类型,下列转化不属于这四种基本反应类型的是 .
A.生石灰与水反应 B.一氧化碳还原氧化铁 C.中和反应
(2)实验是学习化学的一条重要途径,实验室中可用KClO 3在MnO 2催化下受热分解制取氧气,并将反应后的混合物进行分离回收,实验操作如图所示(MnO 2难溶于水)

①图A中试管口略向下倾斜的原因是 ,图B操作中玻璃棒的作用是 .
②图C操作中的一处明显错误是 ,图D操作中,当看到 ,停止加热.
(3)质量守恒定律是帮助我们学习的认识化学反应实质的重要理论.
①下列表述正确的是
A.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
B.每32g S和32g O 2完全反应后,生成64g SO 2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②有机化合物R与足量氧气置于密闭容器中充分反应生成CO 2和H 2O,实验测得反应前后物质的质量如下表:
| |
R |
O 2 |
CO 2 |
H 2O |
| 反应前质量/g |
46 |
128 |
0 |
0 |
| 反应后质量/g |
0 |
32 |
x |
54 |
则x= ,已知参加反应的物质R与氧气的分子个数之比为1:3,则R的相对分子质量是 .
化学使人类生活更美好.
(1)豆浆已成为众多家庭的饮品,下表是豆浆中部分营养成分的平均质量分数.请据表回答:
| 成分 |
蛋白质 |
油脂 |
糖类 |
钙 |
铁 |
维生素 |
| 质量分数/% |
1.8 |
0.7 |
1.1 |
0.01 |
0.0005 |
0.015 |
①豆浆中含有人体所需的微量元素是 ,青少年因缺 而导致佝偻病.
②豆浆所含的营养素中不能供给人体能量,但可以起到调节新陈代谢作用的是 (填字母,下同)
A.蛋白质 B.油脂 C.糖类 D.维生素
(2)材料对我们的生活影响越来越大.
①用作保险丝的武德合金属于
A.金属材料 B.合成材料 C.复合材料
②下列方法不能防止钢铁腐蚀的是
A.表面镀铬 B.表面涂油漆 C.部分浸入食盐水
③有一种用"冰蚕丝"面料做的衣服,面料的主要成分是合成纤维,鉴别"冰蚕丝"和天然蚕丝的化学方法是 .
实验Ⅰ:实验室制O 2。
【实验装置】如图1所示。
【实验步骤】
①检查装置气密性;
②向锥形瓶中加入MnO 2,塞进带导管和仪器A的双孔橡皮塞,关闭活塞C,向A中添加双氧水,塞上塞子B,将导管放入底部有少量黄沙的集气瓶中,盖上玻璃片;
③ ,控制活塞C,逐渐滴加双氧水,收集O 2并验满。
(1)写出仪器A的名称: ;
(2)步骤①中,检查装置气密性的方法是: ;
(3)步骤②中,塞进双孔橡皮塞的方法是: ;
(4)步骤③中,验满的方法是: ;
(5)若用图2装置收集O 2,则O 2由 端通入(填"a"或"b");
(6)下列关于本实验的叙述中,错误的是 :
A.为了快速获得O 2,双氧水的浓度越大越好
B.在橡皮管上增加水夹,可控制反应的开始与停止
C.在装置Ⅰ,Ⅱ间增加装有生石灰的U形管,可制得干燥O 2;
实验Ⅱ:铁丝在O 2中燃烧、
(1)该反应的化学方程式为: ;
(2)该反应的现象为:放热、火星四溅,生成 色固体;
(3)实验表明:改用加热KMnO 4制取、并用向上排空气法收集O 2进行本实验,成功率更高,原因可能是 。

认识常用仪器,学习一些实验的基本操作,才能正确、安全地进行实验,回答下列问题.
(1)用作配置溶液和较大量试剂的反应容器是 .
(2)把玻璃管插入橡胶塞的孔里,应先将玻璃管口 .
(3)细铁丝在氧气中燃烧,实验结束后发现集气瓶底部炸裂,原因是 .
学校新建了塑胶跑道,校园美观了,但空气中总是弥漫着一股难闻的气味.
(1)写出初中化学所涉及到的常用来吸附异味的物质名称.(答一种即可)
(2)空气中弥漫着难闻的气味,体现了分子的什么性质?
(3)合成橡胶除了制作橡胶跑道外还广泛应用于农业、国防、交通及日常生活中,合成橡胶与天然橡胶相比,合成橡胶有哪些优良的性能?(答一点即可)
化学与生活密切相关,请回答下列问题:
(1)打开汽水瓶盖时,汽水为什么会自动喷出来?
(2)在书写具有保存价值的档案时,规定应使用碳素墨水,为什么?
(3)随意丢弃塑料制品会造成"白色污染",请你谈一点减少"白色污染"的措施.
化石能源的大量消耗使环境问题愈加严重,请回答一下问题:
(1)煤燃烧产生的二氧化硫等气体会形成酸雨,酸雨有什么危害?(答一点即可)
(2)请为减缓温室效应提一条合理化建议.
(3)写出一种你知道的新能源.
在汽油中加入适量的乙醇(C2H5OH)作为汽车燃料(车用乙醇汽油),可适当节省石油资源,并在一定程度上减少汽车尾气的污染。请回答下列问题:
(1)乙醇完全燃烧的化学方程式为 。
(2)二氧化碳和水在一定条件下可发生反应,若反应属于化合反应,则在反应后的溶液中滴加紫色石蕊溶液,溶液呈 色:若反应生成了葡萄糖,则反应条件为 。
(3)C2H5OH在物质的分类上属于 。
A.化合物 B.氧化物 C.碱 D.有机物
(4)甲醇(CH3OH)与乙醇 (填“属于”或“不属于”)同一种物质。
请用所学的知识回答下列问题:
(1)量取液体时,如果视线没有与量筒内无色液体凹液面的最低处保持水平,而是采用俯视的方法,将会对读数产生什么影响?
(2)为什么菜刀、镰刀、锤子等用铁制而不是铝制?
试题篮
()