如图是甲、乙两种固体物质的溶解度曲线。下列说法不正确的是( )

A.甲物质的溶解度比乙物质的溶解度大
B.10℃时,甲物质和乙物质的溶解度相等
C.20℃时,100g水中最多能溶解40g甲物质
D.30℃时,甲物质的饱和溶液降温至10℃,有晶体析出
如图为A、B、C三种固体物质的溶解度曲线,请回答下列问题。
(1)20℃时,三种物质的溶解度大小关系为
(2)50℃时,150g A的饱和溶液中,含A g
(3)将C的饱和溶液变为不饱和溶液可采用的一种方法是
(4)50℃时,将A、B、C三种物质的饱和溶液分别降温到20℃,溶质的质量分数变化最大的是 。

甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)温度为 ℃时,甲、乙、丙种物质的溶解度大小关系为甲=乙>丙.
(2)t3℃时等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最大的是 .
(3)降温结晶过程中甲、乙两物质的溶解度都 (选填“增大”、“减小”或“不变”).
(4)接近饱和的丙溶液,在保持溶质质量分数不变的情况下转变为饱和溶液,可采取的方法是 .
(5)将t3℃时等质量的甲、乙两物质的饱和溶液,同时降温到t1℃,析出甲的质量 乙 (选填“>”“<”或“=”).

如图是硝酸钾和氯化钾的溶解度曲线.
(1)两种物质中,溶解度受温度影响较小的是 .
(2)t 2℃时,硝酸钾的溶解度(填">"、"="、"<") 氯化钾.
(3)要使硝酸钾的饱和溶液变为不饱和溶液,除加水外的方法是 .
(4)t 1℃时,硝酸钾饱和溶液中溶质的质量分数是 .

如图为a、b、c三种固体物质的溶解度曲线,请回答:
(1)t2℃时b物质的溶解度是 g。
(2)a中混有少量b,要提纯a可采用采用的结晶方法是 。
(3)t3℃时各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是 。此时,将温度降至t1℃,所得溶液中溶质的质量分数不变的是 。

如图是甲、乙、丙三种物质在水中的溶解度曲线,请回答下列问题:
(1)甲、丙两种物质的饱和溶液在 ℃时溶质质量分数相等。
(2)甲中含有少量的乙时,提纯甲的常用方法是 。
(3)t 1℃时各取25g甲、乙、丙三种物质,分别加入到盛有100g水的三只烧杯中,充分溶解后不能形成饱和溶液的是 ,若将温度升至t 3℃时,甲溶液的溶质质量分数将 (填"变大"、"变小"或"不变")。
(4)t 3℃时将等质量的甲、乙、丙三种物质的饱和溶液降温至t 2℃时,所得溶液中溶剂的质量关系是 。

甲、乙、丙三种固体物质的溶解度曲线如图所示。
(1) ℃时,甲、乙两种物质的溶解度相等。
(2)甲中含有少量的乙,可采用 方法提纯甲。
(3)t 1℃时,要配制100g质量分数为10%的甲溶液,需要甲物质的质量为 g。
(4)t 2℃时,甲、乙、丙三种物质的饱和溶液降温到t 1℃,所得溶液中溶质的质量分数由大到小的顺序是 。
(5)t 1℃时,将15g甲物质加入到50g水中充分溶解后,所得溶液中溶质的质量分数为 。

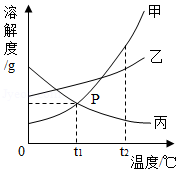
甲、乙、丙三种物质的溶解度曲线,如图所示,回答下列问题:
(1)P点的含义 ;
(2)t 2℃时,甲、乙、丙三种物质溶解度从大到小的顺序为 ;
(3)当乙中混有少量甲时,可采用 (填"降温结晶"或"蒸发结晶")的方法提纯乙。
(4)t 2℃时,将甲、乙、丙三种物质的饱和溶液同时降温t 1℃,所得溶液中溶质质量分数由大到小的顺序为 。
分析如图溶解度曲线,判断下列说法错误的是( )

| A. |
t 2℃时,硝酸钾的溶解度为110g |
| B. |
硝酸钾中含有少量氯化钠时,可以用冷却热饱和溶液的方法提纯硝酸钾 |
| C. |
将t 2℃时硝酸钾的饱和溶液降温到t 1℃,一定会析出(110﹣a)g晶体 |
| D. |
t 2℃时,等质量的两种物质的饱和溶液中,含硝酸钾的质量一定比含氯化钠的质量大 |
t1℃时,向盛有等体积水的①、②两支试管中分别加入等质量的甲、乙两种可溶性固体,充分溶解后,观察到如图1所示的现象。请回答:
(1)t1℃时, (选填“①”或“②”)试管中的溶液一定是饱和溶液;
(2)图2中表示乙的溶解度曲线的是 (选填“a”或“b”);
(3)下列说法正确的是 。
A、若甲中混有少量的乙,可以采用降温结晶的方法提纯甲。
B.t1℃时,试管①中溶液的溶质质量分数小于试管②中溶液的溶质质量分数
C、保持温度不变,向试管①中加入一定质量的水,溶液中溶质的质量分数一定变大

A、B两种固体物质的溶解度曲线如图所示,下列说法正确的是( )

| A. |
恒温蒸发溶剂的方法不可以使B得到饱和溶液析出晶体 |
| B. |
将t 2℃时A.B的饱和溶液分别降温至t 1℃,A成为不饱和溶液 |
| C. |
t 2℃时,用等质量的A.B分别配制成饱和溶液,所得溶液的质量A>B |
| D. |
t 2℃时,将150g A的饱和溶液稀释成质量分数为20%的溶液,需水100g |
a、b、c三种不含结晶水的物质的溶解度曲线如图,下列说法正确的是( )
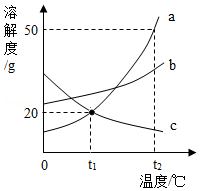
A.a的溶解度大于b的溶解度
B.将a的溶液由t2℃降温到t1℃,一定有晶体析出
C.t2℃时,50g的a溶于50g水,溶液的质量分数为50%
D.c的饱和溶液由t2℃降温到t1℃,溶液的质量分数不变
图1是a、b、c三种固体物质的溶解度曲线。请回答下列问题:
(1)在 ℃时,a、c两种物质的溶解度均为40克。
(2)在t 3℃时将40克a物质放入50克水中,充分搅拌后所得的溶液是 (填"饱和"或"不饱和")溶液,质量为 克。
(3)t 1℃时将等质量的a、b、c三种物质配制成饱和溶液,得到饱和溶液的质量由大到小的关系为 。
(4)如图2所示,试管中盛有稀硫酸,烧杯中盛有某物质的饱和溶液,往试管中加入适量镁条,过一会儿发现烧杯中的溶液变浑浊,则溶液中溶质的溶解度曲线与 (选填"a"、"b"或"c")物质的溶解度曲线最相似。

甲、乙两种物质的溶解度曲线如图所示。下列说法错误的是( )

A.80℃时,甲的饱和溶液中溶质与溶剂的质量比为4:5
B.用蒸发结晶的方法可从乙的饱和溶液中获得大量的乙
C.分别将60℃的甲、乙饱和溶液升温至80℃,此时甲溶液的溶质质量分数最大
D.60℃时,向140g甲饱和溶液中先加50g水,再加20g甲,充分溶解后,溶液仍为饱和状态
如图是两种固体的溶解度曲线。
(1)40℃时,氯化钠的溶解度 (填“>”、“=”或“<”)硝酸钾的溶解度。
(2)硝酸钾的溶解度随温度的升高而 。
(3)若将饱和的硝酸钾溶液从40℃降温到10℃, (填“有”或“无”)晶体析出。
(4)20℃时,某实验小组取不同质量的硝酸钾,分别加入到100g水中,充分溶解后,所得溶液的质量与加入硝酸钾的质量对应关系如表:
实验一 |
实验二 |
实验三 |
实验四 |
|
硝酸钾的质量/g |
20.0 |
25.0 |
30.0 |
35.0 |
所得溶液的质量/g |
120.0 |
125.0 |
130.0 |
131.6 |
根据上表数据,实验二所得的溶液为 (填“饱和”或“不饱和”)溶液;20℃时,硝酸钾的溶解度为 g。

试题篮
()