如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题:
(1)P点含义 ;
(2)t 2℃时,将15gA物质放入50g水中,充分溶解后,形成溶液的质量为 g;
(3)若A物质中含有少量的B物质,提纯A物质的方法是 (填"降温结晶"或"蒸发结晶");
(4)t 3℃时,将A、B、C三种物质的饱和溶液降温到t 1℃,三种溶液中溶质的质量分数由大到小的顺序为 。

如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)A点的含义是 。
(2)在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液是 溶液(填"饱和"或"不饱和")。
(3)若乙中混有少量甲,最好采用 的方法提纯乙(填"降温结晶"或"蒸发结晶")。
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是 。

如图是甲、乙两种固体物质的溶解度曲线图,请回答下列问题:
(1)20℃时,将15g的甲物质充分溶解在50g水中,所形成溶液的溶质质量分数是 .
(2)10℃时,欲将150g乙物质的饱和溶液质量分数减小一半,需要加水 g.
(3)某同学欲将20℃时300g20%的甲溶液溶质质量分数增大一倍.他采用恒温蒸发水的方法,并进行了如下计算:
解:设蒸发水的质量为x,
300g×20%=(300g﹣x)×40%
解得:x=150g
试分析:他能否达到目的,并说明理由.

甲和乙两种物质的溶解度曲线如图所示,回答下列问题:
(1)在t 1℃时,甲、乙溶解度大小关系为 ;
(2)若甲物质中含有少量的乙物质,可用 的方法提纯甲;
(3)在t 2℃时,将20g甲物质加入到50g水中,所得溶液是 (填"饱和"或"不饱和")溶液,溶液质量为 g.

如图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )

| A. |
通过升温可以将甲的不饱和溶液变为饱和溶液 |
| B. |
20℃时分别将甲、乙溶液蒸发相等质量的水,析出甲、乙的质量相等 |
| C. |
10℃时,10g水中分别溶解甲、乙达到饱和溶液,溶解较多的物质是乙 |
| D. |
把100g溶质质量分数为10%的乙溶液从30℃降温到10℃,其质量分数仍为10% |
结合水和溶液的相关知识,回答下列问题:
(1)对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是 。
(2)水是化学实验中常用的试剂,下列各组物质能用水鉴别的是 (填字母)。
A.氢氧化钠和硝酸铵 B.食盐和蔗糖 C.高锰酸钾和碘
(3)欲配制100g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是 。
①溶解 ②把配好的溶液装入细口瓶 ③称量 ④计算 ⑤量取
(4)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:
①P点的含义是 。
②在t 2℃时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是 克。
③将t 1℃时a、b、c三种物质的饱和溶液升温至t 2℃,所得溶液中溶质质量分数大小关系是 。
④a物质中含有少量c物质,可用 方法提纯a物质(填"降温结晶"或"蒸发结晶")。

如图所示的四个图象,能正确反映对应变化关系的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
某同学将甲乙固体各30克分别加入100克水中后,进行了如图1所示的实验。甲乙两种固体的溶解度曲线如图2所示。

请回答:
(1)10℃时,甲乙两种物质的溶解度大小关系:甲 乙(填"<"">"或"=")。
(2)m的取值范围 。
(3)40℃时,取等质量的甲乙两种物质的饱和溶液分别蒸发等量的水后,恢复到40℃.下列说法正确的是 (填字母)。
A.恢复到原温度后,溶液中溶剂的质量:甲=乙
B.恢复到原温度后,析出晶体的质量:乙>甲
C.若再降温到20℃时,溶液的质量:甲>乙
D.若再降温到20℃时,溶液的溶质质量分数:甲=乙
如图为a、b、c三种固体物质的溶解度曲线。
(1)t 1℃时,三种物质溶解度的大小顺序是 。
(2)t 2℃时,将等质量的b、c两物质加水溶解配制成饱和溶液,所得溶液的质量大小关系为m b m c(填">""<"或"=")
(3)t 2℃时,将55gb加入50g水中充分溶解,所得溶液的质量为 g
(4)把b物质的不饱和溶液变为饱和溶液,下列说法正确的是 。
A.溶剂的质量只能变小
B.溶质质量分数一定变大
C.溶质的质量可能变大
D.溶液的质量必然改变
E.该饱和溶液还可以溶解其他溶质

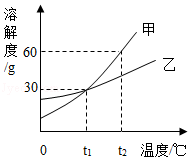
甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
| A. |
甲物质的溶解度大于乙物质的溶解度 |
| B. |
t 1℃时,将甲、乙两种物质各35g,分别加入到100g水中充分溶解,得到的溶液质量都是130g |
| C. |
将t 1℃时,甲的饱和溶液升温到t 2℃,溶质质量分数增大 |
D.t 2℃时,甲溶液的质量分数一定大于乙溶液的质量分数
氯化钠和硝酸钾两种固体物质的溶解度曲线如图所示。下列说法正确的是( )

| A. |
硝酸钾的溶解度大于氯化钠的溶解度 |
| B. |
常用冷却结晶的方法从氯化钠溶液中获得其晶体 |
| C. |
40℃时,将30g硝酸钾晶体放入50g水中,充分搅拌后,所得溶液的溶质质量分数为37.5% |
| D. |
将20℃的硝酸钾饱和溶液升温至60℃,溶液的溶质质量分数增大(忽略水分蒸发) |
在0℃时,配成甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体)。如图1所示,将烧杯的水持续升温,固体物质质量变化情况如图2所示。则下列说法正确的是( )

| A. |
甲溶液中溶质的质量分数随温度升高不断增大 |
B. |
t℃时,甲、乙两物质的溶解度一定相等 |
| C. |
经过升温可以将甲的饱和溶液变为不饱和溶液 |
D. |
乙物质的溶解度随温度的升高而增大 |
t 1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。下列说法正确的是( )

| A. |
烧杯①中的溶液一定未达到饱和状态 |
| B. |
烧杯②中溶解的溶质是氯化钾 |
| C. |
蒸发一定量的水,两烧杯中都一定有固体析出 |
| D. |
将温度升高到t 2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发) |
根据A、B、C三种固体物质的溶解度曲线图,回答下列问题:
(1)P点表示的意义为 。
(2)t3℃时,10g水中最多能溶解3.5g的B物质,则10g水最多溶解的A物质的量 3.5g(选填“>”“<”或“=”)。
(3)满足三种物质溶解度大小关系为 B>A>C的温度t的范围是 。
(4)将t3℃A、B、C的饱和溶液降温至t1℃,溶质质量分数不发生改变的是 的溶液。

水是一种重要的资源,请回答下列各题
(1)下列说法正确的是 (填序号)
A、硬水加入肥皂水容易起浮渣
B、生活中常用煮沸的方法降低水的硬度
C、蒸馏水、矿泉水、纯净水等都属于纯净物
D、自来水厂通过沉淀、过滤、吸附、消毒可将泉水变成纯水
(2)氢气燃烧是人们认识水的组成的开始,该反应的化学方程式为 。
(3)水常用于灭火,其灭火原理是 。
(4)在通电条件下,水和氯化钠发生化学反应生成氢氧化钠、氢气和氯气,写出此反应的化学方程式 。
(5)水是一种重要的溶剂,甲、乙两种物质在水中的溶解度曲线如图所示:
①温度 t 1℃时(填">"或"<"),甲物质的溶解度大于乙物质的溶解度。
②t 2℃时,用等质量的甲和乙分别配成饱和溶液所需要水的质量是甲 乙(填">""="或"<")
③甲、乙两种物质的饱和溶液温度由t 2℃降到t 1℃时,溶液组成不发生改变的是 (填甲或乙)
试题篮
()