下表中,有关量的变化图象与其对应叙述相符的是( )
| A. |
|
| B. |
|
| C. |
|
| D. |
|
如图是甲、乙两物质的溶解度曲线,下列说法不正确的是( )

| A. |
t 1℃时乙的溶解度大于甲的溶解度 |
B. |
t 2℃时甲、乙饱和溶液中溶质的质量分数相等 |
| C. |
升高温度能使饱和的甲溶液变为不饱和溶液 |
D. |
t 3℃时50g水中加入30g甲物质充分溶解后得到80g溶液 |
已知氯化钠、碳酸钠在不同温度时的溶解度如下:
| 温度/℃ |
0 |
10 |
20 |
30 |
40 |
|
| 溶解度/g |
氯化钠 |
35 |
35.5 |
36 |
36.5 |
37 |
| 碳酸钠 |
6 |
10 |
18 |
36.5 |
50 |
|
(1)依据上表数据,绘制出了氯化钠和碳酸钠的溶解度曲线(如图),图中能表示碳酸钠溶解度曲线的是 (填"A"或"B").
(2)图中两溶解度曲线相交于M点,此点表示的意义是 .
(3)40℃时,把50g A物质放入100g水中,充分搅拌,所得溶液是溶液 (填"饱和"或"不饱和").
(4)生活在盐湖(主要成分是NaCl和Na 2CO 3)附近的人们习惯"夏天晒盐(NaCl),冬天捞碱(Na 2CO 3)".请你答出"冬天捞碱"的道理 .

20℃时将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3,请结合图示回答下列问题。
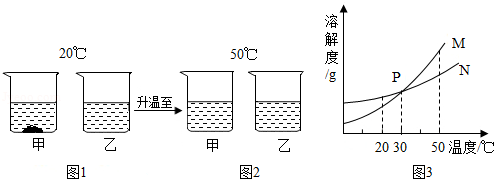
①图1中,一定为饱和溶液的是 。
②图2中,甲、乙两溶液中溶质质量分数为甲 乙( 填"大于""等于""小于")。
③图3中,表示乙的溶解度曲线的是 ,P点表示的含义是 。
A、B、C为三种物质的溶解度曲线,如图所示,请根据图示信息回答下列问题。
(1)t 1℃时,将5gB物质放入10g水中,充分溶解,温度不变,所得溶液的质量为 g。
(2)t 2℃时,A、C两种物质的饱和溶液中所含溶质的质量 (填"一定"或"不一定")相等。
(3)下列说法正确的是
A.t 2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t 1℃,析出的晶体中只有A
B.t 2℃时,将A、B、C的饱和溶液分别降温至t 1℃,所得溶液的溶质质量分数关系是B>A=C
C.若A物质中混有少量B物质,要对A物质进行提纯,可通过冷却热饱和溶液实现
D.用同一种方法能将A、B、C的不饱和溶液均变为饱和溶液。

A、B、C三种固体物质的溶解度曲线如图所示,回答下列问题。
(1)40℃时,溶解10gA物质,至少需要 g水。
(2)探究比较A和B在水中的溶解性,必须控制的相同条件是
A 水的质量 B 固体的颗粒大小 C 温度 D 搅拌速度
(3)配制同温下溶质质量分数相同的A、C饱和溶液,需要把温度控制在
(4)60℃时,A、B两种物质形成溶质质量分数相同的溶液,那么这两种溶液的溶质质量分数最大值为 (计算结果保留一位小数)。

甲物质的溶解度曲线图如图所示,下列说法中正确的是( )

| A. |
甲物质的溶解度随温度的升高而增大 |
B. |
甲物质的溶解度是102g |
| C. |
20℃时,50g水中加入15g甲物质充分溶解可得到65g溶液 |
D. |
70℃时,甲的饱和溶液升高温度或降低温度,都有晶体析出 |
A、B、C三种固体物质的溶解度曲线如图,请回答下列问题:
(1)随着温度升高,C的溶解度 (填"增大""减小"或"不变"),温度为 ℃时,A、B的溶解度相等。
(2)30℃时,将35gB放入100g水中,充分溶解后所得的溶液是 (填"饱和"或"不饱和")溶液。
(4)将30℃时A的饱和溶液升温到50℃,其溶质的质量分数 (填"增大""减小"或"不变")。
(4)50℃时,A、B、C三种物质的溶解度由大到小的顺序是 。
(5)若A的饱和溶液中含有物质C,提纯A的方法是 。

如图是甲、乙、丙三种物质的溶解度曲线,请回答下列问题:
(1)t 1℃时,三种物质中溶解度最大的是 .
(2)溶解度随温度升高而减小的是 .
(3)t 2℃,将质量相等的甲、乙、丙三种物质的饱和溶液降温至t 1℃,析出晶体最多的是 .
(4)t 2℃,将30g甲物质加入到50g水中充分搅拌,形成甲物质的 (填"饱和溶液"或"不饱和溶液")

某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是( )

| A. |
M的溶解度曲线为a曲线 |
B. |
升温可以使N的饱和溶液变浑浊 |
| C. |
M的饱和溶液从t 2℃降温到t 1℃时,溶质质量分数变大 |
D. |
如果t 2℃时,M.N的饱和溶液质量相等,则溶剂质量M>N |
t 2℃时,向盛有10mL水的A、B两试管中分别加入等质量的甲、乙两种可溶性固体,使其充分溶解后,观察到如图一所示的现象,请回答:
(1)t 2℃时, 试管中的溶液一定是饱和溶液.
(2)图二中表示乙物质溶解度曲线的是 .
(3)分别将等质量的甲、乙两种物质的饱和溶液从t 2℃降温到t 1℃,析出晶体较多的物质是 .

25℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3,请结合图示回答下列问题:

(1)图1中甲、乙溶液的溶质质量分数大小关系为
(2)图2中一定为饱和溶液的是 (填"甲"或"乙")
(3)图3中固体甲对应的溶解度曲线是 。
甲物质的溶解度(S)随温度(t)变化曲线如图所示,下列说法正确的是( )

| A. |
20℃时,甲易溶于水 |
B. |
60℃时,甲的溶解度约为0.6 |
| C. |
将80℃时甲的溶液降温至40℃,一定析出甲晶体 |
D. |
90℃时,在50g水中加入0.7g甲,充分搅拌后得到饱和溶液 |
如图是硝酸钾的溶解度曲线,回答下列问题:
(1)硝酸钾的溶解度随温度升高而 ;
(2)当温度为 ℃时,硝酸钾的溶解度为110g;
(3)图中点A所对应的是该温度下硝酸钾的 (填"饱和"或"不饱和")溶液。

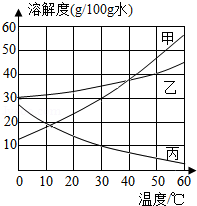
甲、乙、丙三种固体的溶解度曲线如图所示,据图回答:①30℃时,丙的溶解度是 ;②50℃时,在100g水中放入50g乙物质,充分搅拌后所得溶液的溶质质量分数为 。(计算结果保留至0.1%)。③若将20℃时甲、乙、丙三种物质的饱和溶液升温至40℃(不考虑水的蒸发),可析出晶体的是 。④将50℃时甲、乙、丙三种物质的饱和溶液均降温至10℃,所得溶液的溶质质量分数从大到小的顺序是 。
(2)常温下欲配置100g溶质质量分数为10%的乙溶液,操作如图所示。
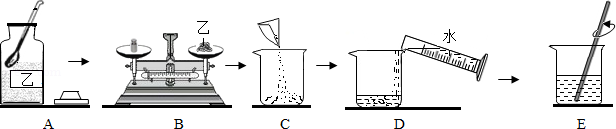
请回答下列问题:
①图中操作有错误的是 (填对应字母)。
②量取水时,若采用仰视的方法读数,会导致所配溶液的溶质质量分数 (填"偏大"、"偏小"或"无影响")
试题篮
()