下列说法中,正确的是
| A.乙醇分子中含有6个极性键 |
| B.乙烯分子中不含非极性键 |
| C.电子云表示电子在核外单位体积的空间出现的机会多少 |
| D.苯分子是单键和双键交替的结构 |
下列分子的键角均是109°28′的是
| A.P4 | B.CH2Cl2 | C.NH3 | D.CCl4 |
已知A、B、C、D是中学化学中常见的四种不同粒子,而且均是10电子的粒子,它们之间存在如图所示的转化关系: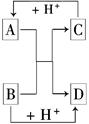
①A的电子式是
②加热条件下A与B在溶液中反应的离子方程式
③C中含有的化学键类型为:
④铝可以与B的某溶液反应,写出此反应的离子方程式
二氧化三碳(C3O2)是金星大气层的一个组成部分,下列关于二氧化三碳的说法错误的是
A.C3O2的电子式为: |
B.C3O2、CO、CO2都是碳的氧化物 |
| C.C3O2和CO一样可以燃烧生成CO2 | D.C3O2和CO2都是碳酸的酸酐 |
下列说 法中,不正确的是
法中,不正确的是
| A.双原子分子中的共价键,一定是非极性键 | B.非极性键也可能存在于离子化合物中 |
| C.分子间作用力,又叫范德华力,它比化学键要弱得多 | D.共价化合物在液态时不能导电 |
下列说法中正确的是
| A.共价化合物中一定只含有极性共价键 |
| B.只含有共价键的物质一定是共价化合物 |
| C.离子化合物中可能含有极性共价键或非极性共价键 |
| D.有较强共价键存在的物质熔沸点一定很高 |
(12分)(1)用电子式表示H2O和MgBr2的形成过程
H2O MgBr2
(2)写出CO2、Na2O2、H2O2的电子式:
CO2 Na2O2 H2O2
(3) H2O以 键结合,MgBr2以 键结合。NaOH以 键结合,Na2O2以 键结合(填极性键、非极性键、离子键)
(4) 、
、 、
、 、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①
、D、E 5种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:① ;②
;② 。
。 据此,回答下列问题:
据此,回答下列问题:
①写出①反应的离子方程式 。
② 和C-的电子式
和C-的电子式 ____________、C-____________。
____________、C-____________。
关于氢键,下列说法不正确的是
| A.每一个水分子内含有两个氢键 |
B.冰、水中 都存在氢键 都存在氢键 |
| C.水是一种非常稳定的化合物,这由于水分子之间形成氢键无关 |
| D.水的沸点很高,原因之一是水分子间存在氢键 |
下列说法中,不正确的是
| A.双原子分子中的共价键,一定是非极性键 |
| B.非极性键也可能存在于离子化合物中 |
| C.分子间作用力,又叫范德华力,它比化学键要弱得多 |
| D.大多数共价化合物在液态时不能导电 |
下列叙述中正确的是( )
| A.化学键只存在于分子之间 | B.化学键只存在于离子之间 |
| C.化学键是相邻的原子或离子间强烈的相互作用 | |
| D.化学键是相邻的分子之间强烈的相互作用 |
下列有关叙述正确的是( )
A.简单离子 An+核外有x个电子,A的质量数可表示为2(x+n) An+核外有x个电子,A的质量数可表示为2(x+n) |
| B.Z为元素的某同位素En-,核外共有x个电子,又知此同位素原子质量数为A,则其原子核内的中子数为A-x-n |
| C.A元素的原子质量数为70,核内中子数为39,它的离子有28个电子,A元素氧化物的化学式为AO |
| D.跟9 g水中所含中子数相同的D2O的质量为8 g |
试题篮
()