根据下面的反应路线及所给信息填空。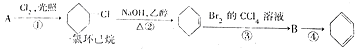
(1)有机物A的实验式是_______________________。
(2)反应①的方程式是_________________________,②的反应类型是___________。
(3)反应④的方程式是______________________________________。
用地壳中硅元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用。例如:
(1)光导纤维的主要成分是 ;
(2)目前应用最多的太阳能电池的光电转化材料是 ;
(3)用作吸附剂、干燥剂、催化剂或催化剂载体的人造分子筛大多是一类具有均匀微孔结构的被称为 (物质类别)的化合物。
(4)赏心悦目的雕花玻璃是用一种物质对玻璃进行化学刻蚀而制成的,该反应的化学方程式为 ;
(5)工业上制取粗硅是用石英和焦炭在高温电炉中反应制得,该反应中氧化剂与还原剂的质量比为 ;用石英和焦炭在高温电炉中反应也可以制得金刚砂(SiC),并产生CO气体,该反应中氧化剂和还原剂的物质的量之比为 。
下列实验的现象与对应结论均正确的是
| |
操作 |
现象 |
结论 |
| A |
将水蒸气通过灼热的铁粉 |
粉末变红 |
铁与水在高温下发生反应 |
| B |
常温下将表面用砂纸打磨过的Al片放入浓硝酸中 |
无明显变化 |
Al与浓硝酸不反应 |
| C |
将SO2气体通入硫酸酸化的高锰酸钾溶液中 |
溶液紫色褪去 |
SO2具有漂白性 |
| D |
将浓硫酸滴到蔗糖表面 |
固体变黑膨胀 |
浓硫酸有脱水性和强氧化性 |
水溶液中能大量共存的一组离子是
| A.Na+ 、Al3+ 、Cl- 、SO42- | B.H+ 、Na+ 、Fe2+ 、NO3- |
| C.K+ 、Cu2+ 、NO3- 、OH- | D.H+ 、NH4+、AlO2- 、SO42- |
下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
| |
实验 |
现象 |
结论 |
| A |
将氯气通入品红溶液 |
溶液红色褪去 |
氯气具有漂白性 |
| B |
将铜粉加入1.0mol·L-1 的Fe2(SO4)3溶液中 |
溶液变蓝,有黑色固体出现 |
金属Fe比Cu活泼 |
| C |
用坩埚钳夹住用砂纸仔细打磨过的铝箔在酒精灯上加热 |
熔化后的液态铝滴落下来 |
金属铝的熔点比较低 |
| D |
向盛有少量浓硝酸、稀硝酸的两支试管中分别加入一片大小相同的铜片 |
浓硝酸中铜片很快开始溶解,并放出红棕色气体;稀硝酸中过一会铜片表面才出现无色气体,气体遇空气变红棕色 |
浓硝酸氧化性强于稀硝酸 |
将2.8 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,设溶液体积不变,关于其结果说法正确的是
| A.铁粉与氯化铁恰好完全反应,Cl- 基本保持不变 |
| B.往溶液中滴入无色KSCN溶液,溶液变红色 |
| C.氧化产物和还原产物的物质的量之比为1: 2 |
| D.反应后溶液中Fe2+离子的浓度为 4 mol·L-1 |
下列关于气体的实验室制取方法,说法正确的是
| A.可用加热试管中的NH4Cl制取NH3 |
| B.可用MnO2固体和稀盐酸共热制取Cl2 |
| C.可用炽热的碳和浓硫酸反应制取SO2 |
| D.可用铝箔和NaOH溶液反应制取H2 |
下列叙述错误的是
| A.SO2使品红溶液褪色与Cl2使品红溶液褪色的原理不同 |
| B.利用焰色反应可以鉴别KCl和NaCl |
| C.利用澄清石灰水可以鉴别NaHCO3溶液和Na2CO3溶液 |
| D.用AgNO3溶液和稀硝酸可以鉴别KCl和K2CO3 |
某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂。用盐酸滴定待测液NaOH,滴定终点时的颜色变化是 ;若滴定前平视读数,滴定终点时俯视读数,则会使所测NaOH溶液的浓度值 (填“无影响”、“偏高”或“偏低”)。
试题篮
()