下列陈述Ⅰ、Ⅱ正确并且有因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
SiO2可与HF反应 |
氢氟酸不能保存在玻璃瓶中 |
| B |
Fe3+具有氧化性 |
用KSCN溶液可以鉴别Fe3+ |
| C |
溶解度:CaCO3<Ca(HCO3)2 |
溶解度:Na2CO3<NaHCO3 |
| D |
SO2有漂白性 |
将SO2通入紫色石蕊试液中溶液先变红后褪色 |
1.5mol N2、H2的混合气体和1.5mol NH3相比较,下列叙述中,一定正确的是
| A.体积相等 | B.原子数相等 | C.分子数相等 | D.质量相等 |
2.3g纯钠在干燥空气中被氧化后得到3.1g固体,由此可判断其产物是
| A.只有Na2O | B.只有Na2O2 | C.Na2O和Na2O2 | D.无法确定 |
下列关于胶体的说法中不正确的是
| A.可以通过过滤的方法将淀粉胶体中混有的氯化钠溶液除去 |
| B.分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| C.一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路 |
| D.制备Fe(OH)3胶体的方法是将饱和FeCl3溶液滴加到沸水中煮沸至溶液呈红褐色 |
有关分散系的下列说法不正确的是
| A.悬浊液的分散质可用过滤的方法从分散剂中分离出来 |
| B.分散质粒子直径为1-100纳米的分散系是胶体 |
| C.相同温度下同一种溶质的饱和溶液要比不饱和溶液的浓度大一些 |
| D.任何物质在水中溶解都有一定的溶解度 |
下列离子方程式错误的是
| A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO42-=BaS04↓+2H2O |
| B.酸性介质中KMnO4氧化H2O2:2MnO4- +5H2O2+6H+=2Mn2++5O2↑+ 8H2O |
| C.等物质的量的MgCl2、Ba(OH)2和HC1 溶液混合:Mg2++2OH-=Mg(OH)2↓ |
| D.铁铜原电池(稀硫酸做电解质)放电时的负极反应:Fe-2e-=Fe2+ |
下列说法不正确的是
| A.为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 |
| B.除去乙醇中的水:加入生石灰,蒸馏 |
| C.为除去乙炔气中少量的H2S,可使其通过CuSO4溶液 |
| D.为除去CO2中少量的SO2,可使其通过饱和Na2CO3溶液 |
下列每步转化不能通过一步反应就实现的是
| A.NH3→NO→NO2→HNO3 |
| B.Al→Al2O3→Al(OH)3→NaAlO2 |
| C.S→SO2→H2SO4→MgSO4 |
| D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
下列各组物质中,X是主体物质,Y是少量杂质, Z是为除去杂质所要加入的试剂,其中所加试剂正确的一组是
| 选项 |
A |
B |
C |
D |
| X |
FeCl2溶液 |
FeCl3溶液 |
Fe |
Na2SO4溶液 |
| Y |
FeCl3 |
CuCl2 |
Al |
Na2CO3 |
| Z |
Cl2 |
Fe |
NaOH溶液 |
BaCl2溶液 |
NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.含0.1 mol BaCl2的溶液中Cl-数为0.1NA |
| B.22 g CO2所含有的分子数为0.5NA |
| C.11.2 L CO2所含有的分子数为0.5NA |
| D.常温下NA个Cl2分子所占有的体积为22.4 L |
在除杂过程中要尽量除去杂质,那么,加入的试剂必须稍过量,且最后的过量物质可以使用物理或化学方法除去。现要除去NaCl中少量的CaCl2、Na2SO4杂质,下列选用试剂及其使用顺序正确的是
| A.Na2CO3、BaCl2、HCl |
| B.BaCl2、Na2CO3、H2SO4 |
| C.BaCl2、Na2CO3、HCl |
| D.Ba(NO3)2、Na2CO3、HCl |
为了将混有Na2SO4、NaHCO3的NaCl提纯,并制得纯净的溶液,某学生设计了如图所示的实验方案:
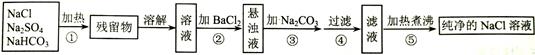
(1)操作①盛放药品可选用 (填仪器名称)。操作①中发生反应的化学方程式是: 。
(2)操作②为什么不用Ba(NO3)2溶液,其理由是 。
(3)进行操作②后,如何判断杂质已除尽?方法是 。
(4)操作③的目的是 ;为何不先过滤后加Na2CO3溶液,其理由是 。
(5)此设计方案是否严密?请说明理由 。
试题篮
()