镁铝合金5.1 g溶于300mL2mol/L的HCl,在标准状况下放出气体的体积为5.6L。向反应后的溶液中加入足量氨水,产生沉淀的质量为( )
| A.5.1g | B.10.2g | C.13.6g | D.15.3g |
某溶液中有Fe3+、Mg2+、Fe2+和Al3+四种阳离子,若向其中加入过量的氢氧化钠溶液,搅拌后,再加入过量的盐酸,溶液中大量减少的阳离子是( )
| A.Fe3+ | B.Mg2+ | C.Fe2+ | D.Al3+ |
大多数非金属元素有含氧酸根离子,某些金属元素也有含氧酸根离子:
MnO4-、MnO42-、Cr2O72-等。某无机盐M是一种优良的氧化剂,为确定其化学式,某小组设计并完成了如下实验:
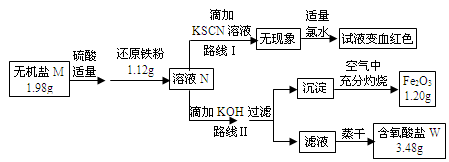
已知:
①无机盐M仅由钾离子和一种含氧酸根组成,其原子个数比为2:1:4
②如图中,将1.98g该无机盐溶于水,滴加适量稀硫酸后,再加入1.12g还原铁粉,整个过程无气体生成,恰好完全反应得混合溶液N.
③该小组同学将溶液N分为二等份,分别按路线Ⅰ、路线Ⅱ进行实验.
④在路线Ⅱ中,首先向溶液N中滴加适量KOH至元素X刚好沉淀完全,过滤后将沉淀在空气中充分灼烧得纯净的Fe2O3粉末1.20g;再将滤液在一定条件下蒸干,只得到3.48g纯净的不含结晶水的正盐W.
请按要求回答下列问题:
(1)由路线Ⅰ的现象可知,溶液N中含有的阳离子是 .
(2)由实验流程图可推得,含氧酸盐W的化学式是 ;由路线Ⅱ可知,1.98g无机盐M中所含钾元素的质量为 g.
(3)无机盐M与1.12g还原铁粉恰好完全反应生成溶液N的化学反应方程为 .
NO分子曾因污染空气而臭名昭著,但随着其“扩张血管、免疫、增强记忆”功能的发现,现在成为当前生命科学研究中的“明星分子”,回答下列问题:
(1)NO的危害在于 。
a.破坏臭氧层 b.参与酸雨和光化学烟雾的形成
c.与人体内血红蛋白结合 d.当它转化为N2后使空气中O2含量降低
(2)NH3与氧气反应可生成NO,化学方程式为 ;若参加反应的NH3为6 mol,则反应中转移了__________mol电子。
(3)一定条件下NO可转化为N2O和另一种红棕色气体,化学方程式为 。
(4)将0.05molNO和0.03molO2气体混合再以适当的速率缓慢通入盛有100mL水的集气瓶中,最终所得溶液中溶质的物质的量浓度为(设溶液体积变化忽视不计) 。
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解.该反应的化学方程式为: .
(2)在一定体积的10mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol.则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180mL.若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 .
(3)镁铁混合物4.9g,溶解在过量的某浓度的稀硝酸中,完全反应后得到标准状况下2.24L NO 气体.若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是 .
FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
I.实验需要90mL 0.10mol·L-1FeBr2溶液
(1)配制FeBr2溶液除烧杯、量筒、胶头滴管外还需的玻璃仪器是________。
(2)下列有关配制过程中说法错误的是________(填序号)。
a.用托盘天平称量质量为1.944g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II.探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
(3)请你完成下表,验证假设
| 实验步骤、预期现象 |
结论 |
| ①向溶液中加入四氯化碳,操作 现象 |
假设1正确 |
| ②向溶液中另入 现象 |
假设2正确 |
若假设1正确,从实验①分离出Br2的实验操作名称是
(4)若在50mL上述FeBr2溶液通入标准状况下112mL Cl2,反应的离子方程式为
某溶液中含有NH4+、SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断不正确的是:
| A.溶液中共发生了1个氧化还原反应 |
| B.反应前后,溶液中离子浓度基本保持不变的有NH4+、Na+ |
| C.有胶状物质生成 |
| D.溶液颜色发生变化 |
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中反应制得:①3SiO2+6C+2N2 Si3N4+6CO,也可由SiCl4的蒸汽和NH3反应制取:
Si3N4+6CO,也可由SiCl4的蒸汽和NH3反应制取:
②3SiCl4+4NH3 Si3N4+12HCl.则下列叙述正确的是
Si3N4+12HCl.则下列叙述正确的是
| A.反应②属于离子反应 |
| B.若制取等量的Si3N4,则反应①②转移电子数目必然相等 |
| C.反应①的氧化剂是N2 |
| D.反应①中氧化产物与还原产物物质的量之比为1:6 |
已知适当条件下+7、+6、+4价锰的化合物都能和浓盐酸反应制得氯气且还原产物都是MnCl2.将6.32g KMnO4粉末加热一段时间后收集到0.112L气体(标准状况,后同),冷却后放入足量的浓盐酸再加热,又收集到VL黄绿色气体,下列说法正确的是
| A.V=2.24L |
| B.参加反应的HCl为0. 18mol |
| C.无法确定最终生成含钾化合物的数量是多少 |
| D.6.32g KMnO4粉末若直接与足量浓盐酸反应可得到2.24L Cl2(标准状况) |
若NA为阿伏加德罗常数的值,下列说法正确的是
| A.NA个Fe(OH)3胶体粒子的质量为107g |
| B.8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA |
| C.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| D.5.6gFe与0.1mol Cl2完全反应,反应中转移的电子数为0.3NA |
胆矾(CuSO4·5H2O)是铜的重要化合物,有着广泛的应用,如用来配制农药波尔多液。以下是CuSO4·5H2O的实验室制备流程图。
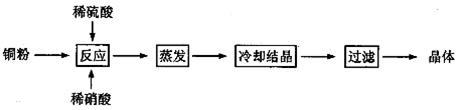
根据题意完成下列填空:
(1)向含有铜粉的稀硫酸中滴加硝酸,在铜粉溶解时最终可以观察到的实验现象: 、 。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是 (填化学式)。
(3)将CuSO4·5H2O与NaHCO3按一定的比例共同投入到150mL沸水中,剧烈搅拌,冷却后,有绿色晶体析出。该晶体的化学组成为Cux (OH) y (CO3) z·nH2O。实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是 。
(4)为了确定晶体的化学式,某实验小组进行如下实验:a.称取3.640g晶体,加入足量的稀盐酸使固体完全溶解,收集到标准状况下的气体448.0 mL;b.称取等质量的晶体,灼烧至完全分解,得到2.400g残余固体。通过计算确定晶体的化学式(写出计算过程)。
下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生白烟,A是强碱,D的焰色反应呈紫色(部分反应物和生成物及溶剂水已略去)。
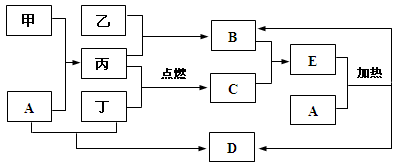
请回答下列问题:
(1)D的化学式为 。
(2)C的电子式为 。
(3)写出A溶液和甲反应的离子方程式: 。
(4)写出工业上制备B的化学方程式: 。
《有机化学基础》
(1)根据结构对有机物进行分类,有助于对其性质的掌握。
① 有机物苯属于 (填字母)。
a.芳香烃 b.烯烃 c.炔烃
② 下列有机物属于酚类的是 (填字母)。

③ 纤维素属于 (填字母)。
a.糖类 b.油脂 c.蛋白质
(2)柴胡红景天中的活性成分之一是鞣花酸(结构式如右图)。
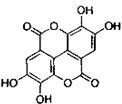
①鞣花酸的分子式为 ;
②鞣花酸分子中含氧官能团为 和 (写名称);
③1mol鞣花酸最多可与 mol Br2发生取代反应;
1mol鞣花酸最多可与含 mol NaOH的溶液发生反应.
(3)莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.

①区别两种酸的方法是 。
莽草酸与溴水的反应方程式: 。
②等物质的量的两种酸与足量NaOH溶液反应,消耗氢氧化钠物质的量之比是 。
③鞣酸的核磁共振氢谱图(H核磁共振谱图)上有 个吸收峰。
本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》
(1)改善环境质量已成为全球共识。保护环境,人人有责。
①空气质量报告的各项指标可以反映出该地区的空气质量状况,下列不需要监测的成分是 (填字母)。
A. SO2 B. N2 C. 可吸入颗粒物
②pH< 的雨水称为酸雨,煤炭燃烧产生的SO2所形成的酸雨,其最终的主要成分是 (填化学式)。
③煤中加入石灰石可以大大减少SO2的排放,发生反应的化学方程式: 。
(2)保持营养均衡,合理使用药物是人类健康的重要保证。
①人体内提供能量的主要营养物质为 、糖类和蛋白质,人体内蛋白质在蛋白酶作用下水解的最终产物是 。
②维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和 试剂共同完成。
③咽喉发炎的病人可以使用药物 (填“氢氧化铝”或“青霉素”),起到杀菌消炎作用。
④阿司匹林(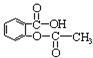 )在人体内可以水解为水杨酸(
)在人体内可以水解为水杨酸( 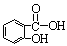 )和一种生活中常见的酸味剂,具有解热镇痛疗效,写出其水解的化学方程式: 。
)和一种生活中常见的酸味剂,具有解热镇痛疗效,写出其水解的化学方程式: 。
(3)(4分)材料是人类生活的物质基础,新型材料的制造则是科技快速发展的重要标志。
①钢铁是制造铁路、桥梁、轮船等的主要材料,钢铁在潮湿的空气中主要发生 腐蚀(填“吸氧”或“析氢”),腐蚀时Fe作为原电池的 极。
②目前,很多地方使用的泡沫塑料快餐具的主要成分是聚苯乙烯(简称EPS),聚苯乙烯属于 (填字母)。
A. 无机非金属材料 B. 金属材料 C. 有机高分子材料
③工业上生产玻璃、水泥都要用到的原料是 。
试题篮
()