X、Y、Z三种元素,原子序数依次减小。X是第四周期主族元素,其部分电离能如图所示;X、Y元素具有相同的最高正化合价;Z原子价电子排布式nsnnpn。回答下列问题:
(1)X原子的电子排布式为 。
(2)电负性:X Y(填“>”、“=”或“<”)。
(3)元素Z的一种氢化物(化学式为Z2H4)是重要的化工原料。 有关Z2H4分子的说法正确的是 (填字母)。
A.分子中含有氢键
B.属于非极性分子
C.含有4个σ键和1个π键
D.Z原子的杂化方式为sp2
(4)X的氧化物与钛(Ti)的氧化物相互作用,能形成钛酸盐,其晶体结构如图所示(X、Ti和O三种元素对应的离子分别位于立方体的体心、顶点和面心)。该晶体中,钛离子和周围 (填数字)个氧离子相紧邻。
(5)NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是 (填字母)。
A.离子键 B.非极性键 C.配位键 D.金属键
现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各离子不重复):
阳离子:H+、Na+、Al3+、Ag+、Ba2+ 阴离子:OH-、Cl-、CO32-、NO3-、SO42-
已知:①A、B两溶液呈碱性,C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
请回答下列问题:
(1)写出A与D的化学式: A______________,D_______________。
(2)写出A与E溶液反应的离子方程式:____________________________________。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1)△H=-akJ·mol-1.请写出表示相同条件下B与C的稀溶液反应的中和热的热化学方程式:________________。
(4)若25℃时,C、E及醋酸三种溶液的pH=4,则E和C溶液中由水电离出的c(H+)的比是_______________;将C与醋酸混合,醋酸的电离程度将____________(填“增大”“不变”或“减小”)(水的浓度视为常数).
(5)用惰性电极电解0.1mol·L-1 D与0.1mol·L-1C各100mL混合后的溶液,电解一段时间后,阴极质量_________(填“增大”“不变”或“减小”,下同);溶液的pH____________.
(6)向(5)中所得溶液中加入足量铁粉,则所能溶解的铁粉质量为___________g。
已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素。其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外最外层电子数与B相同,其余各层均充满。B、E两元素组成化合物B2E的晶体为离子晶体。C、F的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q。
(1)B的单质晶体为体心立方堆积模型,其配位数为 ;E元素的最高价氧化物分子的立体构型是 。F元素原子的核外电子排布式是 ,F的高价离子与A的简单氢化物形成的配离子的化学式为 .
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由 。
(3)A、G形成某种化合物的晶胞结构如图所示 。若阿伏伽德罗常数为NA,该化合物晶体的密度为 a g/cm3,其晶胞的边长为 cm。
。若阿伏伽德罗常数为NA,该化合物晶体的密度为 a g/cm3,其晶胞的边长为 cm。
(4)在1.0l×105 Pa、t1℃时,气体摩尔体积为53.4 L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的组成为(写化学式) 。
A、B、C、D、E为原子序数依次增大的短周期元素。A、C处于同一主族,C、D、E处于同一周期,E原子的最外层电子数是A、B、C原子最外层电子数之和,D是地壳中含量最高的金属元素;A、B组成的常见气体甲能使湿润的红色石蕊试纸变蓝;E的单质与甲反应能生成B的单质,同时生成两种水溶液均呈酸性的化合物乙和丙(该反应中氧化产物只有一种),25℃时0.1 mol/L的乙溶液pH>l;D的单质既能与C元素最高价氧化物的水化物的溶液反应生成盐丁,也能与丙的水溶液反应生成盐。
请回答下列问题:
(1)甲的化学式为 ;B单质的电子式为 。
(2)D元素的名称是 。
(3)写出丁溶液中通入过量二氧化碳时的离子方程式
(4)工业上利用A、B的单质合成甲(BA3):B2 (g)+3A2 (g)  2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
2BA3 (g) △H<0,在一定温度下,在2 L密闭容器中,2 mol单质B2和1.6mol单质A2充分反应后达到平衡,测得BA3的物质的量浓度为0.4 mol/L,计算该温度下的平衡常数K=______________。
(5)E的单质与甲反应生成的乙和丙的物质的量之比为2:4.反应中被氧化的物质与被还原的物质的物质的量之比为 。
X、Y、Z、W、L、M六种短周期主族元素的原子序数依次增大,其中X、M的单质在常温下呈气态,Y的原子最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大, W是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。用化学用语回答下列问题:
(1)L的元素符号为 ;M在元素周期表中的位置为 。
(2)Y、L、M的最高价含氧酸的酸性由弱到强的顺序是 。
(3)Y的最高价氧化物的电子式为 。原子序数比Y多2的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
(4)Z、W各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(5)R与Y同周期,R的单质分子R2中有3个共价键,R与L能形成一种新型无机非金属材料,其化学式是 。
下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 二 |
|
|
|
|
① |
|
② |
|
| 三 |
③ |
④ |
⑤ |
⑥ |
|
|
⑦ |
⑧ |
| 四 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)在这些元素中,化学性质最活泼的非金属原子的原子结构示意图为 。
(2)地壳中含量最多的金属元素是 (写元素符号) 。
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。
(4)写出⑤与氢氧化钠反应的化学方程式: ,
写出⑤的氢氧化物与氢氧化钠溶液完全反应的离子方程式:
A、B、C、D、E、F、G、H和I是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:① A、B 、E、F、G能使湿润的蓝色石蕊试纸变红,I能使湿润的红色石蕊试纸变蓝,C、D、H不能使石蕊试纸变色;② A和I相遇产生白色烟雾;③ B和E都能使品红溶液褪色;④ 将红热的铜丝放入装有B的瓶中,瓶内充满棕黄色的烟;⑤ 将点燃的镁条放入装有F的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;⑥ C和D相遇生成红棕色气体;⑦ G在D中燃烧可以产生E和H2O;⑧ 将B和H在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生A。回答:
(1)A的化学式是 ,②中烟雾的化学式是 ;
(2)④中发生反应的化学方程式是 ;
(3)⑤中发生反应的化学方程式是 ;
(4)C的化学式是 ,D的化学式是 ;
(5)⑦中发生反应的化学方程式是 ;
位于短周期的四种元素a、b、c、d、e,原子序数依次增大,已知a的单质最轻,d是地壳中含量最多的金属元素,a和d的原子序数之和等于b的原子序数的两倍,e的质子数是c的两倍且同主族。据此回答下列问题
(1)d元素在周期表中的位置 。
(2)有a和b元素组成的四核10电子分子的电子式 。实验室制取该种物质的化学方程式为 。
(3)写出由a和c两种元素形成的18电子的物质的结构式 ,往一定量的氯化亚铁溶液中滴加适量该物质溶液,发生反应的离子方程式为 。
(4)由d和e两种元素组成的化合物投入水中所观察到的现象 ,该过程的化学反应方程式为 。
下表为元素周期表前三周期的一部分。
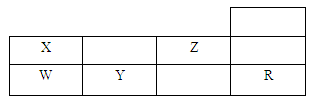
(1)X的氢化物与W的氢化物的比较稳定的是: (填化学式)。(2)从下列选项中选出X的基态原子的最外层原子轨道表示式 ,另一原子轨道表示式不能作为基态原子的轨道表示式是因为它不符合 。(填序号)。
A.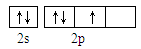 |
B.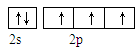 |
| C.泡利原理 | D.洪特规则 |
(3)以上五种元素中, 元素的电负性最大(填元素符号)。
A、B、C、D四种短周期元素,原子序数依次增大;A和C能形成一种分子X或一种+1价阳离子Y;B元素的原子最外层电子数是次外层电子数的2倍;C、D在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体。回答下列问题:
(1) B在周期表中的位置为 。
(2) 写出一种由A、B、C、D四种元素组成的常见化合物的化学式 ,其中所含的化学键类型为 。
(3) 写出Y水解的离子方程式 。
(4) 在101 kPa时,lgX气体在D单质中充分燃烧,生成一种液态化合物和另一种对环境无污的稳定物质,放出18.6 kJ的热量。该反应的热化学方程式为 。
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
所有元素中电负性最大的元素 |
| X |
L层p电子数比s电子数多2个 |
| Y |
其最高价氧化物呈两性 |
| Z |
L层有三个未成对电子 |
(1)写出元素X电子排布式 。
(2)Z原子共有 种运动状态不同的电子。
(3)写出Z元素形成的单质的结构式: 。
(4)元素T与氯元素相比,非金属性较强的是 (用元素符号表示),下列表述 中能证明这一事实的是
A、常温下氯气的颜色比T单质的颜色深
B、T的单质通入氯化钠水溶液不能置换出氯气
C、氯与T形成的化合物中氯元素呈正价态
(5)探寻物质的性质差异性是学习的重要方法之—。T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是 (填化学式),理由 。
(6)T与Z形成的化合物含有的化学键类型 。
A~H均为短周期元素,A~F在元素周期表中的相对位置如图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G组成的气态化合物甲水溶液呈碱性。
| A |
B |
C |
|
| D |
|
E |
F |
请回答下列问题:
(1)写出甲的电子式 ,实验室制取气体甲的化学方程式为 。
(2)B、C、G个数比为1:1:5形成的化合物的化学键类型为 。
A.离子键 B. 极性键 C. 非极性键
(3)请用电子式表示AE2的形成过程 。
(4)用离子符号表示C、E、F、H四种离子的半径由大到小的顺序 。
(5)用一个离子方程式解释A比D非金属性强的原因 。
下表为周期表的一部分,其中的编号代表对应的元素。
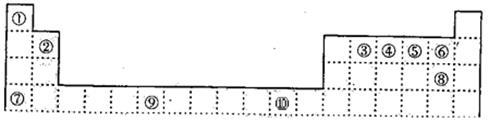
(1)⑨是 (填元素名称)。
(2)画出⑥的离子结构示意图 。
(3)元素⑦和⑧形成的化合物属于 晶体,它比NaF的熔点 (填“高”或“低”)。
(4)在 ①~⑩ 元素的最高价氧化物的水化物碱性最强的是 ,酸性最强的是 。(填化学式)
(5)⑧形成的最高价氧化物化学式是 。
(6)元素⑩在元素周期表的 族,其原子的外围电子排布式 。
(7)第四周期所有元素的基态原子中,4p轨道半充满的是 (请填元素符号,下同),4s轨道半充满的是 。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。
现有A、B、C、D、E五种原子序数依次增加的短周期元素,其中A的最低负价和最高正价代数和为零,且A2常温下为气态,B与其他元素形成的化合物种类最多,C与E可形成EC2和EC3两种物质,D是短周期最活泼的金属元素,用化学用语回答下列问题:
(1)D离子结构示意图_________________,B在元素周期表的位置_______________;
(2)A与C形成含18个电子的化合物的电子式是_______________;
(3)C与D形成的一种化合物颜色为淡黄色,其阴阳离子个数比为_____________,含有的化学键类型为___________;
(4)C、D、E的常见离子的离子半径由大到小的顺序__________________;
(5)B、E两元素得电子能力B________E(填“>”或“<”),试写出证明该结论的一个化学方程式_______;
(6)工业上常用氨水吸收尾气中的EC2,离子方程式为_______________________。
试题篮
()