下列叙述中,正确的是( )
①电解池是将化学能转变为电能的装置 ②原电池是将电能转变成化学能的装置 ③金属和石墨导电均为物理变化,电解质溶液导电是化学变化 ④不能自发进行的氧化还原反应,通过电解的原理有可能实现 ⑤电镀过程相当于金属的“迁移”,可视为物理变化
| A.①②③④ | B.③④ | C.③④⑤ | D.④ |
在北京奥运会期间,氢燃料电池公交汽车已经驶上北京街头,体现“科技奥运,绿色奥运”。下列说法正确的
| A.电解水制取氢气是理想而经济的制氢方法 |
| B.发展氢燃料电池汽车不需要安全高效的储氢技术 |
| C.氢燃料电池把氢气和氧气燃烧放出的热能转化为电能 |
| D.氢燃料电池汽车的使用可以有效减少城市空气污染 |
以煤为主要原料可以制备乙二醇,相关工艺流程下:

(1)写出方法l在催化剂的条件下直接制取乙二醇的化学方程式____________________
(2)合成气在不同催化剂作用下,可以合成不同的物质。下列物质仅用合成气为原料就能得到且原子利用率为100%的是 ____(填字母)。
A.草酸( HOOC-COOH) B.甲醇(CH3OH) C.尿素[CO(NH2)2]
(3)工业上还可以利用天然气(主要成分为CH4。)与C02反应制备合成气。已知:
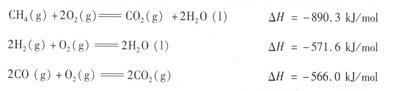
则CH4与CO2生成合成气的热化学方程式为
(4)方法2:在恒容密闭容器中投入草酸二甲酯和H2发生如下反应:
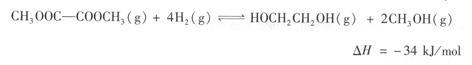
为提高乙二醇的产量和速率,宜采用的措施是___________(填字母)。
A.升高温度 B.增大压强 C.增大氢气浓度
(5)草酸二甲酯水解生成草酸:

①草酸是二元弱酸,可以制备 (草酸氢钾),
(草酸氢钾), 溶液呈酸性,用化学平衡原理解释: 。
溶液呈酸性,用化学平衡原理解释: 。
②在一定的 溶液中滴加NaOH溶液至中性。下列关系一定不正确的是 (填字母)。
溶液中滴加NaOH溶液至中性。下列关系一定不正确的是 (填字母)。
A.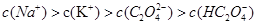
B.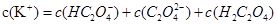
C.
(6)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的 (填“正”或“负”)级,负极反应式为 。
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e-+ OH- =" NiOOH" + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
某课外活动小组用如图装置进行实验,试回答下列问题。

(1)若开始时开关K与a连接,则B极的电极反应式为 。
(2)若开始时开关K与b连接,则B极的电极反应式为 ,
总反应的离子方程式为 。
有关上述(2)实验,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。

①该电解槽的阳极反应式为 。
此时通过阴离子交换膜的离子数 (填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
②若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 。
某酒精检测仪是以酸性燃料电池原理设计的,负极上的反应为:CH3CH2OH-4e-+ H2O=CH3COOH + 4H+。下列有关说法不正确的是
| A.检测时,电解质溶液中的H+向正极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗2.24L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH + O2 = CH3COOH + H2O |
| D.正极上发生的反应为:O2 + 4e-+ 2H2O = 4OH- |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-==Cl2↑ |
| B.氢氧燃料电池的负极反应式:O2+2H2O+4e-==4OH- |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-==Cu2+ |
| D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-==Fe2+ |
关于下列装置说法正确的是
| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.用装置②精炼粗铜,电解液浓度保持不变 |
| C.可以用装置②在铜上镀银,c极为银 |
| D.装置③中一段时间后会有Fe(OH)2生成 |
在 500 g CuSO 4 溶液中插入两根电极,一极为铜,一极为粗铜(含锌)。通电电解至粗铜刚好全部溶解掉,这时铜极质量增加 7.04 g ,电解质溶液质量增加 0.02 g 。求粗铜中含锌的质量分数。
高铁电池是一种可逆电池,该电池能长时间保持稳定的放电电压。高铁电池总反应为3Zn+2K2FeO4+8H20 3Zn(OH)2+2Fe(OH)3+4KOH。下列判断不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列判断不正确的是
| A.放电时,负极反应为Zn-2e-+2OH一=Zn(OH)2 |
| B.充电时,阴极pH增大 |
| C.放电时,若有6mol电子转移,则正极有10 mol OH一移向负极 |
| D.充电时,阳极反应为Fe(OH)3+5OH一+3e一=FeO42-+4H2O |
下列叙述不正确的是
| A.太阳能蓄电池只是将太阳能直接转化为电能的装置 |
| B.燃料电池是将化学能直接转化为电能的装置,所以能量利用率高 |
| C.碱性Zn-Mn干电池比酸性Zn-Mn干电池耐用,且不易漏液 |
| D.手机上用的锂离子电池属于二次电池 |
如右图所示,以稀土金属材料作惰性电极,在两极上分别通入甲烷与空气,电解质为掺杂了Y2O3的 ZrO3固体,它在高温下能传导O2‑。下列说法正确的是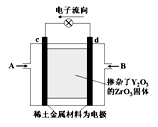
| A.c电极名称为负极,气体A为空气 |
| B.d电极上发生反应:CH4-8e-+4O2-=CO2+2H2O |
| C.O2‑向c电极移动 |
| D.用此装置作电源电解精炼铜,d电极与粗铜相连 |
铅蓄电池的电池反应为 Pb(s)+PbO2(s)+2H2SO4(aq) 2PbSO4(s)+2H2O(l),下列说法错误的是
2PbSO4(s)+2H2O(l),下列说法错误的是
| A.放电时电解质溶液的H+浓度逐渐减小 |
| B.利用铅蓄电池电解饱和食盐水制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少0.10 mol |
| C.充电时阴极的电极反应为 PbSO4(s) + 2e-="Pb(s)" + SO42-(aq) |
| D.放电时负极材料质量减小 |
如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
| A.质子透过离子交换膜由右向左移动 |
| B.铜电极应与X相连接 |
| C.M电极反应式:(C6H10O5)n + 7nH2O-24ne-= 6nCO2↑+ 24nH+ |
| D.当N电极消耗0.25 mol气体时,则铁电极增重16 g |
试题篮
()