随着各地“限牌”政策的推出,电动汽车成为汽车届的“新宠”。特斯拉全电动汽车使用的是钴酸锂(LiCoO2)电池,其工作原理如右图,A 极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过,电池反应式LixC6+Li1-xCoO2 C6+LiCoO2。下列说法不正确的是
C6+LiCoO2。下列说法不正确的是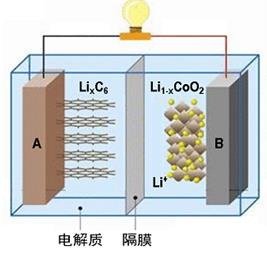
| A.据题意分析可知该隔膜只允许Li+通过,放电时Li+从左边流向右边 |
| B.放电时,正极锂的化合价未发生改变 |
| C.充电时B作阳极,该电极放电时的电极反应式为:Li1-x CoO2+ xLi++ xe-= LiCoO2 |
| D.废旧钴酸锂(LiCoO2)电池进行“放电处理”让Li+进入石墨中而有利于回收 |
一种直接肼燃料电池的结构如图所示,下列说法正确的是
| A.a极为电池的正极 |
| B.电路中每转移6.02×1023个电子,则有1molNa+穿过膜向正极移动 |
| C.b极的电极反应式为H2O2+2e-=2OH- |
| D.用该电池电解饱和食盐水,当阳极生成2.24L(标准状况)Cl2时,消耗肼0.1mol |
近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法正确的是
| A.碳极发生的反应是:2H2O+O2+4e-=4OH- |
| B.有机电解质通过固体电解质可进入水溶液中 |
| C.理论上外电路中每转移1mol电子,负极消耗的质量为7g |
| D.该电池如可以充电,充电时碳极接外加电源的负极,锂极接外加电池的正极 |
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为Cl2+2e-=2Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.01 mol离子 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为。
下列有关说法正确的是
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
C.电池反应的化学方程式为: |
D.正极上发生的反应是: |
新型NaBH4—H2O2燃料电池(DBFC)的结构如图所示(已知.NaBH4中氢为-1价),有关该电池的说法不正确的是
A.放电过程中.Na+从A极区向B极区迁移
B.电极B材料中含MnO2层,MnO2起导电作用
C.在电池反应中,每消耗1 L 6 mol/LH2O2溶液,理论上流过电路中的电子为12 NA
D.电池负极区的电极反应为BH4—+8OH——8e—=BO2—+6H2O
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O Cd(OH)2 +2Ni(OH)2
Cd(OH)2 +2Ni(OH)2
有关该电池的说法正确的是
| A.充电时阳极反应:Ni(OH)2-e— + OH- ="=" NiOOH + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH- 向正极移动 |
美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 =2CO2 +3H2O,电池示意如图,下列说法正确的是
| A.a极为电池的负极,乙醇被还原 |
| B.电池工作时电子由b极沿导线经灯泡再到a极 |
| C.电池正极的电极反应为:2H+ + O2 + 4e-= H2O |
| D.电池工作时1mol乙醇被氧化时,就有12mol质子 |
汽车的启动电源常用铅蓄电池,该电池在放电时的反应如下:Pb (s)+ PbO2(s) +2H2SO4(aq) 2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是
2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb(s)+SO42-(aq)–2e – = PbSO4(s) |
| C.铅蓄电池属于一次电池 |
| D.电池放电时,溶液酸性增强 |
科学家制造出一种使用固体电解质的燃料电池,其效率更高。一个电极通入空气,另一电极通入汽油蒸汽,其中电池的电解质是掺杂了Y2O3(Y为钇)的ZrO2 (Zr为为锆)晶体,它在高温下能传导O2—离子。若以丁烷(C4H10)代表汽油,总反应为2 C4H10+13O2=8CO2+10H2O。有关该电池说法错误的是
| A.该电池负极的电极反应式为:2C4H10+26O2—-52e— = 8CO2+10H2O |
| B.该电池正极的电极反应式为:O2+ 4e—+ 2H2O= 4OH— |
| C.O2—向负极移动 |
| D.丁烷在放电时发生氧化反应 |
一种由甲醇和氧气以及强碱作为电解质溶液的新型手机电池,其电池反应为:
2CH3OH + 3O2 + 4OH- 2 CO32— + 6H2O,则下列说法错误的是
2 CO32— + 6H2O,则下列说法错误的是
| A.充电时电解质溶液的pH逐渐增大 |
| B.放电时CH3OH参与反应的电极为正极 |
| C.充电时每生成1 mol CH3OH转移6 mol电子 |
| D.放电时负极的电极反应为:CH3OH-6e- +8OH- =CO32—+ 6H2O |
下图所示是一种新近开发的一种固态燃料电池。它以熔融的碳酸盐为电解质,以甲烷为燃料,a、b均为惰性电极。关于该电池的下列说法中正确的是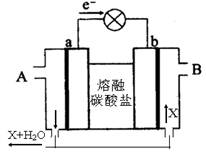
| A.A处通入空气,B处通入甲烷 |
| B.a极电极反应式:CH4+10OH--8e-=CO32-+7H2O |
| C.如用这种电池电镀铜,当镀件增重12.8g时,消耗标准状况下的空气2.24L |
| D.电池工作时电解质组成应保持稳定,因此必须有部分X物质参加循环,则X是二氧化碳 |
某甲烷燃料电池构造示意图如下,关于该电池的说法不正确的是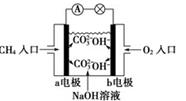
| A.a极是负极,发生氧化反应 |
| B.正极的电极反应是:O2+2H2O+4e-=4OH- |
| C.该甲烷燃料电池的总反应:CH4+2O2=CO2+2H2O |
| D.甲烷燃料电池是环保电池 |
如将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2即构成甲烷燃料电池。已知通入甲烷的一极,其电极反应为CH4 + 10OH--8e-="==" CO32-+ 7H2O 下列叙述正确的是
| A.通入甲烷的一极为正极 |
| B.通入氧气的一极发生氧化反应 |
| C.该电池总反应为CH4 +2 O2 + 2OH-="==" CO32-+ 3H2O |
| D.该电池在工作时,溶液中的阴离子向正极移动 |
试题篮
()