以葡萄糖(C6H12O6)为燃料的微生物燃料电池结构如图所示。认真观察分析图示信息,判断下列叙述正确的是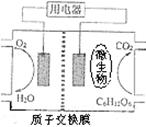
| A.该电池能够在高温下工作 |
| B.电池的正极反应为:O2 + 4e- + 4H+= 2H2O |
| C.放电过程中,H+从正极区向负极区迁移 |
D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体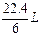 |
某种燃料电池是以甲烷(CH4)和空气为原料,以KOH为电解质溶液构成的原电池。电池的总反应类似甲烷在氧气中的燃烧。下列说法正确的是
①每消耗1molCH4可以向外电路提供8mole-
②CH4在负极发生氧化反应,电极反应式是:CH4 + 10OH- - 8e- = CO32- + 7H2O
③燃料电池把化学能直接转化为电能,而不经过热能这一种中间形式,所以它的能量转化效率高,并且减少了对环境的污染
④这种燃料电池要定期更换电解质溶液
| A.①② | B.①②③④ | C.①③④ | D.②④ |
一种新燃料电池,一极通入空气,另一极通入丁烷(C4H10)气体,电池的总反应是:
2C4H10 + 13O2 → 8CO2 + 10H2O,电解质溶液是稀H2SO4溶液。下列对该燃料说法正确的是( )
| A.在电解质溶液中,SO42-由负极移向正极 |
| B.丁烷在反应过程中被还原 |
| C.通入空气的一极是正极,电极反应为:O2 + 4e- + 4H+ = 2H2O |
| D.通入丁烷的一极是负极,电极反应为:C4H10 + 26e- + 8H2O = 4CO2 + 26 H+ |
可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
| A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e-=4OH- |
| B.以NaOH溶液为电解液时,负极反应为:Al+3OH--3e-=Al(OH)3↓ |
| C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变 |
| D.电池工作时,电子通过外电路从正极流向负极 |
右图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是 ( )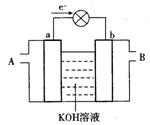
| A.A处通人的是空气,B处通人的是水煤气 |
| B.a电极发生还原反应,b电极发生氧化反应 |
C.a电极的反应式包括:CO+4OH-+2e-=CO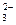 +2H2O +2H2O |
| D.如用这种电池电镀铜,待镀金属增重6.4 g,则至少消耗标准状况下的水煤气2.24 L |
某新型 “纸”电池以碳纳米管和金属锂作为两极,造纸用的纤维素在一种离子液体X中溶解并做成隔离膜,电池工作时的总反应为:xLi+C(碳纳米管) LixC,下列有关说法正确的是
LixC,下列有关说法正确的是
| A.放电时Li+由正极向负极移动 |
| B.充电时的阳极反应为:LixC-xe-=C+xLi+ |
| C.X可能为羧酸、醇等含活泼氢的有机物 |
| D.锂离子电池的比能量(单位质量释放的能量)低 |
镁—过氧化氢燃料电池具有比能量高、安全方便 等优点,
其结构示意图如图所示。
关于该电池的叙述正确的是
| A.该电池可以在高温下正常工作 |
| B.电池工作时,H+向正极移动 |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.该电池的总反应式为: |
Mg+H202+H2S04=MgS04+2H20
Li-SO2电池具有输出功率高和低温性能好等特点。其电解质是LiBr,溶剂是碳酸丙烯酯和乙腈,电池反应为2Li+2SO2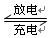 Li2S2O4。下列说法正确的是( )
Li2S2O4。下列说法正确的是( )
| A.该电池反应为可逆反应 |
| B.放电时,Li+向负极移动 |
| C.充电时,阴极反应式为Li++e一=Li |
| D.该电池的电解质溶液可以换成LiBr的水溶液 |
有a、b、c、d四种金属,将a与b用导线连接起来,浸入电解质溶液,b不易腐蚀。将a、d在稀盐酸中构成原电池,电流由a通过导线流向d。将铜浸入b的盐溶液中,无明显变化。如果把铜浸入c的盐溶液中,有金属c析出。这四种金属的活动性由强到弱的顺序是
| A.d c a b | B.d a b c | C.d b a c | D.b a d c |
下列有关电池的说法不正确的是( )
| A.手机上用的锂离子电池属于二次电池 | B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 | D.锌锰干电池中,锌电极是负极 |
下列有关电池的说法不正确的是( )
| A.手机上用的锂离子电池属于二次电池 | B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 | D.锌锰干电池中,锌电极是负极 |
铝-空气电池具有体积小、能量大,污染少等优点,是电动自行车和电动汽车比较理想的电源。电池以食盐水为电解液,总反应为:4Al+3O2+6H2O=4Al(OH)3↓下列说法中正确的是
| A.电池工作时,铝做正极 |
| B.电池负极的电极反应式为:3O2+6H2O+12e-=12OH- |
C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过1mol e—,铝的质量理论上减小9g |
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:( )。 Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是
| A.Cd | B.Ni(OH)2 | C.Cd(OH)2 | D.NiO(OH) |
氢氧燃料电池是一种高性能电池,总反应为2 H2 + O2 =" 2" H2O,电解质溶液为KOH溶液,下列有关该电池的叙述中不正确的是( )。
| A.H2为负极,O2为正极 | B.负极反应:2H2 +4OH-→4H2O + 4e- |
| C.工作时电解质溶液的PH不断增大 | D.正极反应:O2 + 4e- +2 H2O→4OH- |
试题篮
()