X、Y、Z为三种单质。已知:Y能将Z从其化合物的水溶液中置换出来,而Z又能将X从其化合物中置换出来。由此可以推断下列说法中可能正确的是
①单质的氧化性:Y>Z>X;
②单质的还原性:Y>Z>X;
③对应离子的氧化性:X>Z>Y;
④对应离子的还原性:X>Z>Y
| A.只有① | B.只有②③ | C.只有①④ | D.①②③④ |
关于反应K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O的叙述中,正确的是
| A.KCl中含有35Cl | B.生成物Cl2的相对分子质量为73.3 |
| C.该反应转移的电子数为6e- | D.氧化剂和还原剂的物质的量之比为1:6 |
将SO2 气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O===SO
气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O===SO +4H++2Fe2+,
+4H++2Fe2+,
Cr2O +6Fe2++14H+===2Cr3++6Fe3++7H2O。
+6Fe2++14H+===2Cr3++6Fe3++7H2O。
下列说法正确的是( )
| A.还原性:Cr3+>Fe2+>SO2 | B.氧化性:Cr2O >SO2>Fe3+ >SO2>Fe3+ |
C.Cr2O 能将Na2SO3氧化成Na2SO4 能将Na2SO3氧化成Na2SO4 |
D.两个反应中Fe2(SO4)3均作还原剂 |
工业上从硒的废料中提取硒的方法之一是用H2SO4和NaNO3处理废料,获得亚硒酸和少量硒酸。加入盐酸共热,硒酸被转化为亚硒酸(2HCl+H2SeO4==H2SeO3+Cl2+H2O),再将SO2通入亚硒酸溶液中,单质硒即析出。下列叙述正确的是 ( )
| A.H2SeO4的氧化性强于于Cl2 | B.亚硒酸氧化性强于亚硫酸 |
| C.亚硒酸的还原性强于亚硫酸 | D.析出1molSe需H2SeO3、SO2、H2O各1mol |
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为a HClO3 = bO2↑+ c Cl2↑+ d HCl O4 + e H2O。下列有关说法不正确的是
O4 + e H2O。下列有关说法不正确的是
| A.由反应可确定:氧化性HClO3>O2 |
B.由非 金属性Cl>S,可推知酸性HClO3>H2SO4 金属性Cl>S,可推知酸性HClO3>H2SO4 |
| C.若氯酸分解所得混合气体,lmol混合气体质量为45g,则反应方程式可表示为:3HClO3 = 2O2↑+ C12↑+ HClO4 + H2O |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
已知Co2O3在酸性溶液中被还原成Co2+,Co2O3、Cl2、FeCl2、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是
| A.3Cl2 +6FeI2 =2FeCl3 +4FeI3 | B.Cl2 +FeI2=FeCl2 +I2 |
| C.Co2O3+6HCl=2CoCl2 +Cl2 +3H2O | D.2Fe3+ +2I— =2Fe2++I2 |
某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。向该溶液加入溴水后,溴被还原,由此推断该溶液中
| A.不含NO3-,也不含Fe3+ | B.含有NO3-、I-、Cl- |
| C.含I-,不含Cl- | D.含有Fe3+ |
对反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4的下列说法正确的是( )
| A.该反应的氧化剂只有CuSO4 |
| B.SO42﹣既不是氧化产物也不是还原产物 |
C.1molCuSO4氧化了 mol的S mol的S |
| D.被还原的S和被氧化的S的质量比为3:7 |
下列比较中,正确的是
| A.原子半径:Na>Mg | B.碱性:NaOH>KOH |
| C.结合H+的能力:CO32¯<Cl¯ | D.还原性:I¯<Br¯ |
已知在酸性溶液中的还原性强弱顺序为:SO2 > I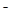 > H2O2 > Fe
> H2O2 > Fe > Cl
> Cl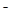 ,下列反应不可能发生的是
,下列反应不可能发生的是
A.2I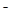 + Fe + Fe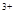 =I2 + Fe =I2 + Fe |
B.2Fe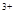 + SO2 + 2H2O=2Fe + SO2 + 2H2O=2Fe + SO + SO + 4H+ + 4H+ |
| C.SO2 + 2H2O + I2=H2SO4 + 2HI |
| D.H2O2 + H2SO4=SO2↑ + O2↑ + 2H2O |
实验室常用NaNO2和NH4Cl反应制取N2。下列有关说法正确的是( )
| A.NaNO2是还原剂 |
| B.NH4Cl中N元素被还原 |
| C.生成1 mol N2时转移6 mol 电子 |
| D.氧化剂和还原剂的物质的量之比是1︰1 |
试题篮
()