根据下列反应判断有关物质的还原性由强到弱的顺序正确的是
①
②
③
A. |
B. |
C. |
D. |
已知下列实验事实:
①Cr2O3固体既能溶于KOH溶液得到KCrO2溶液,又能溶于硫酸得到Cr2(SO4)3溶液;
②向KCrO2溶液中滴加H2O2溶液,再酸化,可得K2Cr2O7溶液;
③将K2Cr2O7溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断不正确的是
| A.化合物KCrO2中Cr元素为+3价 |
| B.实验①证明Cr2O3是两性氧化物 |
| C.实验②证明H2O2既有氧化性又有还原性 |
| D.实验③证明氧化性:Cr2O72— >I2 |
某溶液中含有Cl-与I-的浓度相同,为了氧化I-而不使Cl-氧化,试根据下列三个反应:
①2Fe3++2I-=2Fe2++I2;②2Fe2++Cl2=2Fe3++2Cl-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
判断可选用的氧化剂(氯气除外)是
| A.FeCl2 | B.KMnO4 | C.浓盐酸 | D.FeCl3 |
X、Y、Z、M代表四种金属元素,金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |
下列化学实验事实及其结论都正确的是
| 选项 |
实验事实 |
结论 |
| A |
将SO2通入含HClO的溶液中生成H2SO4 |
HClO的酸性比H2SO4强 |
| B |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面氧化铝熔点高于铝 |
| C |
SiO2可以和NaOH溶液及HF溶液反应 |
SiO2属于两性氧化物 |
| D |
将SO2通入溴水中,溴水褪色 |
SO2具有漂白性 |
Na2FeO4是一种新型水处理剂,可以通过下列反应制取:
湿法制备的主要反应方程为:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3NaCl+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4 +2Na2SO4
下列有关该反应的说法错误的是
| A.两反应中Na2FeO4均为氧化产物 |
| B.Na2FeO4有强氧化性,可消毒杀菌,其还原产物能吸附水中杂质 |
| C.干法中每生成1mol Na2FeO4转移3mol电子 |
| D.碱性条件下,NaClO氧化性大于Na2FeO4 |
已知氧化性:Cl2> Fe3+ >I2。向FeI2溶液中加入一定量的氯水,有关离子方程式错误的是
| A.2 I-+ Cl2 →I2 + 2Cl- |
| B.2Fe2+ + 2I-+ 2Cl2 → 2Fe3+ + I2 + 4Cl- |
| C.2Fe2+ + 4I-+ 3Cl2 → 2Fe3+ + 2I2 + 6Cl- |
| D.2Fe2+ + 6I-+ 4Cl2 → 2Fe3+ + 3I2 + 8Cl- |
下表中叙述Ⅰ和叙述Ⅱ均正确并且互为因果关系的是
| 选项 |
叙述Ⅰ |
叙述Ⅱ |
| A |
NH4Cl是强酸弱碱盐 |
将NH4Cl溶液蒸干可制备NH4Cl固体 |
| B |
Fe3+有强氧化性 |
用KSCN溶液可以鉴别Fe3+ |
| C |
SO2有还原性 |
用SO2可使溴水褪色 |
| D |
Cl2有漂白性 |
用Cl2可与石灰乳反应制备含氯消毒剂 |
下列实验操作、现象和结论均正确的是
| 选项 |
实验操作 |
现象 |
结论 |
| A |
向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 |
有白色沉淀生成 |
该溶液中一定含有Ag+ |
| B |
向AgNO3溶液中滴加过量氨水 |
溶液澄清 |
Ag+与NH3∙H2O能大量共存 |
| C |
用石墨作电极电解MgSO4溶液 |
某电极附近有白色沉淀生成 |
该电极为阳极 |
| D |
将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 |
下层溶液显紫红色 |
氧化性:Fe3+>I2 |
下列实验操作和对应的现象、结论都正确的是
| 选项 |
操 作 |
现 象 |
结 论 |
| A |
在滴有酚酞的Na2CO3溶液中加入BaC12溶液 |
红色褪去 |
Na2CO3溶液中存在水解平衡 |
| B |
将某气体通入品红溶液中 |
品红溶液褪色 |
该气体一定是SO2 |
| C |
将铜板电路投入FeCl3溶液中 |
铜溶于FeCl3溶液 |
氧化性:Fe3+ > Cu2+ |
| D |
向NaCl溶液滴少量AgNO3溶液,再滴加少量NaI溶液 |
先有白色沉淀,后变成黄色沉淀 |
Ksp(AgI) >Ksp(AgCl) |
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通人 SO2气体,溶液逐渐变成无色。下列分析正确的是
| A.滴加KI溶液时,转移2 mol e-时生成 1 mol白色沉淀 |
| B.通入SO2后溶液逐渐变成无色,体现了 SO2的漂白性 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+ >I2 > SO2 |
新型纳米材料MFe2O,(3<x <4)中M表示十2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程为:
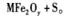 下列判断正确的是
下列判断正确的是
| A.MFe2Ox是还原剂 | B.SO2被氧化 |
| C.x>y | D.氧化性:MFe2Oy>SO2 |
将112mLCl2(标准状况)通入10mL1mol/L的FeBr2溶液中(还原性:Fe2+大于Br-),发生反应的离子方程式是
| A.Cl2+2Br-=2Cl-+Br2 | B.2Fe2++Cl2=2Fe3++2Cl- |
| C.2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 | D.2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
试题篮
()