已知:(1)2Fe3++2I-=2Fe2++I2 (2)Br2+2Fe2+=2Fe3++2Br-由此推断氧化剂的氧化性强弱顺序为
| A.Br2>Fe3+>I2 | B.Fe3+>Br2>I2 | C.I2>Br2>Fe3+ | D.Br2>I2>Fe3+ |
在实验室中常以草酸钠(Na2C2O4)为标准液,通过氧化还原滴定来测定高锰酸钾溶液的浓度,其反应的化学方程式为: C2O42—+MnO4—+H+—→Mn2++CO2↑+H2O。下列有关草酸钠滴定高锰酸钾实验的叙述,正确的是 ( )
| A.滴定过程中,高锰酸钾被氧化,草酸钠被还原 |
| B.用酸式滴定管量取草酸钠溶液 |
| C.该反应中,消耗的草酸钠与高锰酸钾的物质的量之比为5:2 |
| D.为便于滴定终点的判断,滴定时必须往体系中加入指示剂 |
下列关于甲、乙、丙、丁四个图像的说法中,正确的是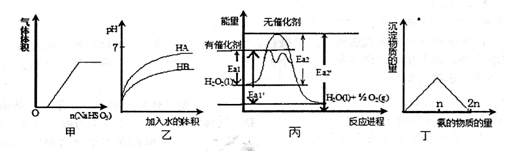
| A.甲是亚硫酸氢钠粉末投入稀硝酸溶液中有关图像 |
| B.乙是等pH的HA和HB两种弱酸溶液稀释时pH变化图,由此可知HA的酸性弱于HB |
| C.由丙可知,双氧水在有催化剂存在时的热化学方程式为 2H2O2(1)="2H" 2O(l)+O2(g) △H=-2(Ea2’-Ea2) kJ·mol-l |
| D.丁是向硝酸银溶液中滴加氨水时,沉淀质量与氨的物质的量的关系图 |
下列事实不能说明元素的金属性或非金属性相对强弱的是
| 序号 |
事实 |
推论 |
| A |
与冷水反应,Na比Mg剧烈 |
金属性:Na > Mg |
| B |
Ca(OH)2的碱性强于Mg(OH)2 |
金属性:Ca > Mg |
| C |
SO2与NaHCO3溶液反应生成CO2 |
非金属性:S > C |
| D |
t℃时,Br2 + H2 2HBr K = 5.6×107 2HBr K = 5.6×107I2 + H2  2HCl K = 43 2HCl K = 43 |
非金属性:Br > I |
已知反应:Na2O2 + SO2 = Na2SO4,则下列判断正确的是
| A.硫元素被还原 |
| B.二氧化硫是还原剂 |
| C.过氧化钠既是氧化剂又是还原剂 |
| D.二氧化硫既不是氧化剂也不是还原剂 |
下列实验方案不能达到预期目的的是( )
| A.用钠、镁分别与水反应,可证明钠、镁的金属性强弱 |
| B.用氯化镁、氯化铝分别于浓氨水反应,可证明钠、镁的金属性强弱 |
| C.用铁、石墨与硫酸铜溶液组成的原电池,可证明铁、铜的金属性强弱 |
| D.把氯气通入溴化钠的水溶液中,看到溶液呈橙色,可证明氯、溴的非金属性强弱 |
甲乙两种非金属,能说明甲比乙的非金属性强的是( )
①甲比乙容易与H2化合;②甲的气态氢化物比乙的气态氢化物稳定;③甲的氧化物对应的水化物的酸性比乙的氧化物对应的水化物酸性强;④与某金属反应时甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低。
| A.①②③ | B.只有⑤ | C.①②③④⑤ | D.①② |
下图所示最验证氯气性质的徼型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O
对实验现象的“解释或结论”正确的是
| 选项 |
实验现象 |
解释或结论 |
| A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
| B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
| C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
| D |
e处变红色 |
还原性:Fe2+>Cl- |
下列陈述正确并且有因果关系的是
| 选项 |
陈述Ⅰ |
陈述Ⅱ |
| A |
SO2有漂白性 |
SO2可使溴水褪色 |
| B |
SiO2有导电性 |
SiO2可用于制备光导纤维 |
| C |
浓硫酸有强氧化性 |
浓硫酸可用于干燥H2和CO |
| D |
Fe3+有强氧化性 |
FeCl3溶液可用于回收废旧电路板中的铜 |
已知:还原性HSO3¯>I¯,氧化性IO3¯> I2。
实验Ⅰ:在一定量NaHSO3的溶液中逐滴加入KIO3溶液;
实验Ⅱ:在一定量的KIO3溶液中逐滴加NaHSO3溶液。下列说法正确的是
| A.两个实验中溶液的pH变化趋势相同 |
| B.两实验中生成等量I2时,转移电子数的物质的量相同 |
| C.在实验Ⅰ的过程中,若NaHSO3初始量为3mol,当溶液中I¯与I2的物质的量之比为5∶2时,氧化产物为3.2mol |
| D.过程Ⅱ中,可以用淀粉作为滴定指示剂,判定第一阶段的反应终点 |
根据表中信息,判断下列叙述中正确的是
| 序号 |
氧化剂 |
还原剂 |
其它反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
/ |
|
Cl- |
| ② |
KClO3 |
浓盐酸 |
/ |
Cl2 |
|
| ③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:
2FeCl3 + 2HI = 2FeCl2 + I2 + 2HCl; 2Co(OH)3 + 6HCl = 2CoCl2 + Cl2↑ + 6H2O
2Fe(OH)2 + I2 + 2KOH= 2Fe(OH)3 + 2KI; 3I2 + 6KOH=" 5KI" + KIO3 + 3H2O
复分解反应:
2HSCN + K2CO3 =" 2KSCN" + CO2 ↑ + H2O; KCN + CO2 + H2O =" HCN" + KHCO3
热分解反应:
4NaClO  3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是:
| A.氧化性(酸性溶液):FeCl3>Co(OH)3>I2 |
| B.还原性(碱性溶液):Fe(OH)2>I2>KIO3 |
| C.热稳定性:NaCl>NaClO4>NaClO |
| D.酸性(水溶液):HSCN>H2CO3>HCN |
下图所示最验证氯气性质的徼型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O
对实验现象的“解释或结论”正确的是
| 选项 |
实验现象 |
解释或结论 |
| A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
| B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
| C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
| D |
e处变红色 |
还原性:Fe2+>Cl- |
根据下表信息,下列叙述中正确的是( )
| 序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
| ① |
Cl2 |
FeBr2 |
Cl- |
||
| ② |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
| ③ |
KClO3 |
浓盐酸 |
Cl2 |
||
| ④ |
KMnO4 |
浓盐酸 |
Cl2 |
Mn2+ |
A.表中①组反应的氧化产物只能是FeCl3
B.氧化性强弱比较:KMnO4>Fe3+>Cl2>Fe2+
C.④的离子方程式配平后,H+的化学计量数为16
D.表中③还原产物是KCl
试题篮
()