某温度下,向pH=6的纯水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2,下列对该溶液的叙述中,不正确的是( )
| A.该温度高于25℃ |
| B.由水电离出来的H+的浓度是1.0×10-10mol/L |
| C.该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性 |
| D.NaHSO4晶体的加入抑制了水的电离 |
室温向10mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目减少 |
B.溶液中 不变 不变 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
| D.再加入10ml pH=11的NaOH溶液,混合液pH=7 |
室温下,水的电离达到平衡H2O H++OH−。下列叙述正确的是( )
H++OH−。下列叙述正确的是( )
| A.加热,平衡向正反应方向移动,Kw不变 |
| B.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大 |
| C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH−)降低 |
| D.向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH−)=c(H+) |
下图是用0.1000 mol/L的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答:
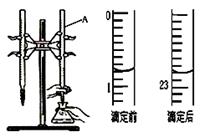
(1) 仪器A的名称是 ;
(2) 盐酸的体积读数:滴定前读数为 mL,滴定后读数为 mL 。
(3) 某实验小组同学的三次实验的实验数据如下表所示。 根据表中数据计算出的待测NaOH溶液的平均浓度是 mol/L。(保留四位有效数字)
| 实验 编号 |
待测NaOH溶液的体积(mL) |
滴定前盐酸的 体积读数(mL) |
滴定后盐酸的 体积读数(mL) |
| 1 |
20.00 |
1.20 |
23.22 |
| 2 |
20.00 |
2.21 |
24.21 |
| 3 |
20.00 |
1.50 |
23.48 |
(4)若用酚酞做指示剂,判断到达滴定终点的实验现象是_____________
(5) 对下列几种假定情况进行讨论:(填“无影响”、“偏高”、“偏低”)
① 若滴定前锥形瓶未用待测液润洗,对测定结果的影响是 ;
②取待测液的滴定管,滴定前滴定管尖端有气泡,滴定后气泡消失。_________
③标准液读数时,若滴定前仰视,滴定后俯视,对测定结果的影响是 ;
下列说法正确的是( )
| A.0.1mol/LCH3COOH溶液加水稀释,溶液中c(OH-)增大 |
| B.将NaOH和氨水溶液各稀释一倍,两者的OH-浓度均减少到原来的1/2 |
| C.相同浓度的HCl和CH3COOH,两溶液中c(H+)相同 |
| D.甲溶液的pH是5,乙溶液的pH是4,则甲溶液与乙溶液的中c(H+)之比为10:1 |
将纯水加热至较高温度,下列叙述正确的是
| A.Kw变大、pH变小、呈酸性 | B.Kw变大、pH不变、呈中性 |
| C.Kw变小、pH变大、呈碱性 | D.Kw变大、pH变小、呈中性 |
25 ℃时,在等体积的①pH=0的H2SO4溶液,②0.05 mol·L-1的Ba(OH)2溶液中,发生电离的水的物质的量之比是( )
| A.1∶10 | B.1∶5 | C.1∶20 | D.1∶10 |
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液。
其操作可分解为如下几步:
a. 移取20.00mL待测的NaOH溶液注入洁净的锥形瓶,并加入2-3滴酚酞
b. 用标准盐酸溶液润洗滴定管2-3次
c. 把盛有标准溶液的酸式滴定管固定好,调节液面使滴定管尖嘴充满溶液
d. 取标准盐酸溶液注入酸式滴定管至0刻度以上2-3cm
e. 调节液面至0或0刻度以下,记下读数
f. 把锥形瓶放在滴定管的下面,用标准盐酸溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)_____________________。
(2)滴定终点时溶液的颜色变化是 。
(3)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
(4)若某次滴定开始和结束时,酸式滴定管中的液面如图所示,则反应消耗盐酸的体积为_____ mL。

(5)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 |
待测NaOH溶液的体积/mL |
0.1000mol/L盐酸的体积/mL |
||
| 滴定前刻度 |
滴定后刻度 |
溶液体积/mL |
||
| 第一次 |
25.00 |
0.20 |
20.22 |
|
| 第二次 |
25.00 |
0.56 |
24.54 |
|
| 第三次 |
25.00 |
0.42 |
20.40 |
|
依据上表数据求得NaOH溶液的物质的量浓度为 (保留4位有效数字)。
室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示.下列有关说法正确的是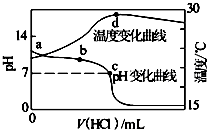
| A.a点由水电离出的c(H+)=1.0×10-14mol·L-1 |
| B.b点:c(NH4+)+c(NH3•H2O)=c(Cl-) |
| C.c点:c(Cl-)=c(NH4+) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
室温下pH=13的NaOH溶液与pH=2的H2SO4溶液混合,所得溶液的pH=11,则NaOH溶液与H2SO4溶液的体积比是
| A.11:1 | B.9:1 | C.1:11 | D.1:9 |
水的电离平衡曲线如图所示,下列说法不正确的是 
| A.图中四点KW间的关系:A=D<C<B |
| B.若从A点到C点,可采用温度不变在水中加少量的CH3COONa固体 |
| C.若从A点到D点,可采用温度不变在水中加入少量酸 |
| D.若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性 |
下列叙述正确的是
| A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵 |
| B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 |
| C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
在一定体积pH = 12的Ba(OH)2溶液中,逐滴加入pH = 2的NaHSO4溶液,当溶液的pH 恰好为7时,则参加反应的Ba(OH)2溶液与NaHSO4溶液的体积比是
| A.1∶9 | B.1∶1 | C.1∶2 | D.1∶4 |
根据所学知识填空。
(1)写出此分子 含有的官能团名称 。
含有的官能团名称 。
(2)写出铝热反应的化学方程式 。
(3)用离子方程式表示泡沫灭火器的灭火原理 。
(4)根据沉淀溶解平衡原理,用离子方程式解释碳酸钙溶于盐酸的过程 。
(5)写出有机物名称为 2,5 -二甲基-4-乙基庚烷的结构简式 。
(6)常温下,将pH=5的盐酸和pH=9的NaOH溶液以一定的体积比混合后,所得溶液的pH=6,则盐酸和氢氧化钠溶液的体积比是 。
(7)下列8组物质,互为同分异构体的是 组。
①甲烷和十七烷 ②金刚石和石墨 ③O2和O3 ④甲苯和苯乙烯
⑤邻二甲苯和间二甲苯 ⑥12C 和14C ⑦ 和
和 ⑧2-丁炔和1,3-丁二烯
⑧2-丁炔和1,3-丁二烯
试题篮
()