常温下a mol/L 稀氨水和b mol/L 稀盐酸等体积混合,对混合后溶液判断一定正确的是
| A.若a=b,则c(NH4+)=c(Cl―) | B.若a>b,则c(NH4+)>c(Cl―) |
| C.若a>b,则c(OH-)>c(H+) | D.若a<b,则c(OH-)<c(H+) |
在25mL 0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1CH3COOH溶液,溶液pH变化曲线如图所示,下列有关离子浓度的比较正确的是

A.在A、B间任一点(不含A、B点),溶液中可能有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C.在C点,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.在D点,c(CH3COO-)+c(CH3COOH)=c(Na+)
已知某温度下0.1mol·L-1的NaHB(强电解质)溶液中c(H+)> c(OH-),则下列有关说法或关系式一定正确的是( )
①HB-的水解程度小于HB-的电离程度; ②c(Na+)=0.1mol·L-1 > c(B2-);
③溶液的pH=1; ④ c(Na+)= c(HB-)+2 c(B2-)+ c(OH-);
| A.①② | B.②③ | C.②④ | D.①②③ |
Na2S溶液中各种离子的物质的量浓度关系不正确的是( )
| A.c(Na+)>c(S2-)>c(OH-)>c(HS-) | B.c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) |
| C.c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) | D.c(OH-)=c(H+) + c(HS-) |
将0.2mol·L-1HCN溶液和0.1mol·L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是
| A.c (HCN)<c (CN-) | B.c (Na+)>c (CN-) |
| C.c (HCN)-c (CN-)=c (OH-) | D.c (HCN)+c (CN-)=0.1mol·L-1 |
下列溶液中有关物质的量浓度关系正确的是( )
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:c(H+) + c(M+)=c(OH-) + c(A-)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) +2c(OH-)=2c(H+) + c(CH3COOH)
D.0.1mol・L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
下列各溶液中,有关成分的物质的量浓度关系正确的是 ( )
A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D.pH相等的(NH4)2SO4、 (NH4)2Fe (SO4)2、NH4Cl溶液:c(NH4Cl)<c[(NH4)2Fe (SO4)2]<c[(NH4)2SO4]
常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通入少量CO2气体生成HX和NaHCO3;往NaY溶液中通入少量CO2生成HY和Na2CO3。下列有关叙述正确的是 ( )
| A.酸性由强至弱:HX>HY>H2CO3 |
| B.结合H+的能力:Y->CO32->X->HCO3- |
| C.溶液碱性:NaX>Na2CO3>NaY>NaHCO3 |
| D.NaX溶液中通入足量CO2后的离子浓度: c(Na+)>c(HCO3-)>c(X-)>c(OH-)>c(H+) |
(2012年高考安徽卷)氢氟酸是一种弱酸,可用来刻蚀玻璃。已知25℃时:
①HF(aq)+OH-(aq)===F-(aq)+H2O(l) ΔH=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
在20 mL 0.1 mol·L-1氢氟酸中加入V mL 0.1 mol·L-1NaOH溶液。下列有关说法正确的是( )
| A.氢氟酸的电离方程式及热效应可表示为:HF(aq) F-(aq)+H+(aq) ΔH=+10.4 kJ·mol-1 |
| B.当V=20时,溶液中:c(OH-)=c(HF)+c(H+) |
| C.当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol·L-1 |
| D.当V>0时,溶液中一定存在:c(Na+)>c(F-)>c(OH-)>c(H+) |
下列溶液中微粒浓度关系一定正确的是( )
A.氨水与氯化铵的pH=7的混合溶液中: (Cl-) (Cl-) |
B.新制氯水中: (Cl-) (Cl-) (ClO-) (ClO-) |
C.室温下,向0.01mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性: |
D.pH=2的一元酸和pH=12的一元强碱等体积混合: |
在常温下,0.1000mol·L-1Na2CO3溶液25mL 用0.1000mol·L-1盐酸滴定,其滴定曲线如下图。对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )

| A.a点:c(CO2-3)=c(HCO-3)>c(OH-) |
| B.b点:5c(Cl-)>4c(HCO-3)+4c(CO2-3) |
| C.c点:c(OH-)=c(H+)+c(HCO-3)+2c(H2CO3) |
| D.d点:c(H+)=c(CO2-3)+c(HCO-3)+c(OH-) |
根据右表提供的数据,下列判断正确的是
A.同温同浓度下,溶液的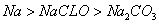 |
B.结合 H+的能力: H+的能力: |
C.碳酸钠溶液中加入少量氢氟酸的离子方程式: |
| D.次氯酸钠溶液中通少量二氧化碳的离子方程式: |
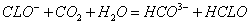
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa与HCl;②CH3COONa与NaOH③CH3COONa与NaCl④CH3COONa与NaHCO3
下列各项排序正确的是
| A.pH:②>③>④>① | B.c(CH3COO-):②>④>③>① |
| C.溶液中c(H+):①>③>②>④ | D.c(CH3COOH):①>④>③>② |
常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定错误的是
| A.若c(OH-)>c(H+),a=b | B.若c(K+)>c(CH3COO-),a>b |
| C.若c(OH-)=c(H+),a>b | D.若c(K+)<c(CH3COO-),a<b |
试题篮
()