(1)在中学所学的金属单质中,在冷的浓硫酸或硝酸中会发生钝化现象的有_______(填化学式);
(2)写出铁与浓硫酸(足量)在加热条件下反应的化学方程式___________________;
(3)铝分别与氢氧化钠溶液和稀硫酸反应,若在相同情况下得到相同体积的气体,则两个反应中消耗氢氧化钠与硫酸的物质的量之比为___________。
(10)按要求填空
(1)二氧化硫气体通入碘水,碘水褪色,该反应的化学方程式 。
(2)实验室制备氨气的化学方程式 。
(3)制备漂白粉的化学方程式 。
(4)收集满一烧瓶纯的二氧化氮气体做喷泉实验,假设溶液不扩散,所得溶液的物质的量浓度 。
(5)金属锌和硝酸物质的量之比为2:5恰好完全反应,该反应的化学方程式 。
(14分)使用如图所示装置进行化学小实验,请填写下列空白: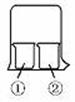
(1)若①中放一片湿润的红色石蕊试纸,②装有浓氨水,可观察到的实验现象为 。
(2)若①装有AlCl3溶液,②装有浓氨水,可观察到的实验现象为 ,反应的离子方程式为 。
(3)若①装有浓硝酸,②装有浓氨水,可观察到的实验现象为 ,反应的化学方程式为 。
(4)若①装有浓硝酸,②装有Na2SO3溶液,实验时有无色气体产生,该气体逐渐变为红棕色,用化学方程式表示无色气体变为红棕色的原因 ,写出浓硝酸和Na2SO3溶液反应的离子方程式 。
按要求回答下列问题:
(1)下列事实反映了硫酸、硝酸的什么性质:
①实验室用锌粒和稀硫酸反应制取氢气 ;
②浓硫酸能使胆矾晶体由蓝变白 ;
③浓硫酸使纸张变黑 ;
④硝酸溶解金属铜 ;
⑤可用稀硝酸与CaCO3作用制取CO2 。
(2)将6.4g铜与一定浓度的浓硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为1.12L,请回答下列问题:
①写出铜与浓硝酸反应生成NO2气体的离子方程式: ;
②参加反应的HNO3的物质的量是: mol。
下图为喷泉实验装置图。
(1)若大烧瓶内充入的为干燥NH3,要使喷泉形成表中的各种颜色,请写出A溶液里溶质(如能用有关离子表示,请写出离子符号)的名称或离子符号。
| 实验编号 |
A溶液颜色 |
B溶液颜色 |
A溶液中溶质 |
| ① |
无色 |
红色 |
|
| ② |
黄色 |
红褐色浑浊 |
|
| ③ |
紫色 |
蓝色 |
|
| ④ |
无色 |
乳白色浑浊 |
|
(2)分析实验①中B溶液变红色的原因(结合方程式说明)______________ 。
实验②反应的离子方程式为________________________________________。
铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)
(1)硝酸在该反应中表现出的性质是_____________________。
(2)0.4molCu被硝酸完全溶解后,硝酸得到的电子数是________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是________mol。
(3)0.3molCu被另一浓度的硝酸完全溶解后,如果此时产生的NO和NO2气体总体积在标准状况下为8.96 L,则被还原的硝酸的物质的量是_______mol,参加反应的硝酸的物质的量是______mol,产生的混合气体中NO和NO2体积比为_______。
按要求填空:
(1)Fe(OH)2在空气中变质的化学方程为:_____________________________。
(2)漂白粉在空气中久置会变质,变质过程中既有非氧化还原反应又有氧化还原反应,其中氧化还原反应的方程式为:_______________________________。
(3)实验室制备氨气的反应方程式为:______________________,收集氨气时,在试管口放一小团棉花其作用是________________,用_______________试纸检验氨气是否收集满。
(4)将CaMg3Si4O12改写为氧化物的形式:_______________________。
(1)写出一个化学方程式,其转化属于“氮的固定”: 。
(2)写出实验室制取氨气的化学方程式: ,
实验室可以用 试纸检验氨气。
(3)NO2与水反应的化学方程式为 ,该反应中氧化剂与还原剂的物质的量之比为 。
硝酸具有强氧化性,请分别写出Cu与浓硝酸、稀硝酸反应的化学方程式。
、 。现有 铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为
铜片与某浓度的硝酸反应,生成气体的体积在标准状况下为 ,则被还原的硝酸的物质的量为 。
,则被还原的硝酸的物质的量为 。
I.小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式: 。
II.氨气通入水中可制得氨水,氨水能使无色的酚酞变红。请写出实验室制取氨气的化学方程式: ,
检验氨气的一种化学方法是: 。
III.火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中氧化剂是 ;还原剂是 。
若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是 ;六种元素中,最高价氧化物对应水化物的酸性最强的是_________(填元素符号)。
已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如下图①所示:
(1)将气体B点燃,把导管伸入盛满气体A的集气瓶,反应过程中的实验现象有 (填序号)。
①放热 ②黄绿色褪去 ③瓶口有白雾 ④瓶口有白烟
⑤安静燃烧,发出黄色火焰 ⑥安静燃烧,发出苍白色火焰
(2)实验室制D的化学方程式为 。
(3)实验室可用如上图②所示装置收集D,下列叙述正确的是 (填序号)。
①D气体不能用排水法收集
②干燥管里盛有碱石灰
③图②中试管口处的a为棉花团,其作用是防止氨气逸出
(4)气体D催化氧化的化学方程式为 。
(5)物质E的化学式是 ;E在下列物质分类中所属的物质种类是 (填序号)。
①电解质 ②化合物 ③混合物 ④纯净物 ⑤非电解质 ⑥盐
(10分)(1)下列实验方法合理的是________。
| A.用加热法除去食盐固体中的氯化铵 |
| B.将碘的饱和水溶液中的碘提取出来,可用酒精进行萃取 |
| C.实验室制取Al(OH)3:往AlCl3溶液中加入NaOH溶液至过量 |
| D.往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质 |
(2)SiO2广泛存在于自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学反应方程式
________________________________________________________________________。
(3)铝是一种重要金属:铝与NaOH溶液反应的离子方程式为:
________________________________________________________________________。
(4)将10.7 g氯化铵固体与足量消石灰混合加热使之充分反应。生成气体在标准状况下的体积是________L。
将1.92 g铜置入一定量的浓硝酸中,并微热,随着铜的不断减少,反应生成的气体颜色逐渐变浅,当铜反应完毕时(铜片完全消失),共收集到标况下气体1.12 L(设不含N2O4),求:
(1)收集到的气体中主要有含有 ;
(2)上述过程中,有关反应的化学方程式为 ; ;
(3)反应中被还原的HNO3的物质的量是 ;
(4)将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2,使其充分反应,若要使水恰好充满容器,理论上需要参加反应的O2的物质的量是多少摩尔?(计算过程)
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
(1)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示该物质C的一个重要应用 ;
(2)若A是一种黄色单质固体,则B→C的化学方程式为 ;
(3)若A是一种黑色非金属单质固体,写出B的一个用途 ;
(4)若C是红棕色气体,则A化学式可能为 ,试写出C与水反应的化学方程式 。
试题篮
()