氨是一种重要的化工产品,其化学式为 ,具有 气味,密度比空气的 (填“大”或“小”), (填“易”或“难”)溶于水,因此,收集氨气应采用_______________法。
如右图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由_______________逐渐变为_______色,试管内的液面会逐渐_____________,剩余气体约占试管容积的__________,用化学方程式表示这种变化__________________________;上述反应停止后向试管中缓慢通入氧气,气体颜色又由______色逐渐变为____________色,之后又变为______色,继续通入氧气,直到试管中充满液体为止,用一个化学方程式表示试管中发生的化学反应_____________________________________。
(12分)工业制硝酸的主要反应之一是: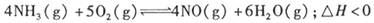
(1)若反应起始的物质的量相同,下列关系图错误的是________ (填编号)。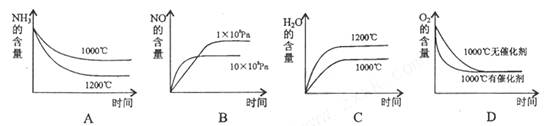
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
①反应在第2min到第4min时,O2的平均反应速率为________mol/(L ? min)。
②反应在第2min时改变了条件,改变的条件可能是________ (填编号)。
A 增加O2的浓度 B.升高温度 C.减小压强 D.使用催化剂
(3)将一定量铝粉和铁粉的混合物与上述反的稀硝酸充分反应,反应过程中无气体放出(氧化物产生)。在反应结束后的溶液中,滴加5mol/L的NaOH溶液,所加NaOH溶液(mL)与产生的沉淀的物质的量关系如图所示则: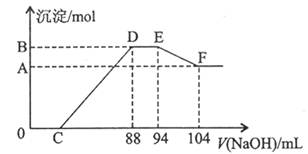
EF段反应的离子方程式是_______________;铝粉与铁粉的物质的量之比是_____________
硝酸溶液中含HNO3的物质的量是__________mol。
将32g铜与200mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
NO的体积为 L,NO2的体积为 L。
待产生气体全部释放后,溶液中加500mL 4mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 mol/L。
三氟化氮(NF3)是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。它可在铜的催化作用下由F2和过量的NH3反应得到,该反应另一种产物为盐。
(1)该反应的化学方程式为 ,生成物NF3中氮原子的杂化方式为 ,NF3分子空间构型为 ;
(2)N、F两种元素的氢化物稳定性比较,NH3 HF(选填“>”或“<”);
(3)N3-被称为类卤离子,写出1种与N3-互为等电子体的分子的化学式 ;
(4)元素A基态原子的核外电子排布式为1s22s22p63s23p64s2,A跟氟可形成离子化合物,其晶胞结构如图,该离子化合物的化学式为 。
(6分)氮气其化合物是中学化学的基础知识,请你回答下列含氮化合物的有关问题。
(1)汽车尾气中含有氮氧化物,严重污染大气。NO和NO2是常见的氮氧化物,这两种氮氧化物中,呈红棕色的是 ;
(2)一氧化氮在常温下很容易与空气中的氧气化合,生成二氧化氮。该反应的化
学方程式为: ;
(3)实验室常用NH3做“喷泉实验”,该实验说明NH3的溶解性是 溶于水(填“极易”或“极难”)。
雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1) As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,则氧化剂与氧化产物的物质的量之比为 。
(2)上述反应中产生的气体可用 吸收。
(3) As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3— = 2H3AsO4+ 3S+10NO2↑+ 2H2O
若生成48g S,则生成标准状况下的NO2的体积为 L。若准确测得的实际体积小于理论值(计算值),请分析可能原因 。
(4)某课外活动小组设计了以下实验方案验证Ag与浓HNO3反应的过程中可能产生NO。其实验流程图如下:
①测定硝酸的物质的量:
反应结束后,从如图B装置中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为 。
②测定NO的体积:
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中 (填“有”或“没有”)NO产生,作此判断的依据是 。
甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系。
甲+乙 丙+丁
丙+丁
(1)转化关系中所涉及的反应甲和乙为非氧化还原反应,且乙为水。
① 若甲为固体,甲和乙反应生成的丙和丁是二种弱碱。则甲的化学式是 。
② 若甲是由N和Cl元素组成的化合物,其分子结构模型如右图所示,则反应的化学方程式是 。

(2)转化关系中所涉及的反应为氧化还原反应,且乙为水。
① 若甲和丙是同主族元素组成的单质,且组成甲的元素位于第三周期,此反应的离子方程式是 。
② 若丙和丁都可在一定条件下还原 ,此反应的化学方程式是 。
,此反应的化学方程式是 。
③ 若甲是由N和O元素组成的气态物质,呈红棕色。将3.36 g 加到一定量丙
加到一定量丙
稀溶液中,收集到1.12 L气体丁(已折算为标准状况),则反应的离子方程式是 。
(3)Hofmann依据上述转化关系测定氨分子的组成。现用如右图所示的装置进行实验,打开分液漏斗的活塞,滴下浓氨水,至不再反应为止;关闭分液漏斗的活塞,待恢复到室温,打开止水夹,试管内液面上升至三分之二处。

① 滴下浓氨水一段时间后,试管内发生反应的化学方程式是 。
② 证明试管内“不再反应”的实验操作和现象是 。
(6分)在50 mL a mol·L-1的硝酸溶液中,加入6.4 g Cu,全部溶解,假设硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100 mL时测得c(NO3-)=3 mol·L-1。
(1)求稀释后的溶液pH=________.
(2)若a=9,则生成的气体中NO2的物质的量为________mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH===2NaNO2+H2O
2NO2+2NaOH===NaNO2+NaNO3+H2O
若将上述的NO2和NO的混合气体通入1 mol·L-1的NaOH溶液恰好被吸收,NaOH溶液的体积为________mL。
发射航天火箭常用氮的氢化物肼(N2H4)作燃料。试回答下列有关问题:
(1)N2H4燃烧时用NO2作氧化剂,它们相互反应生成氮气和水蒸气。
则N2H4和NO2反应生成氮气和水蒸气的热化学方程式为 。
(2)利用肼、氧气与KOH溶液组成碱性燃料电池,氮元素被氧化后只生成氮气,请写出该电池工作时负极的电极反应 ;电池工作时, 极pH升高。
(3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的化学方程式 。
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出盐酸肼第一步水解反应的离子方程式 。
通常采用将钠与亚硝酸钠(NaNO2)在空气中共热的方法制取氧化钠,反应的另一产物为N2,则该反应的化学方程式为_______________,该反应的氧化剂是________,被氧化的元素是___________。
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如下图所示(图 中的ΔH表示生成1 mol产物的数据)。
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热 化学方程式是_________________________________;
化学方程式是_________________________________;
(2)PCl5分解成PCl3和Cl2的热化学方程式是_________________________________;
(3)上述分解反应是一个可逆反应。温度T1时,在密闭容器中加入0.80 mol PCl5,反应达平衡时PCl5[来还剩0.60 mol,其分解率α1等于________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,
α2________α1(填“大于”、“小于”或“等于”)
建筑工地常用的NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生如下反应:

(1)配平并标出电子转移的方向和数目。
(2)上述反应的氧化剂是 ;若有1 mol的还原剂被氧化,则反应中转移电子的的数目是 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别NaNO2和NaCl,可选用的物质有:① 水 ② 碘化钾淀粉试纸  ③ 淀粉 ④ 白酒 ⑤ 食醋,进行实验,下列几组合适的是 (填序号)。
③ 淀粉 ④ 白酒 ⑤ 食醋,进行实验,下列几组合适的是 (填序号)。
| A.③⑤ | B.①②④ |
| C.①②⑤ | D.①②③⑤ |
(4)某厂废切削液中,含有2%—5%的NaNO2,直接排放会造成污染,采用NH4Cl,能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为 ;该反应中被氧化的元素是 。
(5)采用烧碱处理硝酸工业尾气可以获得副产品NaNO2,变废为宝。若采用a L b mol/L的烧碱处理硝酸工业尾气,最多可以获得NaNO2的物质的量为 mol。
(9分)
烟气中NOX是NO和NO2的混合物 (1)根据废气排放标准,1 m3烟气最高允许含400 mg NOx。若NOX中NO质量分数为0.54,则100 m3烟气中最高允许含NOx __________L(标准状况),最高允许NOx分子数目为 。
(1)根据废气排放标准,1 m3烟气最高允许含400 mg NOx。若NOX中NO质量分数为0.54,则100 m3烟气中最高允许含NOx __________L(标准状况),最高允许NOx分子数目为 。
(2)如果用溶质质量分数为0.106的Na2CO3水溶液(密度1.1 g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为____________mol/L。 (3)已知:
(3)已知:

 (NO
(NO 不能直接被Na2CO3水溶液吸收)
不能直接被Na2CO3水溶液吸收)
1000 m3(1)中所述烟气尽可能被(2)中所述Na2CO3水溶液吸收,至少需要 L Na2CO3水溶液(保留2位小数),烟气中NOx (填“能”或 “不能”)被除尽。
“不能”)被除尽。
试题篮
()