下列说法正确的是
| A.分子内共价键越强,分子越稳定,其熔、沸点也越高 |
| B.共价化合物溶于水,分子内共价键一定被破坏 |
| C.离子键的形成一定有电子的得与失 |
| D.分子晶体中一定存在分子间作用力,不一定存在共价键 |
NA为阿伏加德罗常数,下列说法错误的是
| A.0.1mol的甲基(—CH3)与羟基(—OH)所含电子数均为NA |
| B.1molD216O中含中子、质子、电子各10NA |
C.32 g S8单质(分子结构如图)中含有的S—S键个数为NA |
| D.1.5g CH3+中含有的电子数为0.8NA |
下列各组物质中化学键类型和数目都相同的一组
① CO2 ② Na2O2 ③ CaC12 ④ NaOH ⑤ NaC1O
| A.①② | B.④⑤ | C.②③ | D.①③ |
下列各组物质中,含有离子键的是
| A.H2 | B.NaCl | C.HCl | D.CO2 |
下列有关硫元素及其化合物的表示正确的是
A.中子数为18的硫原子: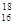 S S |
B.CS2分子的电子式: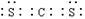 |
C.硫离子(S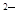 )的结构示意图: )的结构示意图: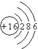 |
D.苯磺酸的结构简式: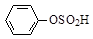 |
最近美国宇航局的科研人员确认火星地表含有溶有高氯酸盐的液态水。下列有关水及高氯酸盐的说法错误的是
| A.水是一种弱电解质 |
| B.NH4ClO4溶液显酸性 |
| C.NaClO4中含有离子键和共价键 |
| D.NH4ClO4只有氧化性,没有还原性 |
已知:(1)Al(OH)3电离方程式为:AlO2-+H++H2O Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-
(2)无水AlCl3晶体沸点为182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:
PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb
则下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
| A.均为强电解质 |
| B.均为弱电解质 |
| C.均为离子化合物 |
| D.均为共价化合物 |
关于化学键的叙述正确的是
| A.离子化合物中只存在离子键 |
| B.非金属元素组成的化合物中可能存在离子键 |
| C.由不同种元素组成的多原子分子里,一定只存在极性共价键 |
| D.含金属元素的化合物中一定存在离子键 |
有如下有机物:
① ②
② ③
③
④CH3CH=CHCH3 ⑤ ⑥
⑥ ⑦
⑦
(1)互为同分异构体的是:__________,存在手性异构体的是:____________,存在顺反异构体的是__________,互为同系物的是(任写一对):__________;

(2)氢核磁共振(1H-NMR)图谱如上图所示的有_______________________;
(3)上述物质中,不属于同分异构体,相同质量时,在氧气中完全燃烧消耗的氧气的质量完全相同的烃是:____________________;
(4)有机物④的系统命名法名称是_____________________;
(5)有机物⑤的键线式_____________,其分子中碳原子_______杂化。
试题篮
()