室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A.溶液中导电粒子的数目增加,导电性增强 |
| B.醋酸的电离程度增大,c(H+)亦增大 |
| C.再加入10mL pH="11" NaOH溶液,混合液pH=7 |
D.溶液中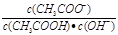 不变 不变 |
用惰性电极电解下列溶液一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),可能使溶液完全复原的是
| A.CuCl2 (CuO) | B.NaOH (NaOH) |
| C.CuSO4 (Cu(OH)2 ) | D.NaCl (Cl2) |
(7分)用电石和水反应,产生的乙炔中含有H2S等杂质。某学生拟选用①NaOH溶液、②KMnO4溶液、③CuSO4溶液、④浓HNO3、⑤浓H2SO4中的一种除去H2S杂质,经研究最后他确定选用的溶液是 (填序号),如果没有该试剂,请你用其它试剂代替(写一种化学式) 。选用前者而发生的离子方程式为 。但这一方程式所表示的制取原理与一般的情况有所不同,如强制弱、稳定制不稳定、难挥发制易挥发等,请用离子方程式表述将稀盐酸逐滴滴加到NaOH和Na2CO3混合溶液中的变化过程: 。
下列有关的叙述正确的是
| A.常温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为 c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.用pH=3和pH=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb |
| D.Na2BeO2溶液的pH>7,BeCl2溶液的pH<7,分别将它们蒸干并灼烧后,都可能生成BeO |
如图所示,将两烧杯用导线如图相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是 
| A.Cu极附近OH-浓度增大 |
| B.Cu极为原电池负极 |
| C.电子流向是由C极流向Pt极 |
| D.当C极上有4 mol电子转移时,Pt极上有1 mol O2生成 |
浓度都是0.1 mol·L-1的弱酸HX溶液与NaX溶液等体积混合后,在所得溶液中,有关离子浓度的关系错误的是( )
| A.C(Na+)+C(H+)=C(X-)+C(OH-) |
| B.C(X-)+ C(HX)=2C(Na+) |
| C.若混合物呈酸性, 则C(X-)>C(Na+)>C(HX)>C(H+)>C(OH-) |
| D.若混合物呈碱性, 则C(Na+)>C(HX)>C(X-)>C(OH-)>C(H+) |
已知下面三个数据:7.2×10-4 mol·L-1、4.6×10-4 mol·L-1、4.9×10-10 mol·L-1分别是下列有关的三种酸的电离常数的数值,若已知下列反应可以发生:
NaCN+HNO2===HCN+NaNO2 NaCN+HF===HCN+NaF
NaNO2+HF===HNO2+NaF,由此可判断下列叙述不正确的是
| A.NaCN和HCN 物质的量比1︰1组成的混合溶液呈酸性 |
| B.物质的量浓度均为0.1mol·l-1的NaF、NaNO2、NaCN溶液的pH逐渐增大 |
| C.根据上述某两个反应即可得出电离常数大小的结论 |
| D.电离常数为:K(HCN)<K(HNO2)<K(HF) |
已知某溶液中含有4种离子:A+、B一、H+、OH一,对这4种离子浓度的大小比较,有以下3种说法。请判断离子浓度大小顺序是否正确,你认为正确的请在相应的空格内填上符合这种情况的A+和B-组成物质的化学式(只写一种情况,可以是一种溶质,或两种溶质);你认为一定不正确的,请在相应的空格内填上你选择“不正确”的理由。供选择的离子有:Na+、Ag+、NH4+、Cl-、NO3-、CH3COO-、H+、OH-
(1)[B- ]>[A+]>[H+]>[OH- ]:
(2)[A+]>[B- ]>[OH- ]>[H+]:
(3)[H+]>[B- ]>[A+]>[OH- ]: 
纯水中c(H+)=5.0×10-7mol/L,则此时纯水中的c(OH-) =_____ mol/L;若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-) =______ mol/L;在该温度时,往水中滴入NaOH溶液,溶液中的C(OH-)=5.0×10-2 mol/L,则溶液的PH值为 。 (已知lg5=0.7,lg3=0.477)
下列说法正确的是( )
| A.物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH)前者小于后者 |
| B.Al3+、NO3-、Cl-、CO32-、Na+可大量共存于pH=2的溶液中 |
| C.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同 |
| D.乙醇和乙酸都能溶于水,都是电解质 |
某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,溶液pH随体积变化的曲线如图所示。据图判断下列说法正确的是 (  )
)
| A.Ⅱ为盐酸稀释时的pH变化曲线 |
| B.b点溶液的导电性比c点溶液的导电性强 |
C.a点K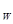 的数值比c点K 的数值比c点K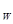 的数值大 的数值大 |
| D.b点酸的总浓度大于a点酸的总浓度 |
(12分)某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离: H2A H++HA-, HA-
H++HA-, HA- H++A2 -已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
H++A2 -已知相同浓度时的电离度α(H2A)>α(HA-),设有下列四种溶液:
A. 0.01 mol·L-1的H2A溶液
B. 0.01 mol·L-1的NaHA溶液
C.0.02 mol·L-1的HCl与0.04 mol·L-1的NaHA溶液等体积混合液
D.0.02 mol·L-1的NaOH与0.02 mol·L-1的NaHA溶液等体积混合液,据此,填写下列空白(填代号):
(1)c(H+)最大的是 ,最小的是 。
(2)c(H2A)最大的是 ,最小的是 。
(3)c(A2-)最大的是 ,最小的是 。
试题篮
()