常温下,下列溶液c(H+)="0.01" mol·L-1的是( )
| A.0.01 mol·L-1 CH3COOH溶液 |
| B.10-3 mol·L-1 H2SO4浓缩到原体积的110. |
| C.pH=1的H2SO4稀释10倍 |
| D.c(OH-)=10-2 mol·L-1的某溶液 |
下列溶液中的Cl-浓度与50mL 1mol/L MgCl2溶液中的Cl-浓度相等的是 ( )
| A.150 mL 1 mol/L NaCl溶液 | B.75 mL 2 mol/L CaCl2溶液 |
| C.150 mL 2 mol/L KCl溶液 | D.75 mL 1 mol/LAlCl3溶液 |
有50 mL 0.2 mol·L-1的氨水溶液,欲使溶液的pH变小,可采用的方法是( )
| A.加少量NaOH |
| B.加100 mL 水 |
| C.加10 mL 0.4 mol·L-1的氨水 |
| D.加少量Na2CO3溶液 |
某学生用 和
和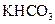 组成的混合物与盐酸反应并进行实验,测得如下数据(盐酸的物质的量浓度相等)
组成的混合物与盐酸反应并进行实验,测得如下数据(盐酸的物质的量浓度相等)
| |
50mL盐酸 |
50mL盐酸 |
50mL盐酸 |
| m(混合物) |
9.2g |
15.7g |
27.6g |
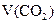 (标准状况) (标准状况) |
2.24L |
3.36L |
3.36L |
则下列分析推理中不正确的是( )
A.盐酸的物质的量浓度为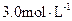 |
B.根据表中数据能计算出混合物中 的质量分数 的质量分数 |
| C.加入混合物9.2g的一组实验中盐酸过量 |
| D.15.7g混合物恰好与盐酸完全反应 |
pH=3的两种酸溶液A、B,分别与足量的锌反应,酸A比酸B产生的氢气的量多。下列说法正确的是( )
A.A是强酸、B是弱酸
B.A是弱酸、B是强酸
C.A是强酸、B是强酸
D.无法判断A、B酸性的相对强弱
36.5gHCl溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质的量浓度为c mol/L,NA表示阿伏加德罗常数,则下列叙述中正确的是( )
| A.所得溶液的物质的量浓度:HCl=1mol/L |
| B.所得溶液中含有NA个HCl分子 |
| C.常温下,36.5g HCl气体占有的体积一定为22.4L |
| D.所得溶液的质量分数:ω=36.5c/(1000ρ) |
对某雨水的水样分析的数据如下
C(CA2+)=3.0×10-6 mol·L-1、C(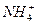 )=2.0×10-6 mol·L-1、C(Cl-)=3.5×10-6 mol·L-1、C(
)=2.0×10-6 mol·L-1、C(Cl-)=3.5×10-6 mol·L-1、C(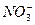 )=4.5×10-6 mol·L-1、C(
)=4.5×10-6 mol·L-1、C(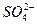 )=5.0×10-6 mol·L-1,则此雨水的pH约为( )
)=5.0×10-6 mol·L-1,则此雨水的pH约为( )
| A.3 | B.4 | C.5 | D.6 |
有两份体积相同的某植物营养液,其配方如下:
| |
KCl |
K2SO4 |
ZnSO4 |
ZnCl2 |
| (1) |
0.15mol |
0.1mol |
0.05mol |
— |
| (2) |
0.05mol |
0.15mol |
— |
0.05mol |
两份营养液的成分
| A.仅c(K+)相同 | B.完全相同 |
| C.仅c(Cl-)相同 | D.完全不同 |
在200 mL某硫酸盐溶液中,含有1.5 NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( )
A.2 mol·L-1 B.2.5 mol·L-1 C.5 mol·L-1 D.7.5 mol·L-1
室温下,将1.00mol· L-1盐酸滴入20.00mL1.00mol· L-1氨水中,溶液pH随加入盐
酸体积变化曲线如图所示。下列有关说法正确的是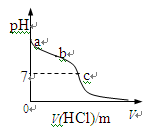
| A.a点:pH=14 |
| B.b点:c(NH4+) +c(NH3·H2O) = c(Cl-) |
| C.c点:水电离出的c(H+) = 1.0×10-7mol· L-1 |
| D.c点后,溶液中离子浓度大小关系一定为: |
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
Mg(ClO3)2在农业上常用作脱叶剂、催熟剂,可采用复分解反应制备:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl。已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示。下列叙述正常的是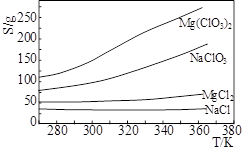
| A.四种化合物的溶解度随温度变化最小的是Mg(ClO3)2 |
| B.300K时,MgCl2的溶解度约为55g |
| C.300K时,100gNaCl饱和溶液中约含有NaCl 36g |
| D.该反应能够进行的条件是生成沉淀,该沉淀是Mg(ClO3)2 |
室温下,向pH=13的氢氧化钡溶液中加入等体积的下列溶液后,滴入石蕊试液,出现蓝色,该溶液可能是:
| A.0.05 mol·L-1的硫酸溶液 |
| B.0.1 mol·L-1的硫酸钠溶液 |
| C.pH=1的醋酸溶液 |
| D.pH=1的盐酸 |
pH=11的x、y两种碱溶液各5mL,分别稀释至500mL,其pH与溶液体积(V)的关系如图所示,下列结论正确的是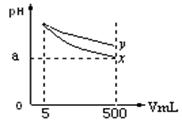
| A.相同温度下,x的电离平衡常数小于y |
| B.若x、y是一元碱,等物质的量浓度的盐酸盐溶液,y的pH大 |
| C.若x、y都是弱碱,则a的值一定大于9 |
| D.完全中和x,y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y) |
将0.1mol/L的醋酸钠溶液20mL与0.1mol/L盐酸10mL混合后,溶液显酸性,则溶液有关微粒的浓度关系正确的是
A c (Ac-)>c (Cl-)>c (H+)>c (HAc)
B c (Ac-)>c (Cl-)>c (HAc)>c(H+)
C c (Ac-)=c (Cl+)>c (H+)>c (HAc)
D c (Na+)+c (H+)=c (Ac-)+c (OH-)
试题篮
()