25℃时,向V mL pH=a的盐酸中,滴加p H=b的NaOH溶液10V mL时,溶液中的Cl-和Na+的物质的量相等,则a+b的值是
H=b的NaOH溶液10V mL时,溶液中的Cl-和Na+的物质的量相等,则a+b的值是
| A.13 | B.14 | C.15 | D.不能确定 |
在密闭容器中发生反应:aX(g)+bY(g) cZ(g)+dW(g),达到平衡后,
cZ(g)+dW(g),达到平衡后, 保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述不正确的是
保持温度不变,将气体压缩到原来的一半体积,当再次达到平衡时,W的浓度为原平衡的1.8倍。下列叙述不正确的是
| A.a+b>c+d | B.平衡向逆反应方向移动 |
| C.Z的体积分数减小 | D.X的转化率下降 |
一定温度 下, 向aL的密闭容器中加入2molNO2(g), 发生如下反应:2NO2
下, 向aL的密闭容器中加入2molNO2(g), 发生如下反应:2NO2 2NO+O2,此反应达到平衡的标志是 ( )
2NO+O2,此反应达到平衡的标志是 ( )
| A.单位时间内生成2nmolNO同时生成2nmolNO2 |
| B.混合气体中NO2、NO和O2的物质的量之比为2:2:1 |
| C.单位时间内生成2nmolNO同时生成nmolO2 |
| D.混合气体的颜色变浅 |
在某温度下,将H2和I2各0.10mol 的气态混合物充入10L的密闭容器中,充分反应,达到平衡后,测得 c(H2)= 0.0060mol/L
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2和I2蒸汽各0.20mol 的气态混合物,试求达到化学平衡状态时各物质的浓度
(每空2分共8分)
向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
①.若a=0,b=0,则c=
②.若a=0.7,b=2.1,则:
Ⅰ.c= .
Ⅱ.这时反应向 进行.
Ⅲ.若要维持反应开始向该反应方向进行,c的范围是
两个完全相同的恒容容器A和B,已知A装有SO2和O2各1g,B中装有SO2和O2各2g,在相同温度下达到平衡,设A中SO2的转化率为a% ,B中SO2的转化率为b%,则A、B两个容器中SO2的转化率的关系是
A.a%> b% B.a%= b%
C.a%< b% D.无法确定
下列说法正确的是
| A.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
| B.NH4HCO3(s)===NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ/mol可能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
对于0.1mol/L CH3COOH溶液,下列叙述正确的是
| A.加入水时,平衡逆反应方向移动 |
| B.加入少量的NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol/L HCl溶液,溶液中C(H+)减少 |
| D.加入少量CH3COONa 固体,平衡向正反应方向移动 |
在100℃和200kPa的条件下,反应aA(g)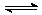 bB(g)+c C(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度。
bB(g)+c C(g)建立平衡后,在不加入任何物质的条件下逐步增大体系的压强(维护温度不变),下表列出的不同压强下反应建立平衡时物质B的浓度。
| 压强(kPa) |
200 |
500 |
1000 |
| B的浓度(mol/L) |
0.04 |
0.1 |
0.27 |
根据表中的数据,回答下列问题:
(1)压强从200kPa增加到500kPa时,平衡 移动(填“正向”或“逆向”或“不”),理由是 。
(2)压强从500kPa增加到1000kPa时,平衡 移动(填“正向”或“逆向”或“不”),其原因可能为 。
25 ℃时,水的电离达到平衡:H2O  H+ + OH-;ΔH > 0 ,下列叙述正确的是
H+ + OH-;ΔH > 0 ,下列叙述正确的是
| A.向水中加人稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加人少量固体NaOH,平衡正向移动,c(OH-)升高 |
| D.将水加热,Kw增大,pH不变 |
T℃时,有甲.乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲.乙两容器中加入6mol A和3mol B,发生反应如下:
3A(g)+b B(g)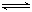 3C(g)+2D(g),(b为
3C(g)+2D(g),(b为 3的正整数) 。
3的正整数) 。
4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;
t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。
根据题给的信息回答下列问题:
(1)甲容器中反应的平均速率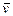 (B)= 。
(B)= 。
(2)在温度T℃时,该反应的化学平衡常数为__________________.
由下表数据可知该反应为______________(填“吸热”“放热”)反应。
化学平衡常数K和温度t的关系如下表:
| t℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
(3)T℃时,在另一个体积与乙相同的丙容器中,为了达到平衡时B的浓度仍然为0.8mol/L,起始时,向丙容器中加入C、D的物质的量分别为3mol.2mol,则还需加入A.B的物质的量分别是___________.___________。
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g) H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
试回答下列问题:
⑴下列措施中有利于提高尿素的产率的是___________。
A.采用高温 B.采用高压 C.寻找更高效的催化剂
⑵合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l) △H1
H2NCOONH4(氨基甲酸铵) (l) △H1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2
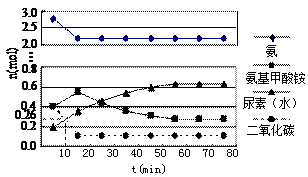 |
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol 氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
图Ⅰ 图Ⅱ
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 ▲ 步反应决定,总反应进行到 ▲ mi n时到达平衡。
n时到达平衡。
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)= ▲ 。
③第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2 ▲ 0(填“>”“<”或“=”)
某温度下,反应N2O4(g)  2NO2(g);(△H>0)在密闭容器中达到平衡.下列说法不正确的是
2NO2(g);(△H>0)在密闭容器中达到平衡.下列说法不正确的是
| A.加压时(体积变小),将使正反应速率增大 |
| B.保持体积不变,加入少许NO2,将使正反应速率减小 |
| C.保持体积不变,加入少许N2O4,再达平衡时颜色变深 |
| D.保持体积不变,升高温度,再达平衡时颜色变深 |
在一定温度下,向一个容积不变的密闭容器中加入 2 molA 和 2 molB ,发生反应:2A(g) + B(g) 3C( g) ΔH=-a kJ/mol(a>0),达到平衡时放出的热量为 bkJ,B的体积分数为ω1%。试回答:
3C( g) ΔH=-a kJ/mol(a>0),达到平衡时放出的热量为 bkJ,B的体积分数为ω1%。试回答:
(1)该反应平衡常数K表达式为________________________。 a与b的关系是a b(填“>”、“<”、“=”)。
(2)若升高温度,平衡常数K__________(填“增大”、“减小”或“不变”,下同),达到平衡时B的体积分数_________。
(3)下列说法中能表明该反应已达到平衡状态的是_________。
| A.温度和体积一定时,容器内压强不再变化 |
| B.温度和体积一定时,某一物质浓度不再变化 |
| C.条件一定,混合气体的平均相对分子质量不再变化 |
| D.温度和压强一定时,混合气体的密度不再变化 |
(4)若向上述平衡体系中再充入1 molB 和3 molC,在相同条件下达到平衡时B的体积分数为ω2 %,则ω1% ω2 % (填“>”、“ =”或“<”),理由是 。
试题篮
()