在一定的温度下, 将 2mol SO2和1mol O2充入一定容积密闭容器中, 在催化剂存在下进行下列反应: 2SO2(g) + O2(g) 2SO3(g) △H="-197" kJ/mol, 当达到平衡状态时, 下列说法中正确的是( )
2SO3(g) △H="-197" kJ/mol, 当达到平衡状态时, 下列说法中正确的是( )
| A.生成 SO3 2 mol | B.放出 197 kJ 的热量 |
| C.吸收197 kJ 的热量 | D.SO2和 SO3共有 2 mol |
在2 L和密闭容器中放入4mol ,发生如下反应:
,发生如下反应: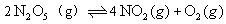 ,反应进行到5min时,测得
,反应进行到5min时,测得 转化了20%,求:
转化了20%,求:
(1)5min时,剩余 的物质的量;
的物质的量;
(2)前5min,v( )为多少;
)为多少;
(3)5min时,O2的物质的量占混合气体总物质的量的百分比。
在一定条件下,对于密闭容器中进行的可逆反应: ,下列说法中,表明这一反应已达到化学平衡状态的是
,下列说法中,表明这一反应已达到化学平衡状态的是
A. 的浓度相等 的浓度相等 |
B.反应停止,正、逆反应速率都等于零 |
C. 在密闭容器中共存 在密闭容器中共存 |
D. 的浓度不再变化 的浓度不再变化 |
下列说法错误的是
| A.化学反应的限度可以通过改变条件而改变 |
| B.可逆反应达到平衡状态时,就是此条件下该反应所能达到的限度 |
C.2mol 与1mol 与1mol 混合一定能生成2mol 混合一定能生成2mol  |
| D.不同可逆反应的反应限度不同 |
一定条件下,可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z起始浓度分别为C1、C2、C3(均不为0),平衡时,X、Y、Z的浓度分别为0.1mol·L-1,0.3 mol·L-1,0.08 mol·L-1,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为C1、C2、C3(均不为0),平衡时,X、Y、Z的浓度分别为0.1mol·L-1,0.3 mol·L-1,0.08 mol·L-1,则下列判断不合理的是
| A.C1∶C2=1∶3 | B.平衡时,Y和Z的生成速率之比为3∶2 |
| C.X、Y的转化率不相等 | D.C1的取值范围为0<C1<0.14 mol·L-1 |
CO和H2在一定条件下可以合成乙醇:2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
CH3CH2OH(g)+H2O(g),下列叙述中能说明上述反应在一定条件下已达到最大限度的是( )
| A.CO全部转化为乙醇 |
| B.正反应和逆反应的化学反应速率均为零 |
| C.CO和H2以1∶2的物质的量之比反应生成乙醇 |
| D.反应体系中乙醇的物质的量浓度不再变化 |
可逆反应N2 + 3H2 2 NH3在一定条件下达到化学反应的限度时,下列判断正确的是
2 NH3在一定条件下达到化学反应的限度时,下列判断正确的是
| A.N2完全转化为NH3 |
| B.反应混合物中,NH3的质量分数不再改变 |
| C.N2、H2与NH3的物质的量之比为1∶3∶2 |
| D.消耗1 mol N2的同时消耗2 mol NH3 |
下列关于化学反应的限度的说法中,正确的是
| A.当可逆反应达到平衡时,这就是这个反应所能达到的限度 |
| B.当可逆反应进行到平衡状态时,那么这个反应的正向反应的速率和逆向反应的速率都为零 |
| C.平衡状态是一种静止的状态,因为反应物和生成物的浓度都不再改变 |
| D.化学反应的限度不可以通过改变反应条件而改变 |
高温下,炼铁高炉中存在下列平衡:FeO(s)+CO(g) 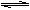 Fe(s)+CO2(g) △H>0
Fe(s)+CO2(g) △H>0
试回答下列问题:
⑴铁在元素周期表中位于 ▲ 周期 ▲ 族。
⑵写出该反应的平衡常数表达式: ▲ ,升高温度,该反应的平衡常数K值将
▲ (填“增大”、“减小”或“不变”,下同),平衡体系中固体的质量将 ▲ 。
⑶为减少高炉冶铁时,含有CO的尾气排放,下列研究方向不可取的是 ▲ 。
| A.其它条件不变,增加高炉的高度 | B.调节还原时的炉温 |
| C.增加原料中焦炭与赤铁矿的比例 | D.将生成的铁水 及时移出 及时移出 |
⑷1100℃时, FeO(s)+CO(g)  Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2g的FeO,同时通入4.48L的CO气体(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为 ▲ 。(精确到0.1%)
Fe(s)+CO2(g),平衡常数K=0.4。今在一密闭容器中,加入7.2g的FeO,同时通入4.48L的CO气体(已折合为标准状况),将其升温到1100℃,并维持温度不变,达平衡时,FeO的转化率为 ▲ 。(精确到0.1%)
在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
| A.从反应开始到平衡,氢气的平均反应速率为0.225mol/(L·min) |
| B.图中交点表示反应达到化学平衡状态 |
| C.升高温度,n(CH3OH)/n(CO2)减小 |
| D.10分钟后向容器再充入1mol CO2和3mol H2,重新达平衡后,CO2体积分数将增大 |
可以证明可逆反应N2(g)+3H2(g) 2NH3(g)已达平衡状态的是:①一个N≡N键断裂的同时,有3个H-H键断裂;②一个N≡N键断裂的同时,有6个N-H键断裂;③其他条件不变时,混合气体的总质量不变;④恒温恒容下的反应,体系压强不再改变;⑤反应体系中反应物和生成物的百分含量都不再改变;⑥恒温恒压下的反应,密度不再改变;⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)( )
2NH3(g)已达平衡状态的是:①一个N≡N键断裂的同时,有3个H-H键断裂;②一个N≡N键断裂的同时,有6个N-H键断裂;③其他条件不变时,混合气体的总质量不变;④恒温恒容下的反应,体系压强不再改变;⑤反应体系中反应物和生成物的百分含量都不再改变;⑥恒温恒压下的反应,密度不再改变;⑦正反应速率v(H2)=0.6mol/(L·min),逆反应速率v(NH3)=0.4mol/(L·min)( )
| A.全部 | B.②④⑤⑥⑦ | C.②③④⑤⑥⑦ | D.③④⑤⑥⑦ |
在一定条件下,可逆反应A(g)+3B(g) 4C(g)达到平衡时,下列叙述正确的是( )
4C(g)达到平衡时,下列叙述正确的是( )
A.此时反应物B全部转化成了生成物
B.单位时间内生成n mol A,同时生成3n mol B
C.若改变条件,A、B、C的浓度有可能再变化
D.A、B、C的分子数比为1:3:4
(14分) 对于反应A(g) 2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。
2B(g) DH>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示。回答下列各题。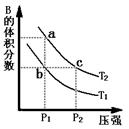
(1)根据曲线图,分析下列说法正确的是 ▲ (填字母) 。
A.a、c两点的反应速率:a 〉c
B.由状态b到状态a,可以通过加热的方法
C.b、c两点A气体的转化率相等
(2)上述反应在密闭容器(定容)中进行,达到平衡状态的标志是 ▲ (填字母) 。
A.单位时间内生成n mol A的同时分解2n molB
B.两种气体的体积分数不再改变
C.v正(A)=2v逆(B)
D.混合气体的密度不再发生变化
E.混合气体的压强不再发生变化
(3)若上述反应达平衡时,B气体的平衡浓度为0.1 mol·L-1,通过减小体积来增大体系的压强(温度保持不变),重新达平衡后,B气体的平衡浓度 ▲ 0.1 mol·L-1(填“〉”、“〈”或“=”)。
(4)在100℃时,将0.40mol的B气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表的数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| n(B)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
| n(A)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
① 在上述条件下,从反应开始至40s时,以A气体表示的该反应的平均反应速率为 ▲ ;
② 上表中n3 ▲ n4(填“〉”、“〈”或“=”),反应A(g) 2B(g)在100℃时的平衡常数K的值为 ▲ ,升高温度后,反应2B(g)
2B(g)在100℃时的平衡常数K的值为 ▲ ,升高温度后,反应2B(g)  A(g)的平衡常数K的值 ▲ (填“增大”、“减小”或“不变”);
A(g)的平衡常数K的值 ▲ (填“增大”、“减小”或“不变”);
③ 若在相同情况下最初向该容器中充入的是A气体,要达到上述同样的平衡状态,A气体的起始浓度为 ▲ mol·L-1。
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示。回答下列问题:
(1)反应开始到10s,用Z表示的反应速率为 ;
(2)反应开始到10s,X的物质的量浓度减少了 ;
(3)反应开始到10s时,Y的转化率为 ;
(4)反应的化学方程式为 。
将4 mol A气体和2 mol B气体在2L的密闭容器中混合并在一定条件下发生反应2A(g)+B(g) 2C(g),2s时测得C的浓度为0.6mol·L-1。下列说法正确的是
2C(g),2s时测得C的浓度为0.6mol·L-1。下列说法正确的是
| A.用物质A表示的平均反应速率为0.3mol/(L·s); |
| B.用物质B表示的平均反应速率为0.6mol/(L·s); |
| C.2 s时物质A的转化率为70%; |
| D.2 s时物质B的浓度为0.35mol·L-1。 |
试题篮
()