将1 mol氧气和一定量的HCl放入2L的密闭容器中,420℃时,在催化剂作用下发生反应:4HCl+O2 2Cl2+2H2O。5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0 mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2 g。
2Cl2+2H2O。5分钟后反应达到平衡,将容器中的混合气体通过过量NaOH溶液,消耗NaOH 2.0 mol;再将剩余气体干燥后通过焦性没食子酸的碱性溶液吸收O2,溶液增重19.2 g。
请回答下列问题:
(1)写出平衡时,混合气体通入NaOH溶液中所发生反应的离子方程式。
(2)计算0~5分钟时,Cl2的平均生成速率是多少。
(3)计算平衡时HCl的转化率。
一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)  Y(g)+Z(s),以下能说明作为反应达到平衡标志的是
Y(g)+Z(s),以下能说明作为反应达到平衡标志的是
| A.X的分解速率与Y的消耗速率相等 |
| B.反应容器中压强不再变化 |
| C.混合气体的密度不再变化 |
| D.单位时间内生成lmolY的同时分解2mol X |
将0.6 mol A和0.5 mol B充入0.4L密闭容器中发生2A(g)+B(g)  mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2 mol。又知5min内用E表示的平均反应速
mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2 mol。又知5min内用E表示的平均反应速
率为0.1 mol·L-1·min-1,下列结论正确的是( )
A.A、B的转化率均为20%
B.m值为1
C.5min内用A表示的平均反应速率为0.1 mol·L-1·min-1
D.平衡时混合物总物质的量为1 mol
可逆反应,C(s)+H2O CO(g)+H2(g);△H>0,下列说法正确的是( )
CO(g)+H2(g);△H>0,下列说法正确的是( )
| A.达到平衡时,反应物的浓度和生成物的浓度相等 |
| B.达到平衡时,反应物和生成物的浓度不随时间的变化而变化 |
| C.由于反应前后分子数相等,所以增加压力对平衡没有影响 |
| D.加入正催化剂可以加快反应达到平衡的速度 |
把6molA和5molB两气体通入容积为4L的密闭容器中,一定条件下反应:
3A(g)+B(g) 2C(g)+xD(g);△H<0,5min达平衡,此时生成2molC,测得D的平均反应速率为0.1mol·(L·min)-1。下列说法中正确的是 ( )
2C(g)+xD(g);△H<0,5min达平衡,此时生成2molC,测得D的平均反应速率为0.1mol·(L·min)-1。下列说法中正确的是 ( )
| A.降低平衡体系的温度,逆反应速率变小,正反应速率增大,平衡正向移动 |
| B.恒温下达到平衡的标志是C和D的生成速率相等 |
| C.A的平均反应速率为0.15mol·(L·min)-1 |
| D.B的转化率为25% |
在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4(s) 时刻测得各物质的浓度如表。据此下列结论正确的是
A.在t3时刻反应已经停止 B.A的转化率比B的转化率低
C.在容器中发生的反应为:
D.在t2~t3内A的平均反应速率为[1/(t3-t2)]mol/(L·s)
在体积不变的密闭容器中发生的反应是CO(g)+H2O(g) CO2(g)+H2(g)下列情况中,能说明该反应达到化学平衡状态的是
CO2(g)+H2(g)下列情况中,能说明该反应达到化学平衡状态的是
| A.混合气体的密度不再改变 | B.混合气体的质量不再改变 |
| C.混合气体的物质的量不再改变 | D.CO的浓度不再改变 |
一定条件下,反应 ,下列哪一种状态可能没有达到化学反应限度:
,下列哪一种状态可能没有达到化学反应限度:
| A.速率比:V(NO2):V(NO):V(O2)=2:2:l时的状态 |
| B.混合气体的平均相对分子质量保持不变时的状态 |
| C.生成NO2的速率与生成O2的速率比等于2:l时的状态 |
| D.体系中的颜色保持不变时的状态 |
在一定温度下的密闭容器中存在如下反应:2SO2(g)+ O2 (g) 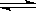 2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)
2SO3(g),已知c始(SO2)=0.4mol/L,c始(O2)=1mol/L,经测定该反应在该温度下的平衡常数K=19。判断:当SO2转化率为50%时,该反应是否达到平衡状态,若未达到,向哪个方向进行?(要求写出计算过程)
在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)  CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K与温度t的关系如下表:
| t/℃ |
700 |
800 |
830 |
1000 |
1200 |
| K |
0.6 |
0.9 |
1.0 |
1.7 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(填“吸热”“放热”)。
t℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A (g)+B (g) x C(g),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
x C(g),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)v(B) = mol/(L·min),v(C) = mol/(L·min),x= 。
(2)比较达到平衡时,A、B两反应物的转化率之比为α(A):α(B)= ;
(3)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是____________(填写字母序号)
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
一定温度下将amolPCl5通入一个容积不变的反应器中,达到如下平衡:PCl5 PCl3+Cl2测得压强为P1,此时向反应器中再通入amolPCl5,在温度不变的情况下再度达到平衡,测得压强为P2。则P1和P2的关系是( )
PCl3+Cl2测得压强为P1,此时向反应器中再通入amolPCl5,在温度不变的情况下再度达到平衡,测得压强为P2。则P1和P2的关系是( )
| A.2P1>P2 | B.2P1=P2 | C.2P1<P2 | D.无法判断 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
下列说法错误的是高( )
| A.反应达到平衡时,X的转化率为50% |
B.上述反应为X+3Y  2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.增大压强使平衡向生成Z的方向移动,平衡常数不变 |
| D.若改变温度反应的平衡常数变大,则一定为升高温度 |
在一定温度的定容密闭容器中,反应A2(g)+B2(g) 2AB(g)达到平衡状态的是( )
2AB(g)达到平衡状态的是( )
| A.混合气体的密度不再改变 |
| B.容器内的总压强不随时间而变化 |
| C.单位时间内生成2n mol AB的同时,生成n mol的B2 |
| D.A2、B2、AB的分子数之比为1:1:2时 |
试题篮
()