右图是某反应体系中的三种气态物质M、N、P的物质的量浓度随时间的变化情况,则下列判断不正确的是 ( )
A.该反应的化学方程式可表达为2M+N 2P 2P |
| B.在反应时间为20min—25min之内,物质 M的反应速率为0.002mol/(L·min) |
| C.当反应时间为20min时,曲线开始发生变化 的原理可能是由于增大压强引起的 |
| D.反应在10min达到化学平衡状态,若曲线的 |
变化是由于升温造成的(其它条件不变),
则该反应的正反应一定为吸热反应
在一定温度下,把2 mol SO2和1mol O2通入一个一定容积的密闭容器里,发生如下反应:
2SO2(g)+O2(g)  2SO3(g)
2SO3(g)
当此反应进行到一定程度时,反应混合物就处于平衡状态,现在该容器中维持温度不变,令a、b、c分别代表初始加入的SO2、O2、SO3的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能保证平衡时反应混合物中3种气体的百分含量,仍跟上述平衡时完全相同,请填写下列空白:
(1)若a=0,b=0,则c=___________;
(2)若a=0.5,则b=___________和c=___________;
(3)a、b、c取值必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b和c):___________。
如右图所示,一定条件下将1mol A2气体和3molB2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1所示。在恒温恒压下发生如下反应:A2+3B2 2AB3。当反应达到平衡时,活塞位置如图2所示,则平衡时A的转化率是

| A.20% | B.40% | C.60% | D.无法确定 |
X,Y,Z三种气体,把a molX和b molY充入一密闭容器中,发生反应:X+2Y 2Z达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为( )
2Z达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为( )
A. |
B. |
C. |
D. |
T℃时,将3mol气体A和1mo1气体B通入容积为2L且固定不变的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
(1)从反应开始到平衡状态,生成C的平均速率为 ;X= ;
(2)若向原平衡混合物的容器中再充入amolC,在T℃达到新的平衡,此时B的物质的量为n(B)= ;
(3)保持温度和容积不变,对原平衡混合物中三者的物质的量作如下调整,可使平衡
向右移动的是 ;
A.均减半 B.均加倍 C.均增加0.4mol D.均减少0.4mol
(4)若上述可逆反应的热化学方程式为:
3A(g)+B(g)  xC(g) ;△H =-QKJ/mol (Q>0)
xC(g) ;△H =-QKJ/mol (Q>0)
①若可逆反应达到平衡后升高体系温度,正反应速率 (填“增大”、“减小”或“不变”),平衡将 (填“左移”、“右移”或“不移动”)
②若可逆反应达到平衡后增大压强,则体系温度将 (填“升高”、“降低”或“不变”)
③若可逆反应达到平衡后,加入A,则△H (填“变大”、“变小”或“不变”
一定条件下,在体积为3 L的密闭容器中反应CO(g)+ 2H2(g) CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
(1)该反应的平衡常数表达式K= ;根据右图,升高温度,K值将 (填“增大”、“减小”或“不变”)。
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是 (用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是 (填字母)。
a. v生成(CH3OH)= v消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d. CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母)。
a.c(H2)减少 b正反应速率加快,逆反应速率减慢
c. CH3OH的物质的量增加 d.重新平衡时c(H2)/ c(CH3OH)减小
(14 分)在T1℃时,向容积为2 L 的密闭容器甲中加人1mol N1、3mol H2及少量固体催 化剂,发生反应N2(g) + 3H2(g)  2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
(1) 该反应在0 ~l0min 时间内H2的平均反应速率为______,N2的转化率为______。 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
a.大于25% b.等于25% c.小于25%
(3)右图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T1>T2)时H2的体积分数随时间t的变化曲线。
(4)若保持T1℃,在体积也为2 L 的密闭容器乙中通入一定量的N2、H2、NH3,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入H2的物质的量x的取值范围是____________。
如右图所示,某刚性容器内有一活塞和弹簧,B内为真空,A内已充入2 mol SO2和1 mol O2,在一定条件下发生可逆反应2SO2+O2 2SO3;ΔH<0,此时活塞已保持静止,SO2反应速率为v0。再往A内迅速充入2 mol SO2和1 mol O2,当活塞再次保持静止时,SO2反应速率为v,在此过程中,下列说法正确的是
2SO3;ΔH<0,此时活塞已保持静止,SO2反应速率为v0。再往A内迅速充入2 mol SO2和1 mol O2,当活塞再次保持静止时,SO2反应速率为v,在此过程中,下列说法正确的是
| A.活塞先下移,后上移到原静止位置,v>v0 |
| B.活塞先下移,后上移到原静止位置,v=v0 |
| C.活塞先下移,后上移,不到原静止位置,v>v0 |
| D.活塞先下移,后上移,不到原静止位置,v=v0 |
在一密闭容器中通入一定量SO2和O2两种气体,在一定条件下反应:2SO2(气)+O2(气) 2SO3(气);△H<0,当达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是: ( )
2SO3(气);△H<0,当达到平衡后,改变一个条件(x),下列量(y)一定符合图中曲线的是: ( )
| A.x为压强,y为SO2的浓度; |
| B.x为温度,混合气体平均相对分子质量; |
| C.x为加入SO2的量,y为O2的转化率; |
| D.x为改变容器的体积,y为SO3的百分含量; |
已知可逆反应A(g) + 3B(g)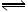 2C(g) ;△H>0中,为了使原料B的充分利用,应采取的反应条件是 ( )
2C(g) ;△H>0中,为了使原料B的充分利用,应采取的反应条件是 ( )
| A.高温、高压 | B.高温、低压 | C.低温、低压 | D.低温、高压 |
在一定温度下,体积不变的密闭容器中有可逆反应A(g) + B(g) 2C(g) + D(s) ,可以判断反应达到平衡是( )
2C(g) + D(s) ,可以判断反应达到平衡是( )
| A.单位时间内反应n molB,同时生成2n molC; | B.容器内气体的物质的量不再变化; |
| C.A的生成速率与B的生成速率相等;; | D.容器内气体的密度不再变化; |
一定温度下,有可逆反应:2X(g)+2Y(g) Z(g)+3P(g);ΔH<0。现将2molX和2molY充入体积为V的甲容器,将2molZ和6molP充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同。下列说法正确的是()
Z(g)+3P(g);ΔH<0。现将2molX和2molY充入体积为V的甲容器,将2molZ和6molP充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同。下列说法正确的是()
| A.向甲容器中再充入2molX和2molY,平衡后甲中物质Z的浓度不变 |
| B.甲、乙两容器中的反应达到化学平衡时,Z的体积分数相等 |
| C.甲、乙两容器中的反应达到化学平衡时,乙容器内压强大 |
| D.向乙容器中再充入1molZ和3molP,平衡后乙中物质Z的浓度为原来的1.5倍 |
已知H2(g)+I2(g)  2HI(g);△H<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
2HI(g);△H<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
| A.甲升高温度,乙不变 |
| B.甲中加入0.1molHe,乙不变 |
| C.甲、乙提高相同温度 |
| D.甲增加0.1molH2,乙不变 |
某温度下,在容积为2L的密闭容器中,发生X(g)+2Y(g)  2W(g)的反应,充入1molX和1molY,经20s达到平衡时生成了0.4molW。下列说法正确的是
2W(g)的反应,充入1molX和1molY,经20s达到平衡时生成了0.4molW。下列说法正确的是
| A.若升高温度,W的体积分数减小,则该反应△H>0 |
| B.以Y的浓度变化表示的反应速率为0.01mol/(L.s) |
| C.在其它条件不变的情况下,增加1molX,则X和Y的转化率均提高 |
| D.增大压强,正反应速率增大,逆反应速率减小,则平衡向正反应方向移动 |
试题篮
()