一定条件下,通过下列反应可实现燃煤烟气中硫的回收,其中Y是单质。
SO 2(g) + 2CO(g) 2X(g)+Y(l)
2X(g)+Y(l)
为了测定在某种催化剂作用下的反应速率,在某温度下用超灵敏气体传感器测得不同时间的SO2和CO浓度如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
| c(SO2)/mol·L-1 |
1.00 |
0.50 |
0.23 |
3.00×10-37 |
3.00×10-37 |
| c(CO)/mol·L-1 |
4.00 |
3.00 |
2.46 |
2.00 |
2.00 |
下列说法不正确的是
A.X的化学式为CO2
B.前1s内v(X)=" 1.00" mol·L-1·s-1
C.该回收原理运用了SO2的还原性
D.该温度下,此反应的平衡常数的数值是3.33×1036
某温度下,碳和H2O(g)在密闭容器里发生下列反应:
①C(s)+H2O(g) CO(g)+H2(g),
CO(g)+H2(g),
②CO(g)+H2O(g) CO2(g)+H2(g),
CO2(g)+H2(g),
当反应达到平衡时,c(H2)=1.9mol•L-1、c(CO)=0.1mol•L-1。
则下列叙述正确的是
| A.CO在平衡时转化率为10% |
| B.平衡浓度c(CO2)=c(H2) |
| C.其他条件不变时,缩小体积,反应②平衡不移动 |
| D.平衡时增大碳的质量,反应①中热量值不变 |
在密闭容器中通入NO和CO各2mol发生反应: 2NO(g)+ 2CO(g) 2CO2(g)+ N2(g)
2CO2(g)+ N2(g)
容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如下图所示。
以下说法合理的是
| A.温度T2>T1 |
| B.压强P2>P1 |
| C.II曲线表示NO平衡转化率为25% |
| D.该反应的焓变△H<0 |
某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A + 3B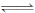 2C,若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中C气体的体积占 10%,下列推断正确的是
2C,若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中C气体的体积占 10%,下列推断正确的是
①原混合气体的体积为1.2VL
②原混合气体的体积为1.1VL
③反应达平衡时,气体A消耗掉0.05VL
④反应达平衡时,气体B消耗掉0.05V L
| A.②③ | B.②④ | C.①③ | D.①④ |
一定条件下,在体积恒定的密闭容器中加入1 mol N2和3 mol H2发生反应:
N2(g)+ 3H2(g) 2NH3(g)△H<0 。下列有关说法正确的是
2NH3(g)△H<0 。下列有关说法正确的是
| A.降低温度可以加快反应速率 |
| B.达到化学反应限度时,生成2mol NH3 |
| C.1mol N2和3mol H2的总能量低于2mol NH3的总能量 |
| D.向容器中再加入N2可加快正反应速率 |
下列关于化学反应限度的说法正确的是
| A.当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 |
| B.当一个可逆反应进行到平衡状态时,这个反应的正向反应速率和逆向反应速率相等 |
| C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变 |
| D.化学反应的限度不可以通过改变条件而改变 |
关于可逆反应达到平衡状态的说法错误的是
| A.外界条件不能改变平衡状态 |
| B.达平衡时正、逆反应速率相等 |
| C.各组分的含量不随时间而变化 |
| D.是动态平衡 |
在一定温度下,下列叙述不是可逆反应A(g)+3B(g) 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
(1)C的生成速率与C的分解速率相等;(2)单位时间内amol A生成,同时生成3amol B;(3)A、B、C的浓度不再变化;(4)体积不变得密闭容器中混合气体的总压强不再变化;(5)混合气体的物质的量不再变化;(6)单位时间消耗amol A,同时生成3amol B;(7)A 、B、C的分子数目比为1:3:2。
A.(2)(5) B.(1)(3) C.(2)(7) D.(5)(6)
可逆反应N2+3H2 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是
| A.3 v正(N2)= v正(H2) | B.v正(N2)= v逆(NH3) |
| C.2 v正(H2)= 3v逆(NH3) | D.v正(N2)= 3v逆(H2) |
一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)  Y(g)+Z(g),达到反应限度的标志是
Y(g)+Z(g),达到反应限度的标志是 ①X的分解速率与X的生成速率相等
①X的分解速率与X的生成速率相等
②反应容器中压强不再变化 ③X、Y、Z的浓度不再变化
③X、Y、Z的浓度不再变化
④单位时间内生成l molY的同时生成l mol Z
| A.①③ | B.②③ | C.①② | D.②④ |
下图是可逆反应X2 + 3Y2 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是:
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是:
| A.t1时,只有正方向反应 |
| B.t2时,反应未到达最大限度 |
| C.t2- t3,反应不再发生 |
| D.t2- t3,各物质的浓度不再发生变化 |
一定条件下,可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.08mol•L﹣1,则下列判断不正确的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol•L﹣1、0.3mol•L﹣1、0.08mol•L﹣1,则下列判断不正确的是
| A.c1:c2的值不能确定 |
| B.平衡时,Y和Z的生成速率之比为3:2 |
| C.0.28mol•L﹣1<c1+c2+c3<0.56mol•L﹣1 |
| D.c1的取值范围为0<c1<0.14mol•L﹣1 |
对一定温度下的恒容容器中的可逆反应A(g)+3B(g) 2C(g),下列叙述不能作为平衡标志的是
2C(g),下列叙述不能作为平衡标志的是
①C的生成速率与C的分解速率相等
②单位时间内生成amol A,同时生成3amol B
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amol A,同时生成3amol B
⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①⑥ C.②④ D.③⑧
可逆反应:2NO2(g) 2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状态的标志是
①单位时间内生成nmol O2的同时生成2nmol NO2
②单位时间内生成nmol O2的同时生成2nmol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
| A.①③④ | B.②③⑤ | C.①④ | D.①③④⑤ |
试题篮
()