t℃时,将3molA和2molB气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A (g)+B (g) x C(g),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
x C(g),2min时反应达到平衡状态(温度不变),剩余1.8molB,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)v(B) = mol/(L·min),v(C) = mol/(L·min),x= 。
(2)比较达到平衡时,A、B两反应物的转化率之比为α(A):α(B)= ;
(3)若继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,下列说法中正确的是____________(填写字母序号)
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不会发生移动 D.正、逆反应的化学反应速率保持不变
工业上利用反应:CO(g)+H2O(g) CO2(g)+H2(g) △H=Q kJ·mol―1,制备H2 。已知该反应的平衡常数K与温度的关系如图所示。
CO2(g)+H2(g) △H=Q kJ·mol―1,制备H2 。已知该反应的平衡常数K与温度的关系如图所示。

若在一容积固定的密闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系
如下表:
| t/min |
CO(g) |
H2O(g) |
CO2(g) |
H2(g) |
| 0 |
0.200 |
0.300 |
0 |
0 |
| 2 |
0.138 |
0.238 |
0.062 |
0.062 |
| 3 |
c1 |
c2 |
c3 |
c4 |
| 4 |
c1 |
c2 |
c3 |
c4 |
已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是 。
| A.单位时间内减少CO(g)的浓度等于生成CO2(g)的浓度 |
| B.反应容器内的压强不发生变化 |
| C.混合气体中H2(g)的浓度不再发生改变 |
| D.氢气的生成速率等于水的消耗速率 |
(2)Q 0(填“>”、“=”或“<”)。
(3)若在850℃时向反应容器中充入H2O(g),K值 (填“增大”、“减小”或“不变”)。
(4)达平衡时CO2的反应速率 ,CO(g)的转化率为 。
一氧化碳与水蒸气的反应为CO(g) + H2O(g) 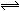 CO2(g) + H2(g)在密闭容器中,将1.0 mol CO与1.0mol H2O混合加热到434℃,在434℃的平衡常数K1 =9
CO2(g) + H2(g)在密闭容器中,将1.0 mol CO与1.0mol H2O混合加热到434℃,在434℃的平衡常数K1 =9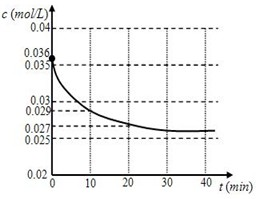
(1)跟踪测定H2O的物质的量浓度,如图所示,则0 —20 min ,H2O的反应速率是
(2)请在图中用实线绘制出在该温度下加入正催化剂后,H2O的物质的量浓度变化图线。
(3)从434℃升温至800℃,800℃的平衡常数K2 =1,则正反应为_____________(填“放
热反应”或“吸热反应”或“不能确定”)。
(4)求在800℃反应达平衡时,CO转化为CO2的转化率(写出必要的计算过程)
尿素(H2NCONH2)是一种非常重要的高氮化肥,工业上合成尿素的反应如下:
2NH3(l)+CO2(g) H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
H2O(l)+H2NCONH2 (l) △H=-103.7 kJ·mol-1
试回答下列问题:
⑴下列措施中有利于提高尿素的产率的是___________。
A.采用高温 B.采用高压 C.寻找更高效的催化剂
⑵合成尿素的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4(氨基甲酸铵) (l) △H1
H2NCOONH4(氨基甲酸铵) (l) △H1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l) △H2
H2O(l)+H2NCONH2(l) △H2
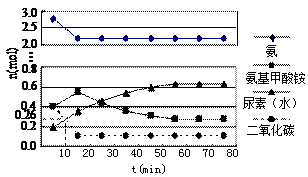 |
某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol 氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下图Ⅰ所示:
图Ⅰ 图Ⅱ
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 ▲ 步反应决定,总反应进行到 ▲ mi n时到达平衡。
n时到达平衡。
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)= ▲ 。
③第二步反应的平衡常数K随温度的变化如上右图Ⅱ所示,则△H2 ▲ 0(填“>”“<”或“=”)
如图所示,600K时,在容积可变的透明容器内,反应2HI(气)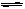 I2(气)+H2(气)达到平衡状态A。保持温度不变,将容器的容积压缩成为原容积的一半,达到平衡状态B。按图示观察方向__▲__(填“能”或“不能”)看出两次平衡时容器内颜色深浅的变化,理由是_▲__。若从水平方向观察,能否看到容器内颜色深浅的变化__▲___。
I2(气)+H2(气)达到平衡状态A。保持温度不变,将容器的容积压缩成为原容积的一半,达到平衡状态B。按图示观察方向__▲__(填“能”或“不能”)看出两次平衡时容器内颜色深浅的变化,理由是_▲__。若从水平方向观察,能否看到容器内颜色深浅的变化__▲___。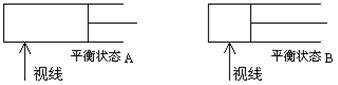
工业废水中常含有一定量的Cr2O72—和CrO42—,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为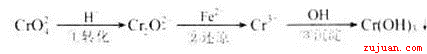
其中第①步存在平衡:2CrO42—(黄色)+2H+ Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显 色.
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72—和CrO42—的浓度相同 b.2v (Cr2O72—) ="v" (CrO42—) c.溶液的颜色不变
(3)第②步中,还原1mol Cr2O72—离子,需要________mol的FeSO4·7H2O。
( 4 ) 第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+ (aq)+3OH—(aq)
Cr3+ (aq)+3OH—(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH—)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
方法2:电解法
该法用Fe做电极电解含Cr2O72—的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
已知:化合物B、C、E中含有两种相同的元素,A可用于玻璃、洗涤剂等的生产,B可用于制作光纤,G的组成元素与D相同。这些化合物之间存在下图所示的转化关系。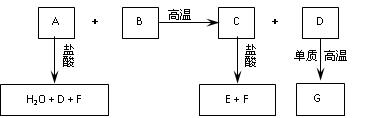
请回答:
(1)在化合物A、C、F中含有的 相同元素 。
相同元素 。
(2)化合物C的化学式为 ,其水溶液的pH 7(填“>”或“<”) 。
。
(3) 700 ℃时,向容积为 2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
G(g)+H2O(g)  D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
| 反应时间/min |
n(G)/mol |
n(H2O)/ mol |
| 0 |
1.20 |
0.60 |
| t1 |
0.80 |
|
| t2 |
|
0.20 |
① 反应在t1min内的平均速率为v(H2)= mol/(L·min)
② 保持其他条件不变,起始时向容器中充入0.60 mol G和1.20 mol H2O,到达平衡时,
n(D)= mol。
③ 温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO (g)  Fe(s)+ CO2(g) △H>0
Fe(s)+ CO2(g) △H>0
(1)此反应的平衡常数表达式为:K=
(2)温度升高,达到新的平衡后,高炉内CO2与CO的体积比 (填“增大”、 “减小”或“不变”)。
(3)已知1100℃时,K= 0.263。某时刻测得高炉中c(CO2)=" 0.025" mol·L-1,c(CO)=" 0.1" mol·L-1,在这种情况下,该反应 (填“是”或“不是”)处于化学平衡状态。
如果“不是”,此时化学反应向 方向进行(填“正反应”或“逆反应”)。如果“是”,此空不填
(1)对反应N2O4(g) 2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1 T2(填“>”、“<”或“=”);A、C两点的速率vA vC(
2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1 T2(填“>”、“<”或“=”);A、C两点的速率vA vC( 同上)。
同上)。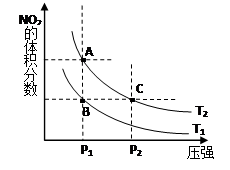
(2)在100℃时,将0.400mol的NO2气体充入2L真空定容密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| n(NO2)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
| n(N2O4)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
①在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为 ;
②该反应的平衡常数K的值为 ;
③若在相同情况下最初向该容器充入的是N2O4,要达到上述同样的平衡状态,N2O4的起始浓度是 mol/L。
④计算③中条件下达到平衡后混合气体的平均相对分子质量为 ;(结果保留小数点后一位)
在一个容积为500mL的密闭容器中,充入5molH2和2molCO。在一定温度,一定压强下,发生如下反应:2H2(g)+CO(g)  CH3OH(g),经过5min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,以H2的浓度变化表示的该反应的速率 ;平衡混合气的密度与相同状况下的氢气密度之比 。
CH3OH(g),经过5min后达到平衡状态。若此时测得CH3OH蒸气的浓度为2mol/L,以H2的浓度变化表示的该反应的速率 ;平衡混合气的密度与相同状况下的氢气密度之比 。
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
请填空:
(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g) △H>0。
CO(g)+3H2(g) △H>0。
在其它条件不变的情况下降低温度,逆反应速率将 (填“增大”、“减小”或“不变”)。将1.0molCH4和2.0molH2O通入反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)= 。
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为 。
(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g) +2H2(g)  CH3OH(g),CO的平衡转化率与温度、压强的关系如右图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如右图所示,则:
① P1 P2 (填“<”、“>”或“=")。
②在其它条件不变的情况下,反应室3再增加amolCO与2amolH2,达到新平衡时,CO的转化率______(填“增大”、“减小”或“不变”。下同。),平衡常数 。
③在P1压强下,100℃时,CH3OH(g)  CO(g) + 2H2(g)反应的平衡常数为
CO(g) + 2H2(g)反应的平衡常数为
(用含a、V的代数式表示)。
(8分)有两只密闭的容器A和B,A能保持恒压,B能保持恒容。起始时向容积相等的两容器中通入体积比为2:l的等量的S02和02,使之发生反应: 2S02 +02 2S03,并达到平衡。则(填<、=、>;左、右;增大、减小、不变)
2S03,并达到平衡。则(填<、=、>;左、右;增大、减小、不变)
(1)达到平衡所需的时间:tA tB,S02的转化率:aA aB。
(2)起始时两容器中的反应速率:vA_______vB,反应过程中的反应速率:vA______vB
(3)达到平衡时,向两容器中分别通入等量的氩气。A容器中的化学平衡向 反应方向移动,B容器中的化学反应速率
(4)达到平衡后,向两容器中分别通入等量的原反应气体,再次达到平衡时,A容器中的S02的百分含量 ,B容器中S02的百分含量 。
(每空2分共8分)
向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气体共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
①.若a=0,b=0,则c=
②.若a=0.7,b=2.1,则:
Ⅰ.c= .
Ⅱ.这时反应向 进行.
Ⅲ.若要维持反应开始向该反应方向进行,c的范围是
Ⅰ.在一定条件下,xA+yB zC,达到平衡,试填写下列空白:
zC,达到平衡,试填写下列空白:
(1)已知C是气体,且x+y=z,加压时平衡如果发生移动,则平衡必向 方向移动。
(2)若B、C是气体,其他条件不变时增加A的用量,平衡不移动,则A的状态为 。
Ⅱ.已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如下图。
N2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为2L的恒温密闭玻璃容器中,反应物浓度随时间变化关系如下图。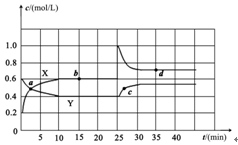
(1)图中共有两条曲线X和Y,其中曲线 表示NO2浓度随时间的变化;
a、b、c、d四个点中,表示化学反应处于平衡状态的点是 。
下列不能说明该反应已达到平衡状态的是 。
A.容器内混合气体的压强不随时间变化而改变
B.容器内混合气体的密度不随时间变化而改变
C.容器内混合气体的颜色不随时间变化而改变
D.容器内混合气体的平均分子量不随时间变化而改变
(2)前10min内用NO2表示的化学反应速率v(NO2)= 。
(3)反应25min时,若只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是 (用文字表达);
(4)若要达到使NO2(g)的百分含量与d点相同的化学平衡状态,在25min时还可以采取的措施是 。
A.加入催化剂 B.缩小容器体积 C.升高温度 D.加入一定量的N2O4
将1mol CO和1mol H2O充入某固定容积的反应器中,在某条件下达到平衡:CO+H2O(g)?CO2+H2,此时有2/3的CO转化为CO2。
(1)该平衡混合物中CO2的体积分数为__________。
(2)若在相同条件下,向容器中充入1mol CO2、1mol H2和1mol H2O,则达到平衡时与(1)中平衡相比较,平衡应向__________(填“正反应方向”、“逆反应方向”或“不”)移动,此时平衡混合物中CO2的体积分数可能是下列各值中的__________
| A.22.2% | B.27.55% | C.33.3% | D.36.8% |
(3)结合(2)中计算结果分析若平衡向正反应方向移动时,则下列说法中正确的是__________。
①生成物的产量一定增加;②生成物的体积分数一定增加;③反应物的转化率一定增大;④反应物的浓度一定降低;⑤正反应速率一定大于逆反应速率;⑥一定使用了催化剂
试题篮
()