在一定条件下,反应N2+3H2 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g, 则反应速率为( )
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g, 则反应速率为( )
| A.V(H2)=0.03mol/(L·min) | B.V(N2)="0.02mol/(L·min)" |
| C.V(NH3)=0.17mol/(L·min) | D.V(NH3)=0.01mol/(L·min) |
关于化学反应速率的说法正确的是
| A.化学反应速率可表示可逆反应进行的程度 |
| B.化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
| C.对于任何化学反应来说,反应速率越快,反应现象就越明显 |
| D.根据反应速率的大小可知化学反应进行的相对快慢 |
20mL 0.5mol/L的盐酸与一块大理石反应,下列措施不能提高反应速率的是
| A.加入10mL 1mol/L的盐酸 | B.加入30mL 10mol/L的盐酸 |
| C.所用的大理石研磨成粉末 | D.加入10mLH2O |
影响化学反应速率的因素有多方面,如浓度、压强、温度、催化剂等。下列有关说法不正确的是( )
| A.改变压强能改变气体反应的速率 |
| B.增大浓度能加快化学反应速率,原因是增大浓度就增加了反应体系中活化分子的百分数 |
| C.温度升高使化学反应速率加快的主要原因是增加反应体系中活化分子的百分数 |
| D.催化剂能加快化学反应速率主要原因是降低反应所需的能量 |
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol·L-1·s-1
B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1
D.v(D)=1.6 mol·L-1·min-1
下列关于化学理论学习和研究的说法错误的是
| A.化学键的变化不一定会引起化学反应的变化 |
| B.外界条件改变一定会引起化学反应的快慢变化 |
| C.化学模型的建立有助于解释一些化学现象 |
| D.化学基本原理的应用是建立在有一定条件的基础上的 |
运用相关化学知识进行判断,下列结论错误的是
| A.某吸热反应能自发进行,因此该反应是熵增反应 |
| B.NH4F 水溶液中含有 HF,因此 NH4F 溶液不能存放于玻璃试剂瓶中 |
| C.可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成 H2 的速率 |
使反应4NH3(g)+3O2(g)⇌2N2(g)+6H2O在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol.此反应的平均速率v(X)为
| A.v(NH3)="0.02" mol•L﹣1•s﹣1 | B.v(O2)="0.01" mol•L﹣1•s﹣1 |
| C.v(N2)="0.02" mol•L﹣1•s﹣1 | D.v(H2O)="0.02" mol•L﹣1•s﹣1 |
在2A(g)+B(g)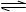 3C(g)+4D(g)反应中表示该反应速率最快的是 ( )
3C(g)+4D(g)反应中表示该反应速率最快的是 ( )
A.v(A)="0.5mol/(L·" s) B.v(B)="0.3mol/(L·" s)
C.v(C)="0.8mol/(L·" s) D.v(D)="1mol/(L·" s)
下列说法一定正确的是
A.反应A(s)  2B(g) + C(g),当C的体积分数不变时,反应达到平衡状态 2B(g) + C(g),当C的体积分数不变时,反应达到平衡状态 |
| B.将钢闸门与直流电源的正极相连,可防止钢闸门腐蚀 |
| C.用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+ Hg2+(aq)=HgS(s)+Fe2+(aq) |
| D.增大反应物浓度可加快反应速率,因此可用浓硫酸与铁反应增大生成氢气的速率 |
在体积均为1.0L的恒容密闭容器中加入足量的相同的炭粉,再 分别加入0.1molCO2和
0.2molCO2,在不同温度下反应CO2(g)+C(s) 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )

| A.体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) |
B.反应CO2(g)+C(s) 2CO(g)的△S>0、△H<0 2CO(g)的△S>0、△H<0 |
| C.体系的总压强P总:P总(状态Ⅱ)<2P总(状态Ⅰ) |
| D.逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ) |
在一个容积不变的密闭容器中,发生反应:2NO(g)+O2(g) 2NO2(g)
2NO2(g)

(1)当n(NO):n(O2)=4:1时,O2的转化率随时间的变化关系如下图所示。
①A点的逆反应速率v逆 (O2)_____B点的正反应速率v正(O2)(填“大于”、“小于”或“等于” )。
②NO的平衡转化率为______;当达到B点后往容器中再以4:1 加入些
NO和 O2,当达到新平衡时,则NO的百分含量 B点NO的百分含量(填“大于”、“小于”或“等于” )。
③到达B点后,下列关系正确的是( )
| A.容器内气体颜色不再变化 |
| B.v正(NO)="2" v正(O2) |
| C.气体平均摩尔质量在此条件下达到最大 |
| D.容器内气体密度不再变化 |
(2)在下图1和图2中出现的所有物质都为气体,分析图1和图2,可推测:4NO(g)+3O2(g)=2N2O5(g)△H= 。


(3)降低温度,NO2(g)将转化为N2O4(g),以N2O4、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨I电极反应生成一种氧化物Y,Y为 ,有关石墨I电极反应式可表示为: 。
可逆反应2SO2(g)+O2(g) 2SO3(g),在不同条件下测得化学反应速率最快的为
2SO3(g),在不同条件下测得化学反应速率最快的为
| A.v(O2)=3 mol·L-1·min-1 |
| B.v (SO2) =4 mol·L-1·min-1 |
| C.v (SO3) =0.1 mol·L-1·s-1 |
| D.v (O2) =0.1 mol·L-1·s-1 |
将5.6g铁粉投入100mL2mol/L的稀硫酸中,2min时铁刚好完全溶解(忽略溶液体积变化)。下列有关这个反应的反应速率表示正确的是( )
| A.铁的反应速率为0.5mol/(L·min) | B.硫酸的反应速率为0.5mol/(L·min) |
| C.硫酸亚铁的反应速率为0.5mol/(L·min) | D.氢气的反应速率为0.5mol/(L·min) |
试题篮
()