一定条件下,反应N2(g)+3H2(g) 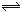 2NH3(g)在10L的密闭容器中进行,测得2min内N2的物质的量由20mol减小到8mol,则2min内用NH3表示的反应速率为
2NH3(g)在10L的密闭容器中进行,测得2min内N2的物质的量由20mol减小到8mol,则2min内用NH3表示的反应速率为
| A.1.2mol/(L·min) | B.6.0mol/(L·min) |
| C.0.6mol/(L·min) | D.0.4mol/(L·min) |
把4mol A和2.5mol B混合于2L密闭容器中,发生反应:3A(g)+2B(s)  xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol•L-1•min-1,下列结论错误的是
xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol•L-1•min-1,下列结论错误的是
| A.A的平均反应速率为0.15 mol•L-1•min-1 |
| B.平衡时,C的浓度为0.25mol•L-1 |
| C.B的平均反应速率为0.1 mol•L-1•min-1 |
| D.平衡时,容器内压强为原来的0.875倍 |
下列说法错误的是
| A.决定化学反应速率的主要因素是参加反应的物质的性质 |
| B.升高温度可使吸热反应的反应速率增大,使放热反应的反应速率减小 |
| C.对于有气体参加的反应,增大压强,反应速率加快 |
| D.催化剂能增大单位体积内活化分子的百分数,从而增大化学反应速率 |
反应A(g)+3B(g) 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
A.v(C)=0.04mol·(L·s)-1 B.v(B)=0.06mol·(L·s)-1
C.v(A)=0.03mol·(L·s)-1 D.v(D)=0.01mol·(L·s)-1
2A(g)+B(g)  3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是
A.V(A) = 0.7mol·L-1·min-1 B.V(B) = 0.3mol·L-1·min-1
C.V(C) = 0.9mol·L-1·min-1 D.V(D) = 1.1mol·L-1·min-1
下列情况下,反应速率相同的是
| A.等体积0.1 mol/L HCl和0.05 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应 |
| B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应 |
| C.等体积等浓度HCl和CH3COOH分别与等质量的Na2CO3粉末反应 |
| D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应 |
在一个2L的容器内充入6.0mol某气态反应物,经过3s后,它的浓度变成1.2mol/L,在3s内用该反应物浓度的变化表示的反应速率为
| A.0.6mol·L—1·s—1 | B.0.8mol·L—1·s—1 |
| C.0.4mol·L—1·s—1 | D.2.4mol·L—1·s—1 |
设C+CO2 =2CO;△H>0,反应速率为v1 ;N2 +3H2 =2NH3 ;△H<0,反应速率为v2 ,对于上述反应,当温度升高时,v1 和v2 的变化情况为
| A.同时增大 | B.同时减小 | C.v1 增大,v2减小 | D.v1 减小,v2 增大 |
在 A+2B  3C+4D 反应中,表示该反应速率最快的是 ( )
3C+4D 反应中,表示该反应速率最快的是 ( )
A.v(A)=0.3 mol/(L·s) B.v(B)=0.5 mol/(L·s)
C.v(C)=0.8 mol/(L·s) D.v(D)=1 mol/(L·min)
下列叙述中,正确的是
| A.熵变大于0的反应肯定是自发的 |
| B.焓变小于0的反应肯定是自发的 |
| C.对于同一物质在不同状态时的熵值是:气态>液态>固态 |
| D.自发反应的反应速率肯定很快 |
在密闭容器中合成氨反应:N2(g)+3H2(g)  2NH3(g),在下列情况下,不能使反应速度加快的是
2NH3(g),在下列情况下,不能使反应速度加快的是
| A.加入氮气 | B.扩大容器体积,减小压强 |
| C.加入适量催化剂 | D.适当升高温度 |
将0.5 mol SO2和0.2 mol O2置于密闭容器中发生反应:2SO2+O2 2SO3。下列关于该反应的说法正确的是
2SO3。下列关于该反应的说法正确的是
| A.最终可生成0.4 mol SO3 | B.当v正(O2)= v逆(SO2) = 0时一定达化学平衡 |
| C.升高温度反应速率减小 | D.缩小体积增大压强反应速率增大 |
试题篮
()