一定温度下,容积为2 L的甲、乙两固定容积的密闭容器中,发生反应: 2SO2(g)+O2(g) 2SO3(g)。达平衡时测得有关数据如下表:
2SO3(g)。达平衡时测得有关数据如下表:
| 容 器 |
甲 |
乙 |
| 反应物投入量 |
2 mol SO2、1 mol O2 |
4 mol SO3 |
| n(SO3)/mol |
1.6 |
a |
| 反应物的转化率 |
α1 |
α2 |
下列说法正确的是( )
A.α1+α2>1
B.1.6<a<3.2
C.若甲中反应2 min时达到平衡,则2 min 内平均速率ν(O2)=" 0.2" mol·L-1·min-1
D.甲平衡后再加入0.2 mol SO2、0.2 mol O2和0.4 mol SO3,平衡逆向移动
900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应: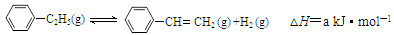 。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
。经一段时间后达到平衡。反应过程中测定的部分数据见下表:
| 时间/min |
0 |
10 |
20 |
30 |
40 |
| n(乙苯)/mol |
0.40 |
0.30 |
0.24 |
n2 |
n3 |
| n(苯乙烯)/mol |
0.00 |
0.10 |
n1 |
0.20 |
0.20 |
下列说法正确的是
A.反应在前20 min的平均速率为v(H2)=0.004mol·L-1·min-1
B.保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol·L-1,则a<0
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为50.0%
D.相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v(正)>v(逆)
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是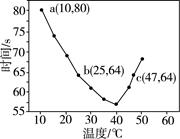
| A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反 |
| B.图中b、c两点对应的NaHSO3的反应速率相等 |
| C.图中a点对应的NaHSO3的反应速率为5.0×10-5 mol·(L·s)-1 |
| D.温度高于40 ℃时,淀粉不宜用作该实验的指示剂 |
在一定条件下CO(g)和H2(g)发生反应:CO(g)+2H2(g) CH3OH(g)。在容积固定且均为1L的a、b、c三个密闭容器中分别充入1mol CO(g)和2mol H2(g),三个容器的反应温度分别为T1、T2、T3(依次升高)且恒定不变,测得反应均进行到5min时CH3OH(g)的浓度如下图所示。下列说法正确的是
CH3OH(g)。在容积固定且均为1L的a、b、c三个密闭容器中分别充入1mol CO(g)和2mol H2(g),三个容器的反应温度分别为T1、T2、T3(依次升高)且恒定不变,测得反应均进行到5min时CH3OH(g)的浓度如下图所示。下列说法正确的是
| A.a容器中,0~5min时平均反应速率ν(H2)=0.04mol/(L.min) |
| B.反应均进行到5min时,三个容器中一定达到化学平衡状态的是b |
| C.当三个容器内的反应都达到化学平衡时,CO转化率最大的是a |
| D.保持温度和容积不变,若开始时向b容器中充入0.6mol CO(g)、1.2mol H2(g)和0.4mol CH3OH(g),则反应开始时ν(正)< ν(逆) |
一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2 2NH3,反应过程如下图所示,下列说法正确的是
2NH3,反应过程如下图所示,下列说法正确的是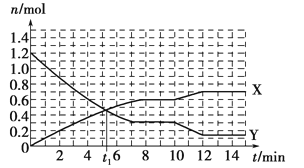
| A.t1 min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间变化的关系 |
| C.0~8 min,H2的平均反应速率v(H2)=0.75 mol·L-1·min-1 |
| D.10~12 min,N2的平均反应速率为v(N2)=0.25mol·L-1·min-1 |
将4 mol A气体和2 mol B气体在 2 L容器中混合并在一定条件下发生如下反应:2A(g)+B(g)=" 2C" (g)若经2 s后测得C的浓度为0.6 mol•L-1,现有下列几种说法,其中正确的是
①用物质A表示的反应的平均速率为0.3 mol•L-1•S-1
②用物质B表示的反应的平均速率为0.6 mol•L-1•S-1
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol•L-1
| A.①③ | B.①④ | C.②③ | D.③④ |
在373K 时,把0.5 mol N2O4气体通入体积为5 L的真空密闭容器中,立即出现红棕色。反应进行到2 s时,NO2的浓度为0.02 mol/L。在60 s时,体系已达到平衡,此时容器内压强为反应前的1.6倍。下列说法正确的是
| A.前2 s,以N2O4浓度变化表示的平均反应速率为0.01 mol·L-1·s-1 |
| B.在2 s时,体系内压强为反应前的1.1倍 |
| C.平衡时,体系内含N2O4 0.25 mol |
| D.平衡时,若往容器内充入氮气,则可提高N2O4的转化率 |
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
一定温度时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应:PCl5(g)⇌Cl2(g)
+PCl3(g)经一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
下列说法正确的是
| A.反应在前50 s内的平均速率为v(PCl3)="0.0032" moI·L-l·s-l |
| B.保持其他条件不变,若升高温度,反应重新达到平衡,平衡时c(PCl3)=0.11moI·L-l, 则正反应的△H<0 |
| C.相同温度下,若起始时向容器中充入1.0 molPCl5、0.20mol PCl3和0.20 mol Cl2,则反应达到平衡前v(正)<v(逆) |
| D.相同温度下,若起始时向容器中充入1.0mol PCl3、1.0 mol Cl2,则反应达到平衡时PCl3的转化率为80% |
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是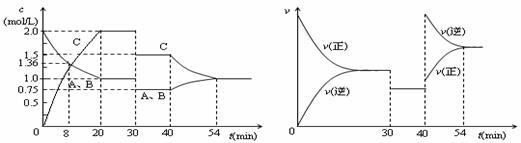
| A.第8min时 A的反应速率为0.08mol·L-1·min-1 |
| B.在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C.30min时改变的条件是降低温度,40min时改变的条件是升高温度 |
| D.反应方程式中的x=1,且正反应为放热反应 |
用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是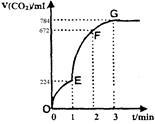
| A.OE段表示的平均速率最快 |
| B.EF段,用盐酸表示该反应的平均反应速率为0.6mol/(L·min) |
| C.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7 |
| D.G点表示收集的CO2的量最多 |
下列说法中正确的是( )
| A.Na2S2O3+2HCl==2NaCl+S↓+SO2↑+H2O在加热条件下化学反应速率增大的主要原因是该反应是吸热反应,加热使平衡向正反应方向移动 |
B.若在恒容容器中发生反应:N2+3H2 2NH3,达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动 2NH3,达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动 |
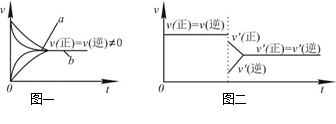
| C.在合成氨反应中,其他条件相同时,在有催化剂时(a)和无催化剂时(b)的速率—时间图像可用图一表示 |
D.若在恒压容器中发生反应:2SO3 2SO2+O2,达到平衡后再充入适量He,其速率—时间图像可用图二表示 2SO2+O2,达到平衡后再充入适量He,其速率—时间图像可用图二表示 |
下列有关化学反应原理的应用叙述中,正确的是
| A.用明矾净水是因为Al3+水解生成的Al(OH)3胶粒具有很强的吸附性 |
| B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极 |
| C.钢铁因含杂质而容易发生电化学腐蚀,所以合金都不耐腐蚀 |
| D.工业合成氨使用催化剂是为了加快反应速率和提高氨的产量 |
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示,下列结论不正确的是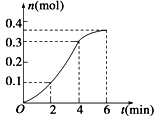
| A.反应开始2 min内平均反应速率最大 |
| B.反应速率先增大后减小 |
| C.反应2 min到第4 min内温度对反应速率的影响比浓度大 |
| D.反应在第2 min到第4 min内生成CO2的平均反应速率为前2 min的2倍 |
试题篮
()