下列做法不能使CaCO3 + 2HCl = CaCl2 + CO2á + H2O的反应速率增大的是
| A.把2mol/L盐酸换成2mol/LH2SO4 | B.碾碎碳酸钙 |
| C.适当加热 | D.增大盐酸的浓度 |
过量铁粉与100 mL 0.01 mol·L-1的稀盐酸反应。为了加快此反应速率而不改变H2的总量,可以使用如下方法中的
| A.加NaCl溶液 | B.加水 |
| C.升高温度(不考虑盐酸挥发) | D.滴入几滴浓盐酸 |
(12分)一定温度下,某容积为2 L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图所示:
(1)该反应的化学方程式是 。
(2)在图上所示的三个时刻中, (填“t1”“t2”或“t3”)时刻处于平衡状态,此时v正 v逆(填“>”“<”或“=”);0- t2时间段内v(N) = 。
(3)已知M、N均为气体,若反应容器的容积不变,则“压强不再改变” (填“能”或“不能”)作为该反应已达到平衡状态的判断依据。
(4)已知M、N均为气体,则下列措施能增大反应速率的是 (选填字母)。
| A.升高温度 | B.降低压强 |
| C.减小M的浓度 | D.将反应容器体积缩小 |
将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是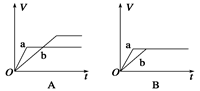
某学生为了探究足量的锌与盐酸反应过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) |
1 |
2 |
3 |
4 |
5 |
| 氢气体积(mL,标况下) |
50 |
120 |
232 |
290 |
310 |
(1)假设用V1、V2、V3、V4、V5依次表示0~1、1~2、2~3、3~4、4~5每分钟内的反应速率,则速率由大到小的排列顺序为 。
(2)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率V3= 。
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是(填编号) 。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.CuSO4溶液
用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是
| A.不用稀硫酸,改用98%浓硫酸 | B.加热 |
| C.滴加少量CuSO4溶液 | D.不用铁片,改用铁粉 |
下列条件一定能使反应速率加快的是:①增加反应物的物质的量②升高温度③缩小反应容器的体积 ④加入生成物 ⑤加入MnO2
| A.全部 | B.①②⑤ | C.② | D.①②③ |
一定量的锌粉和6mol·L-1的过量盐酸反应,当向其中加入少量的下列物质:①石墨 ②CuCl2 ③铜粉 ④铁粉 ⑤浓盐酸 ⑥硝酸时,能够加快反应速率,又不影响产生H2总量的是
| A.②④⑤ | B.①②③⑤ | C.①③⑤ | D.①③⑤⑥ |
对于以下反应:A(s)+3B(g) 2C(g)+D(g),在一定温度和容积固定的容器中,下列判断正确的是
2C(g)+D(g),在一定温度和容积固定的容器中,下列判断正确的是
| A.若反应是放热反应,升高温度,正反应速率增大 |
| B.往容器中通入稀有气体He,由于压强增大,所以反应速率增大 |
| C.往容器中加入少量A,反应速率增大 |
| D.当容器内的压强不再变化,可以判断反应已经达到平衡 |
下列有关化学反应速率的说法正确的是
| A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |
| B.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速度不变 |
| C.SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢 |
| D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢 |
某课外兴趣小组对H2O2的分解速率做了如下实验探究。
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10 mL H2O2制取150 mL O2所需的时间(秒)
①研究小组在设计方案时,考虑了浓度、 、 等因素对过氧化氢分解速率的影响。
②上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响 。
(2)将质量相同但聚集状态不同的MnO2分别加入到5mL 5%的双氧水中,并用带火星的木条测试。测定结果如下:
①写出H2O2发生的化学反应方程式 。
②实验结果说明催化剂作用的大小与 有关。
下列措施中,能加快化学反应速率的是
| A.将食物储存在冰箱里 |
| B.往H2O2溶液中加入几滴FeCl3溶液 |
| C.用块状碳酸钙代替粉末状碳酸钙与稀盐酸反应 |
| D.用0.1 mol/L H2SO4溶液代替1 mol/L H2SO4溶液与锌粒反应 |
用铁片与稀盐酸反应制取氢气时,下列措施不能使氢气生成速率增大的是
| A.给该反应体系适当加热 | B.向反应体系中加水稀释 |
| C.向反应体系中加入适量浓盐酸 | D.将铁片换成铁粉 |
已知反应N2(g) + 3H2(g) 3NH3(g) ΔH < 0,能增大正反应速率的措施是
3NH3(g) ΔH < 0,能增大正反应速率的措施是
| A.通入N2 | B.扩大容器容积 | C.移去部分NH3 | D.降低体系温度 |
试题篮
()