下列说法中不正确的是
| A.对于任何化学反应来说,反应速率越大,反应现象就越明显 |
| B.在其他条件不变时,升高温度一定会加快化学反应的反应速率 |
| C.使用合理的催化剂,可以改变化学反应速率,但不能改变化学平衡状态 |
| D.增大反应物浓度,可使单位体积内活化分子数增加,反应速率加快 |
对于反应2SO2(g)+O2(g) 2SO3(g),能增大正反应速率的措施是
2SO3(g),能增大正反应速率的措施是
| A.通入大量O2 | B.增大容器容积 |
| C.移去部分SO2 | D.降低体系温度 |
反应 A+B→C 的反应速率方程式为:v=k c (A) c (B),v为反应速率,k为速率常数。当c (A)=c (B)=1mol/L时,反应速率在数值上等于速率常数。下列说法正确的是
A.只增大c (A)时,v也增大 B.只增大c (A)时,v值不变
C.只升高温度时,k值不变 D.只升高温度时,k值变小
下列各条件下发生反应X+Y=XY时,速率最快的是
| A.常温下,20mL中含X、Y各0.003mol的溶液 |
| B.常温下,100mL中含X、Y各0.005mol的溶液 |
| C.常温下,0.1mol/L的X、Y溶液各l0mL相混合 |
| D.标准状况下,0.1mol/L的X、Y溶液各l0mL相混合 |
下列说法正确的是
| A.活化分子间所发生的碰撞为有效碰撞 |
| B.增大反应物浓度,可增大活化分子的百分数,从而使反应速率增大 |
| C.升高温度能使化学反应速率增大的主要原因是增加了单位体积内活化分子百分数 |
| D.有气体参与的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子总数,从而使反应速率增大 |
下列说法中正确的是( )
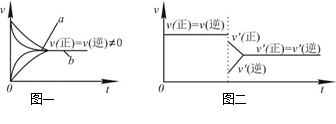
| A.Na2S2O3+2HCl==2NaCl+S↓+SO2↑+H2O在加热条件下化学反应速率增大的主要原因是该反应是吸热反应,加热使平衡向正反应方向移动 |
B.若在恒容容器中发生反应:N2+3H2 2NH3,达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动 2NH3,达到平衡后再充入适量He,由于压强增大,化学平衡向正反应方向移动 |
| C.在合成氨反应中,其他条件相同时,在有催化剂时(a)和无催化剂时(b)的速率—时间图像可用图一表示 |
D.若在恒压容器中发生反应:2SO3 2SO2+O2,达到平衡后再充入适量He,其速率—时间图像可用图二表示 2SO2+O2,达到平衡后再充入适量He,其速率—时间图像可用图二表示 |
下列说法正确的是( )
| A.Na与H2O的反应是熵增的放热反应,该反应能自发进行 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.增大压强会加快化学反应速率,其原因是增加了活化分子的百分率 |
| D.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱 |
将等质量的A、B两份过量的锌粉装入试管中,分别加入浓度和体积均相同的稀硫酸,同时向装A的试管中加入少量CuSO4溶液。如图表示产生氢气的体积V与时间t的关系,其中正确
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
| 实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
| V/mL |
c/(mol·L-1) |
V/mL |
c/(mol·L-1) |
V/mL |
||
| A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
| B |
25 |
6 |
0.2 |
5 |
0.2 |
9 |
| C |
35 |
8 |
0.15 |
10 |
0.1 |
2 |
| D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
在一定温度下,10mL0.40mol/L H2O2发生催化分解。不同时刻测定生成O2的体积(已折算为标准状况)如下表。
| t/min |
0 |
2 |
4 |
6 |
8 |
10 |
| V(O2)/mL |
0.0 |
9.9 |
17.2 |
22.4 |
26.5 |
29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:
B.6~10min的平均反应速率:
C.反应至6min时,c(H2O2)=0.3mol/L
D.反应至6min时,H2O2分解了50%
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、
KIO3(过量)酸性溶液40.0 mL混合,记录10~55 ℃间溶液变蓝时间,55 ℃时未观察到溶液变蓝,实验结果如右图。据图分析,下列判断不正确的是
| A.40 ℃之前与40 ℃之后溶液变蓝的时间随温度的变化趋势相反 |
| B.图中a点对应的NaHSO3反应速率为5.0×10-5 mol·L-1·s-1 |
| C.图中b、c两点对应的NaHSO3反应速率相等 |
| D.温度高于40 ℃时,淀粉不宜用作该实验的指示剂 |
升高温度时,化学反应速率加快,主要原因是
| A.分子运动速率加快,使该反应物分子的碰撞机会增多 |
| B.反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
| C.该化学反应的过程是吸热的 |
| D.活化能降低,活化分子百分数增加 |
一定条件下的密闭容器中,进行如下反应:NO(g)+CO(g)  1/2N2(g)+CO2(g) ΔH=-373.2 kJ/mol,为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是
1/2N2(g)+CO2(g) ΔH=-373.2 kJ/mol,为提高该反应的反应速率,缩短达到平衡的时间,下列措施不可取的是
| A.加(正)催化剂 | B.增大压强(体积减小) |
| C.给体系加热 | D.从体系中不断移去部分CO2 |
试题篮
()