科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机酸转化为氢气,氢气进入以磷酸为电解质的燃料电池发电。电池负极反应为
| A.H2+2OH--2e-=2H2O | B.O2+4H++4e-=2H2O |
| C.H2-2e-=2H+ | D.O2+2H2O+4e-=4OH- |
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。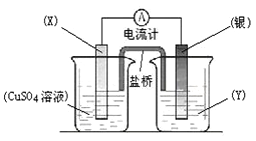
(1)电极X的材料是_____________;电解质溶液Y是_____________;
(2)银电极为电池的_________极,发生的电极反应为__________;X电极上发生的电极反应为__________;
(3)外电路中的电子是从__________电极流向_________电极(填电极材料的名称)。
在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,按下图连接。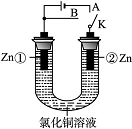
(1)如果把电键K接A,该装置应是________,Zn①为________极,Zn②的电极反应为________________。
(2)上述反应进行5 min后,转换电键K到B,则这一装置是________,Zn②为________极,Zn①的电极反应式是____________________。
(3)将Zn②换成铁片,电解质溶液换成ZnCl2饱和溶液,K接A,此时该装置为______池,阴极电极反应式为____________________________。
氯铝电池是一种新型的燃料电池,电解质溶液是KOH溶液。试回答下列问题:
(1)通入氯气的电极是__________极(填“正”或“负”);
(2)铝电极是__________极(填“正”或“负”);
(3)电子从__________(填“Al”或“Cl2”,下同)电极流向__________的电极。
在医疗上常使用一种热敷袋,袋内盛装的主要成分是:铁屑、碳粉、木屑、食盐、水等。热敷袋使用之前用塑料袋封装,使之与空气隔绝。使用时,打开塑料袋让空气进入,轻揉热敷袋,就会放出热量。使用完后,会发现袋内有许多铁锈生成。试填写下列空白:
(1)热敷袋放出的热量来源于_____________________________。
(2)铁屑、碳粉、食盐、水混合后,发生化学变化的原理是_____________________。
(3)写出使用热敷袋的过程中发生的电极反应式和有关的化学方程式:
负极:____________,正极:____________,总反应:___________________。
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )

| A.有O2放电的a极为电池的负极 |
| B.有H2放电的b极为电池的正极 |
C.a极对应的电极反应为O2+2H2O+4e- 4OH- 4OH- |
D.该电池的总反应方程式为2H2+O2 2H2O 2H2O |
在理论上不能用于设计原电池的化学反应是
| A.Al(OH)3(s)+NaOH(aq)=NaAlO2(aq)+2H2O(l) ΔH<0 |
B.C2H5OH(l)+3O2(g) 2CO2(g)+3H2O(l) ΔH<0 2CO2(g)+3H2O(l) ΔH<0 |
| C.CO2(g)+C(s)=2CO(g) ΔH>0 |
| D.H2(g)+Cl2(g)=2HCl(g) ΔH<0 |
2008北京奥运会圆满结束,其中“祥云”火炬燃料是丙烷(C3H8)气体。以丙烷、氧气和CO2及熔融碳酸盐可制作新型燃料电池,电池的总反应式为:C3H8+5O2====3CO2+4H2O。下列说法正确的是
| A.每消耗1 molC3H8可以向外电路提供12 mole- |
| B.负极通入C3H8,发生还原反应 |
| C.正极通入氧气和CO2,正极反应式是:O2+2CO2+4e-=2CO32- |
| D.CO32-移向电池的正极 |
银器的保护主要是维持它的原貌,对于轻微腐蚀蒙有硫化银的银器,可将其和铝片接触一起浸泡在稀NaOH溶液中,经一定时间污迹消失,取出后用水洗干净,再用软布或棉团擦光。有关叙述不正确的是
| A.溶液中的OH-向负极移动 |
| B.在银表面上的反应为:Ag2S+2e-=2Ag+S2- |
| C.在铝表面的反应为:Al-3e-=Al3+ |
| D.在铝表面的反应为:Al+4OH--3e-=AlO2-+2H2O |
氰(CN)2的化学性质与卤素很相似(X2),称为拟卤素,氰能和氢气反应生成HCN,其水溶液是一种酸。氰的氧化性比溴弱、比碘强。
(1)HCN分子中含有4个共价键,写出HCN的结构式:____________。
(2)KCN溶液显碱性,原因是____________(用离子方程式表示)。
(3)下列有关方程式不正确的是____________。
| A.(CN)2+2NaOH===NaCN+NaCNO+H2O |
| B.MnO2+4HCN===Mn(CN)2+(CN)2+2H2O |
| C.I2+2KCN===2KI+(CN)2 |
| D.向NaBr(aq)和KCN(aq)中加入少量Cl2:Cl2+2NaBr===2NaCl+Br2 |
(4)25℃,0.1mol/LKOH溶液和0.2mol/LHCN溶液等体积混合,若溶液最终PH=8,则c(CN-) c(HCN),原因是 。此溶液中c(CN-)与c(HCN)差值的数值为:
(5)已知HCN可以在氧气中燃烧成CO2、H2O和N2,由此原理可以设计酸性条件下原电池,书写其负极反应式: 。
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是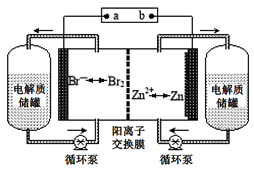
| A.阳离子交换膜可阻止Br2与Zn直接发生反应 |
| B.放电时正极的电极反应式为Br2+2e-=2Br- |
| C.充电时电极b连接电源的正极 |
| D.放电时左侧电解质储罐中的离子总浓度增大 |
运用化学反应原理研究物质的性质具有重要意义。请回答下列问题:
(1)氨气可以构成燃料电池,其电池反应原理为4NH3+3O2═2N2+6H2O。电解质为KOH溶液,则负极反应式为______________________________。
(2)向BaCl2溶液中通CO2不会出现沉淀,因此某同学根据相同的理由认为向BaCl2溶液中通入SO2也不会出现沉淀,但在实验验证中发现了异常情况,将SO2通入BaCl2溶液中开始并无沉淀,放置一段时间出现了白色沉淀,则产生该沉淀的离子反应方程式为_ 。
(3)有人认为Mg、Si的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写):___________________。
右图为某种乙醇燃料电池示意图,工作时电子流方向如图所示,下列判断正确的是
| A.X为氧气 |
| B.电极A反应式:CH3CH2OH-12e-+3H2O=2CO2+12H+ |
| C.电极材料活泼性:A>B |
| D.B电极附近溶液pH增大 |
试题篮
()